Гаг что это в медицине
Орфанные заболевания в практике педиатра: мукополисахаридоз
Mucopolysaccharidoses were considered- a group of connective tissue hereditary diseases, conditioned by disorders of glycosaminoglycan metabolism. Types of mucopolysaccharidoses were presented, as well as the main approaches to the patients treatment, a clinical example was given.
С 1 января 2012 г. в силу вступил новый Федеральный закон от 21.11.2011 № 323-ФЗ «Об основах охраны здоровья граждан в Российской Федерации», в котором впервые на государственном уровне введено понятие редких (орфанных) заболеваний. В список орфанных болезней на сегодняшний день внесено 230 наименований, однако в случае выявления новых болезней он будет пополняться. По данным Формулярного комитета Российской академии медицинских наук (РАМН), насчитывается около 300 тыс. россиян с этими болезнями.
Редкие (орфанные) заболевания — это встречающиеся с определенной частотой жизнеугрожающие или хронические прогрессирующие заболевания, при отсутствии лечения приводящие к смерти или пожизненной инвалидизации пациентов.
В разных странах определение и перечень орфанных болезней принимаются на государственном уровне, единого определения для них не существует, также как нет единого критерия отнесения заболеваний к этой группе.
В нашей стране к орфанным относятся заболевания, которые имеют распространенность не более 10 случаев заболевания на 100 000 населения.
Сегодня в мире насчитывается около 7000 редких заболеваний. Примерно половина из них обусловлена генетическими отклонениями. Симптомы могут быть очевидны с рождения или проявляться в детском возрасте.
Одним из заболеваний, включенным в группу орфанных, является мукополисахаридоз (МПС) (код по МКБ-10 Е76.1 — «нарушение обмена гликозаминогликанов», Постановление Правительства № 403 от 26 апреля 2012 г.).
Мукополисахаридоз — это группа наследственных болезней соединительной ткани, обусловленных нарушением обмена гликозаминогликанов (ГАГ) (кислых мукополисахаридов) в результате генетически обусловленной неполноценности 1 из 11 известных ферментов, участвующих в их расщеплении. Относится к лизосомным болезням накопления (табл.).
Для МПС характерно полисистемное поражение: прогрессирующие психоневрологические нарушения, гепатоспленомегалия, сердечно-легочные расстройства, костные деформации [1–3].
В Московской области зарегистрированы и получают лечение 3 ребенка с МПС: 1 девочка с МПС I типа (синдром Гурлер–Шейе) и 2 мальчика с МПС II типа (синдром Хантера). Еще два ребенка в настоящее время находятся в стадии обследования, уточняется тип МПС.
Представляем клиническую и лабораторную характеристику заболевания на примере МПС II типа.
Мукополисахаридоз II типа (синонимы: недостаточность фермента лизосомной идуронат-2-сульфатазы (a-L-идуроносульфатсульфатазы), синдром Гунтера (Хантера) — сцепленное с Х-хромосомой рецессивное заболевание, возникающее в результате снижения активности лизосомной идуронат-2-сульфатазы, участвующей в метаболизме ГАГ. Возникает почти исключительно у мальчиков (XY). У гетерозиготных женщин клинических проявлений синдрома Хантера, как правило, не наблюдается («носители»). К настоящему моменту описано лишь 2 случая заболевания у девочек, связанных с инактивацией второй, нормальной, Х-хромосомы.
Это панэтническое заболевание, частота встречаемости в мире — около 1 на 75 000 живых новорожденных мальчиков. Частота заболевания в популяции варьирует от 1 на 165 000 (Австралия) до 1 на 34 000 (Израиль). Развитие МПС II типа обусловлено мутациями в структурном гене лизосомной идуронат-2-сульфатазы — IDS, расположенном на длинном плече Х-хромосомы в локусе Xq28. В настоящее время описано более 300 различных мутаций в гене IDS. Более 50% мутаций составляют точечные мутации, около 26% — мелкие делеции и вставки, 11% — крупные делеции и перестройки гена IDS. Для пациентов России ДНК-анализ гена IDS показал, что крупные делеции и перестройки гена IDS составляют только 5,4% числа найденных мутаций.
Клинический фенотип гетерогенен и довольно условно подразделяется на тяжелую и легкую формы, различающиеся по тяжести клинических фенотипов. У пациентов с тяжелой формой наблюдают сходные с МПС I типа (синдромом Гурлер) клинические симптомы, но заболевание прогрессирует медленнее (рис.).
Заболевание манифестирует в возрасте от 1 до 3 лет. Отмечается изменение черт лица по типу гаргоилизма, задержка роста, признаки множественного костного дизостоза, огрубление и утолщение кожи, прогрессирующее снижение интеллекта. Специфичными для данного типа МПС являются изменения на коже спины, груди, шеи цвета слоновой кости, «монголоидные пятна» в пояснично-крестцовой области. Нарушения функции органов пищеварения проявляются в виде гепатомегалии, хронической диареи. Среди неврологических нарушений преобладают симптомы прогрессирующей сообщающейся гидроцефалии, спастическая параплегия в результате компрессии спинного мозга и прогрессирующая тугоухость. У детей с синдромом Хантера отмечается тугоподвижность крупных и мелких суставов. Прогрессируют сердечно-легочные расстройства. Летальный исход обычно наступает на втором десятилетии жизни.
Для подтверждения МПС II типа проводится определение уровня экскреции ГАГ с мочой и измерение активности лизосомной идуронат-2-сульфатазы в лейкоцитах или культуре кожных фибробластов. В случае заболевания в моче возрастает суммарная экскреция ГАГ.
Проведение ДНК-анализа — длительная и сложная диагностическая процедура, позволяющая определить молекулярные дефекты, приводящие к болезни Хантера, наиболее часто используется для определения носительства и пренатальной диагностики в семьях, имеющих больного ребенка. Применяются методы косвенной ДНК-диагностики, основанной на исследовании локусов Х-хромосомы, расположенных близко к гену IDS.
Кроме того, пренатальная диагностика проводится путем измерения активности идуронат-2-сульфатазы в биоптате ворсин хориона на 9–11 неделе беременности или определения спектра ГАГ в амниотической жидкости на 20–22 неделе беременности.
Наиболее часто дифференциальная диагностика проводится внутри группы МПС, а также с другими лизосомными болезнями накопления (муколипидозами, галактосиалидозом, ганглиозидозом и др.).
Основным подходом к лечению больных с МПС является проведение пожизненной ферментозаместительной терапии. При МПС II типа используется препарат идурсульфаза (Элапраза) производства компании «Шайер», США, зарегистрированный в странах Европы, США, России для лечения мукополисахаридоза II типа (болезнь Хантера). Препарат вводится еженедельно, внутривенно, капельно, медленно в дозе 2 мг/кг.
В качестве клинического примера приводим выписку из истории болезни.
Никита Б., дата рождения 11.12.2011.
Анамнез жизни. Ребенок от второй беременности (первая беременность окончилась выкидышем на раннем сроке), протекавшей на фоне маловодия, гипоксии плода, угрозы прерывания, отеков. Роды срочные, самостоятельные. Вес при рождении 4040 г, рост 58 см. С рождения на грудном вскармливании.
Формула развития: голову держит с 2 мес, переворачивается с 5 мес, сидит с 9 мес, ходит с 1 г 1 мес. К году — 5 слов. Перенесенные заболевания — острая респираторная вирусная инфекция 2 раза, трахеит.
Анамнез заболевания. С рождения — водянка оболочек яичек, с 5 мес — пахово-мошоночная грыжа, в 7 мес диагностирован кифоз поясничного отдела позвоночника, в 12 мес по данным электрокардиографии (ЭКГ) — синдром ранней реполяризации желудочков, неполная блокада правой ножки пучка Гиса (НБПНГ), в 1 г 3 мес проведена эхокардиография (Эхо-КГ), выявлена аневризма межпредсердной перегородки (МПП).
В 1 г 4 мес ребенок обследован в МГНЦ РАМН, заподозрен и подтвержден биохимическим и молекулярно-генетическим методами МПС II типа.
При поступлении в клинику состояние ребенка средней тяжести. Вес 15 кг. Рост 93 см. Волосы жесткие, тусклые, макростомия, макроглоссия, короткая шея, легкие черты гаргоилизма, камподактилия 4,5 пальца справа, широкое пупочное кольцо, кифоз поясничного отдела позвоночника, килевидная деформация грудной клетки, пахово-мошоночная грыжа слева, кожа — плотная на ощупь. Гипертрофия миндалин 2–3 ст. Дыхание через нос не затруднено. Дыхание везикулярное. Тоны сердца ритмичные, акцент второго тона. Частота сердечных сокращений (ЧСС) 120 уд./мин. Живот увеличен в объеме, печень +3,5 см, +4 см верхняя треть. Селезенка не пальпируется. Стул оформленный. Дизурических явлений нет.
Неврологический статус: в сознании, гиперактивен, быстро возбудим, говорит отдельные слова. Общемозговых, менингеальных знаков нет. Окружность головы = 50 см. Глазные щели OD = OS. Зрачки OD = OS. Движение глазных яблок в полном объеме. Низкий тембр голоса. Быстро истощается, ходит самостоятельно, легкая атаксия. Мышечная гипотония. Сухожильные рефлексы живые.
Общий анализ крови и мочи без патологических изменений.
Биохимический анализ крови — умеренное повышение уровня аланинаминотрансферазы (АЛТ) (42 Ед/л), аспартатаминотрансферазы (АСТ) (49 Ед/л).
ЭКГ: вертикальное положение электрической оси сердца (ЭОС), выраженная синусовая тахикардия 182–200 на фоне беспокойства. В ортостазе ЧСС 111–166 уд./мин.
Ультразвуковое исследование (УЗИ) брюшной полости: печень увеличена, правая доля 100 мм, левая — 45 мм. Структура однородная, стенки сосудов и протоков уплотнены. Эхогенность повышена. Поджелудочная железа 14 × 8 × 15 мм, структура неоднородная, эхогенность не изменена. Желчный пузырь — форма обычная, просвет чистый, стенки не утолщены. Селезенка не увеличена, 62 × 32 мм. Структура однородная. Почки без патологических изменений. Яички в мошонке, вагинальный отросток брюшины расширен с обеих сторон до 3 мм.
Электроэнцефалография (ЭЭГ): диффузные общемозговые изменения биоэлектрической активности по органическому типу в виде доминирования дельта-активности частотой 3–4 Гц по всем отделам конвекса безградиентно в сочетании с отдельными группами низкочастотных тета-колебаний. Эпилептиформная активность, фотопароксизмальная реакция не выявлены.
На основании комплексного исследования установлен диагноз: «Мукополисахаридоз II типа (синдром Хантера). Дегенеративное заболевание нервной системы. Задержка речевого развития. Синдром гипервозбудимости. Множественный костный дизостоз. Порок развития L1-L2 позвонков, врожденный кифоз. 2-стороннее гидроцеле. Пупочная грыжа».
По жизненным показания ребенку назначено внутривенное введение Элапразы в дозе 0,5 мг/кг еженедельно (15 кг × 0,5 = 7,5 мг на введение).
Ребенок с июля 2013 г. (возраст 1 г 7 мес) получает ферментозаместительную терапию в условиях детского отделения ГБУЗ МО МОНИКИ. В комплексную терапию включены занятия с логопедом, дефектологом, курсы физиотерапии, лечебная физкультура, L-карнитин (Элькар), Кудесан, глицин, церебролизин, Магне В6.
Литература
ГБОУ МО МОНИКИ им. М. Ф. Владимирского, Москва
Мукополисахаридозы – путь к диагнозу
Мукополисахаридозы (МПС) – это группа редких наследственных заболеваний, которые обусловлены дефицитом определенных лизосомных ферментов, участвующих в разрушении гликозаминогликанов (ГАГ), и характеризуются накоплением последних в различных органах и тканях. У части больных наблюдается медленное прогрессирование МПС, а типичные фенотипические признаки появляются в подростковом или зрелом возрасте, что в значительной степени затрудняется диагностику. Одним из типичных симптомов МПС является нарастающая тугоподвижность суставах, поэтому такие больные могут обращаться за помощью к ревматологам. Особенность поражения опорно-двигательного аппарата при МПС – отсутствие локальных и системных признаков воспаления. Важное диагностическое значение имеют системные проявления, такие как пупочная и паховая грыжа, изменение черт лица, помутнение роговицы, низкий рост, увеличение печени и селезенки, рецидивирующие инфекции дыхательных путей и средний отит и др. Для подтверждения диагноза определяют экскрецию ГАГ с мочой и активность лизосомных ферментов, а также проводят молекулярно-генетическое исследование.
Мукополисахаридозы (МПС) – это группа редких лизосомных болезней накопления, характеризующихся нарушением обмена гликозаминогликанов (ГАГ). Причиной каждого МПС является генетически обусловленный дефицит определенного лизосомного фермента, участвующего в разрушении ГАГ. Практически все МПС (за исключением МПС II) наследуются по аутосомно-рецессивному типу и с равной частотой встречаются у мальчиков и девочек. МПС II – это Х-сцепленное рецессивное заболевание, которое развивается у мальчиков, хотя описаны отдельные случаи и у девочек [1].
Накопление ГАГ в лизосомах различных тканей сопровождается разнообразными системными проявлениями, в том числе поражением опорно-двигательного аппарата, сердца, нервной системы, органа зрения и др., и приводит к прогрессирующему ухудшению функции внутренних органов. МПС в целом характеризуются тяжелым течением и неблагоприятным прогнозом, поэтому многие пациенты умирают в детском или подростковом возрасте. Однако возможно и более легкое течение заболевания, в частности МПС I и МПС VI, когда симптомы появляются в подростковом или старшем возрасте и нарастают более постепенно, а пациенты доживают до зрелого возраста [2,3]. В таких случаях диагноз нередко устанавливают с опозданием, а МПС длительно протекает под маской других болезней, прежде всего ревматических. Выделение легкого варианта течения МПС весьма условно, так как при медленном прогрессировании заболевания в конечном итоге развивается тяжелое поражение отдельных органов, которое приводит к инвалидизации пациентов и может потребовать оперативного вмешательства (например, протезирование тазобедренного сустава, имплантация искусственного клапана сердца, декомпрессия спинного мозга) [4]. МПС – это неоднородная группа заболеваний, которые имеют как общие фенотипические признаки, так и существенные различия (табл. 1, 2)
| • МПС I, II и VII – системные заболевания, поражающие различные органы и ткани, включая ЦНС; неврологические нарушения не бывают изолированными. |
| • МПС III характеризуется поражением ЦНС при отсутствии соматических проявлений. |
| • МПС IV поражает в основном опорно-двигательный аппарат и не сопровождается снижением интеллекта. |
| • При МПС VI наблюдается поражение различных органов и систем, интеллект остается нормальным. |
| Тип | Название | Фермент | Ген | Тип наследования | Лечение |
|---|---|---|---|---|---|
| МПС I | Синдромы Гурлера, Шейе или Гурлера-Шейе | α-L-идуронидаза | IDUA 4p16.3 | Аутосомно-рецессивный | Ларонидаза |
| МПС II | Синдром Хантера | Идуронат-2-сульфатаза | IDS Xq28 | X-сцепленный рецессивный | Идурсульфаза |
| МПС IIIA | Синдром Санфилиппо A | Гепаран-N-сульфатаза | SGSH 17q25.3 | Аутосомно-рецессивный | Разрабатывается |
| МПС IIIB | Синдром Санфилиппо В | α-N-ацетилглюкозаминидаза | NAGLU 17q21 | Аутосомно-рецессивный | |
| МПС IIIC | Синдром Санфилиппо С | Ацетил-КоА α-глюкозамин-ацетил-трансфераза | HGSNAT 8p11.1 | Аутосомно-рецессивный | |
| МПС IIID | Синдром Санфилиппо D | N-ацетилглюкозамин-6-сульфатаза | GNS 12q14 | Аутосомно-рецессивный | — |
| MПС IVA | Синдром Моркио А | Галактозамин-6 сульфатсульфатаза | GALNS 16q24.3 | Аутосомно-рецессивный | Элосульфаза |
| MПС IVB | Синдром Моркио В | β-Галактозидаза | GLB1 3p21.33 | Аутосомно-рецессивный | — |
| MПС VI | Синдром Марото-Лами | Арилсульфатаза B | ARSB 5q11.q13 | Аутосомно-рецессивный | Галсульфаза |
| МПС VII | Синдром Слая | β-Глюкуронидаза | GUSB 7q21.11 | Аутосомно-рецессивный | Разрабатыва |
| МПС IX | Синдром Натовича | Гиалуронидаза I | AH 3p21.3-p21.2 | Аутосомно-рецессивный | — |
Своевременная диагностика МПС сегодня приобрела особое значение, учитывая возможность заместительной терапии рекомбинантными ферментами, такими как идурсульфаза (МПС II), ларонидаза (МПС I), галсульфаза (МПС VI) и элосульфаза (МПС IVA), которые позволяют улучшить состояние больных или по крайней мере затормозить прогрессирование заболевания [5]. Ферментозаместительная терапия (ФЗТ) более эффективна, если ее начинают на более раннем этапе, когда еще отсутствуют необратимые проявления болезни.
Трудности диагностики МПС
МПС относятся к очень редким (орфанным) заболеваниям. В разных странах различные МПС регистрировали с частотой 1 на 16000-29000 живых новорожденных [6,7], а в 2007 году в Скандинавских странах распространенность МПС составила всего 4-7 случаев на 1 млн населения [8]. В связи с этим информированность врачей, особенно наблюдающих взрослых пациентов, о МПС низкая. Дополнительные сложности в диагностике возникают при более легком течении МПС, особенно при отсутствии типичных фенотипических проявлений, таких как низкий рост и характерные черты лица. Например, в зависимости от клинических проявлений и течения выделяют три формы МПС I – тяжелую (синдром Гурлера), промежуточную (синдром Гурлера-Шейе) и более легкую (синдром Шейе). Во всех случаях причиной заболевания является мутация гена, кодирующего α-L-идуронидазу. У пациентов с синдромом Гурлера симптомы появляются в раннем детском возрасте и часто наблюдается тяжелое поражение ЦНС, в то время как при синдроме Шейе симптомы менее выражены и возникают значительно позднее, а когнитивные расстройства обычно отсутствуют [9]. Два варианта течения заболевания – тяжелый и более легкий – возможны и при МПС VI (синдроме Марото–Лами), обусловленном мутациями гена, кодирующего арилсульфатазу В.
В клинике им. Е.М. Тареева за последние 3 года были обследованы 5 взрослых пациентов в возрасте от 20 до 33 лет с МПС VI. У трех из них диагноз был установлен в подростковом возрасте (от 7 до 16 лет), а у двух – в возрасте 23 и 30 лет, соответственно. Необ хо димо подчеркнуть, что хотя у двух последних пациенток наблюдалось замедленное прогрессирование заболевания, тем не менее, в обоих случаях на момент госпитализации в клинику имелось тяжелое поражение опорно-двигательного аппарата с резким ограничением подвижности в суставах, пороки клапанов сердца, стеноз шейного отдела позвоночника, нарушение проходимости дыхательных путей, поражение органа зрения и др. Обе пациентки были низкого роста (132 и 146 см) [4].
Замедленное прогрессирование течение иногда на блюдается и при МПС II (синдроме Хантера). Два года назад в нашу клинику был госпитализирован 42-летний пациент с МПС II, который был диагностирован в возрасте 13 лет на основании характерных изменений внешнего вида и наличия синдрома Хантера у старшего брата и подтвержден при энзимологическом (дефицит активности идуронат-2-сульфатазы) и молекулярногенетическом (мутация с.236С>А гена IDS в гемизиготном состоянии) исследованиях [10]. В течение длительного времени состояние пациента оставалось удовлетворительным. Успешно закончил школу, а затем институт. Работал инженером на заводе. С 30-летнего возраста прогрессирующее снижение чувствительности и боли в кистях и стопах, ухудшение зрения и выпадение центральных полей зрения, однако продолжал работать. Резкое ухудшение состояния, связанное с развитием сердечной недостаточности на фоне тяжелого порока аортального клапана, было отмечено только за год до госпитализации, т.е. в возрасте около 40 лет.
При обращении к ревматологу на МПС может указывать поражение суставов, не сопровождающееся признаками воспаления, такими как припухание, повышение СОЭ и/или уровня С-реактивного белка [12]. T. Rocha Siqueira и соавт. измеряли экскрецию ГАГ с мочой у 55 пациентов в возрасте от 3 до 21 года (в среднем 9 лет) с невоспалительной артропатией неясного генеза. У всех больных определялись дискомфорт или боль в суставах, а у 2/3 – скованность [12]. Экскре ция ГАГ была повышена у 1 из 55 больных. При дополнительном обследовании у 15-летней пациентки был установлен диагноз МПС II. Хотя очевидным ограничением этого исследования было небольшое число обследованных пациентов, тем не менее, полученные данные указывают на возможную роль скрининга в диагностике более легких форм МПС.
Как заподозрить МПС?
В настоящее время известно 11 лизосомных ферментов, дефицит которых приводит к развитию 7 типов МПС [13]. Замедленное прогрессирование заболевания и более поздняя диагностика чаще отмечаются у пациентов с МПС I, IV, VI и VII, в то время как другие типы МПС обычно характеризуются тяжелым течением и более короткой продолжительностью жизни. Следует отметить, что в задачи практического врача не входит дифференциальная диагностика различных МПС – вполне достаточно заподозрить этот диагноз и направить пациента на консультацию к генетику и/или провести скрининговое исследование (определение экскреции ГАГ с мочой).
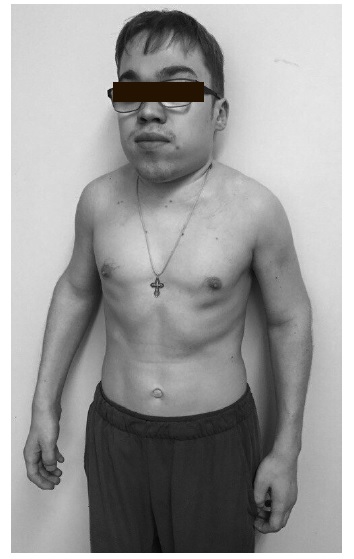
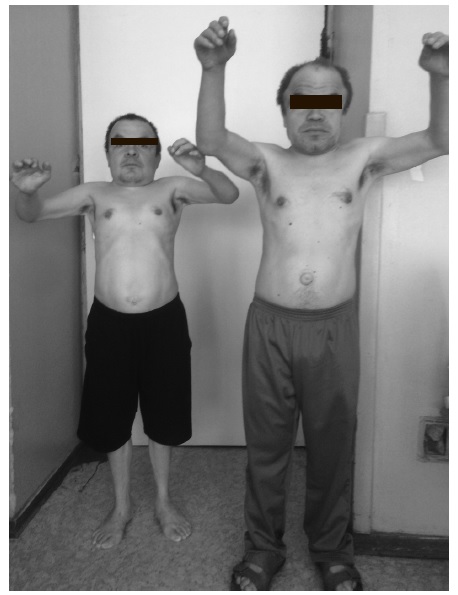
Хотя МПС представляют собой неоднородную группу болезней и отличаются по тяжести течения и частоте поражения центральной нервной системы, тем не менее, в целом клинические проявления некоторых из них достаточно однотипны и позволяют предположить наличие заболевания, особенно у пациентов старшего возраста при наличии типичного фенотипа. При осмотре пациентов с МПС прежде всего обращают на себя внимание низкий рост, непропорциональное строение скелета (короткие туловище и шея, длинные конечности), а также грубые черты лица, толстые губы, увеличение языка, запавшее переносье, увеличение расстояния между глазами (гипертелоризм) (рис. 1, 2). При тяжелом течении МПС рост пациентов не превышает 95-100 см, хотя при медленном развитии заболевания может достигать 140-150 см. Например, в нашей серии наблюдений рост 5 взрослых пациентов с МПС VI варьировался от 132 до 153 см, а рост 42-летнего пациента с МПС II составлял 158 см. В крупном исследовании среди 121 пациента с МПС VI доля взрослых составляла около 25% [14]. Средний рост больных в возрасте 19-24 и 25-56 лет равнялся 142,7±20,1 и 157,0±8,5 см, соответственно. Таким образом, по крайней мере у части больных МПС рост может быть фактически нормальным.
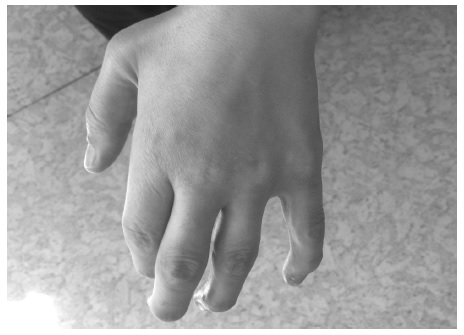
При всех МПС развивается тяжелое поражение опорно-двигательного аппарата (множественный дизостоз), которое проявляется тугоподвижностью и контрактурами суставов (в большей степени ухудшается разгибание), деформацией кистей (“когтистая лапа”) (рис. 3) и позвоночника (кифоз, сколиоз), воронкообразной грудной клеткой. Наблю даются недоразвитие таза, дисплазия головок бедренных костей и вальгусное положение шейки бедренной кости. Ограничение подвижности суставов отмечается уже в детском или подростковом возрасте, постепенно нарастает и в конечном итоге служит причиной инвалидизации больных.
Для МПС IV (синдрома Моркио), в отличие от других типов МПС, типично развитие гипермобильности суставов, обусловленной деформацией метафизов, гипоплазией костей и деградацией соединительной ткани, окружающей суставы [15].
У пациентов с МПС часто наблюдаются обструкция глотки, верхних и нижних дыхательных путей, связанная с увеличением языка и миндалин, сужением трахеи, утолщением надгортанника и голосовых связок, отложением ГАГ в слизистой оболочке бронхов. Обструкция дыхательных путей сопровождается затрудненным дыханием и громким храпом с эпизодами апноэ во время сна. Характерно развитие рецидивирующего среднего отита, вызывающего прогрессирующую тухоугость, которая обусловлена как кондуктивными, так и нейросенсорными механизмами. Причинами нарушения функции дыхания могут быть также небольшие размеры и малоподвижность грудной клетки, растя жение живота в сочетании с кифозом, сколиозом и значительным поясничным лордозом, а также рецидивирующие инфекции нижних дыхательных путей.
Еще одно типичное проявление МПС – поражение клапанов сердца, частота которого достигает 60-90%. С. Wippermann и соавт. обследовали 84 больных в возрасте от 1 до 47 лет с различными типами МПС [16]. Частота недостаточности митрального и/или аортального клапана составила 75,0%, однако тяжелая митральная или аортальная регургитация наблюдалась только в 4,8% и 8,3% случаев, соответственно. Частота пороков клапанов сердца достигала 89-100% у больных МПС I, II и VI, но была ниже у пациентов с МПС III и IV – 3366%. В другом исследовании у 28 больных МПС VI частота поражения митрального клапана составила 96%, трикуспидального – 71% и аортального – 43% [17]. Следует отметить, что, в отличие от некоторых других лизосомных болезней накопления, таких как болезнь Фабри, для МПС не характерно тяжелое поражение миокарда.
У большинства больных МПС I, VI и VII часто отмечается помутнение роговицы, в то время как при других типах МПС оно отсутствует [18].
У пациентов с тяжелыми формами МПС I и II наб лю дается поражение ЦНС (поведенческие расстрои ̆ства, задержка умственного развития, ухудшение интеллекта, тяжелая когнитивная дисфункция) [10]. Выраженные неврологические и когнитивные расстройства характерны также для МПС III. В то же время у большинства пациентов с МПС VI сохраняется нормальный интеллект.
МПС I, II и VI могут привести к развитию синдрома запястного канала, проявляющегося стойкой болью и онемением пальцев кисти в результате сдавления срединного нерва между костями и сухожилиями мышц запястья. Возможно также сдавление спинного мозга вследствие сужения спинно-мозгового канала и нестабильности атлантоаксиального канала. Компрессион ная миелопатия может осложниться слабостью в нижних конечностях и спастической параплегией или квадриплегией.
Диагноз и дифференциальный диагноз
Алгоритм диагностики и дифференциальной диагностики МПС у пациентов с поражением опорно-двигательного аппарата представлен на рис. 4 [19]. Если контрактуры суставов определяются у новорожденного ребенка, то наиболее вероятен диагноз артрогрипоза – заболевания, характеризующегося врожденными контрактурами двух и более суставов несмежных областей в сочетании с мышечной гипо- или атрофией. Различают артрогрипоз с поражением верхних и/или нижних конечностей, генерализованный и дистальный варианты. Артрогрипоз – это не самостоятельная нозологическая форма, а скорее физический симптом, который может быть обусловлен различными причинами, например, ограничением движений плода во время его развития (многоводие, маловодие, пороки развития и опухоли матки, многоплодная беременность), нарушением развития мышц (вирусные инфекции), генетическими факторами и др.
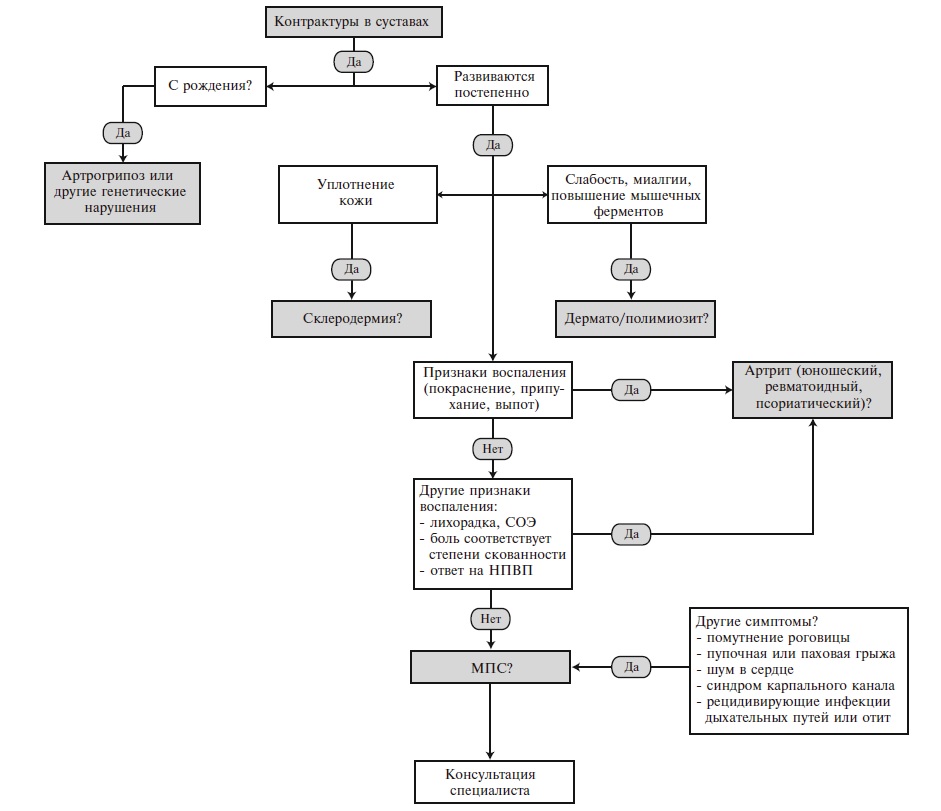
Боли и тугоподвижность суставов, появляющиеся в детском или подростковом возрасте, могут имитировать ревматические заболевания, в частности юношеский идиопатический артрит, ревматоидный или псориатический артрит. Основное значение для дифференциальной диагностики с этими заболеваниями имеют отсутствие воспалительной боли (т.е. боли, возникающей по утрам и сопровождающейся скованностью, которая уменьшается на фоне физической активности), локальных (припухание и болезненность при пальпации суставов) и системных (повышение температуры тела и/или СОЭ и уровня С-реактивного белка) признаков воспаления (рис. 4) [19]. Глюкокортикостероиды неэффективны, хотя нестероидные противовоспалительные препараты могут несколько уменьшить имеющиеся симптомы.
Признаки поражения суставов, появляющиеся в более старшем возрасте, часто расценивают как первичный остеоартроз. Дифференцировать поражение опорно-двигательного аппарата при МПС с этим забо леванием позволяют развитие артропатии в подростковом или молодом возрасте при отсутствии факторов риска первичного остеоартроза и наличие других типичных проявлений генетического заболевания (карликовый рост, измененные черты лица, порок клапана сердца, помутнение роговицы и т.п.) (табл. 3).
| Поражение опорно-двигательного аппарата |
| Контрактуры суставов, развивающиеся в раннем возрасте и не сопровождающиеся признаками воспаления или эрозивными изменениями костей |
| “Когтистая лапа” |
| Деформация позвоночника (сколиоз, кифоз, лордоз) |
| Рентгенологические признаки множественного дизостоза |
| Другие клинические проявления |
| Нарастающая “грубость” черт лица |
| Помутнение роговицы |
| Короткая ригидная шея |
| Частые респираторные инфекции, рецидивирующий средний отит, заложенность носа, шумное дыхание/храп |
| Шум в сердце |
| Пупочные и/или паховые грыжи |
| Низкий рост |
| Нарушение походки |
| Увеличение живота за счет печени и селезенки |
Скрининговым методом диагностики МПС является измерение экскреции ГАГ с мочой. Определение типа ГАГ в моче (дерматансульфат, гепарансульфат, хондороитинсульфат и кератансульфат) с помощью тонкослойной хроматографии или электрофореза имеет определенное значение для дифференциальной диагностики МПС, однако результаты этих исследований все же не позволяют установить окончательный диагноз. Экскреция ГАГ с мочой у детей, подростков и молодых людей с МПС обычно превышает таковую у здоровых людей сопоставимого возраста [13]. Однако у взрослых людей с МПС, особенно с более легкими и медленно прогрессирующими формами заболевания, она может оказаться близкой к норме. Соответственно, следует осторожно интерпретировать результаты этих тестов и продолжать обследование, если диагноз МПС представляется вероятным на основании клинических данных.
Следующий этап диагностики – определение активности лизосомных ферментов в высушенных пятнах крови, лейкоцитах или фибробластах. Анализ высушенных пятен крови обычно проводят в тех случаях, когда образец необходимо отправить в лабораторию, находящуюся в другом городе или стране. Более надежным считают исследование лейкоцитов, выделенных из цельной крови, или культивированных фибробластов.
Для подтверждения диагноза проводят молекулярногенетическое исследование, которое необходимо также для выявления носителей мутантных генов и пренатальной диагностики.
Лечение мукополисахаридозов
Для патогенетической терапии МПС применяют рекомбинантные формы ферментов, дефицит которых лежит в основе развития соответствующего заболевания, в том числе ларонидазу для лечения МПС I, идурсульфазу – МПС II, галсульфазу – МПС VI, элосульфазу альфа – МПС IVa (в Российской Федерации последний препарат не зарегистрирован). Все препараты предназначены для внутривенного введения. Их эффективность и безопасность установлены как в рандомизированных, двойных слепых, плацебо-контролируемых исследованиях, так и длительных наб людательных исследованиях, позволивших изучить отдаленные эффекы ФЗТ [20].
Эффективность и безопасность галсульфазы оценивали в рандомизированном, двойном слепом, плацебоконтролируемом, 24-недельном исследовании 3 фазы у 39 больных МПС VI [21]. Критериями эффективности были толерантность к физической нагрузке и экскреция ГАГ с мочой. Лечение галсульфазой в течение 24 недель по сравнению с плацебо привело к значительному увеличению пройденной за 12 минут дистанции (р=0,025) и скорости подъема по лестнице (р=0,053) и достоверному снижению экскреции ГАГ с мочой (p
Заключение
МПС – это группа редких заболеваний, которые обычно диагностируют поздно вследствие низкой информированности врачей о лизосомных болезнях накопления. Наибольшие диагностические трудности возникают при более легких формах МПС, которые характеризуются медленным развитием соматических проявлений и стертостью типичных внешних признаков. Выделение легких, или ослабленных (attenuated), форм МПС весьма условно, так как в конечном итоге у таких больных развиваются инвалидизирующие осложения, часто требующие оперативного лечения. Одним из типичных симптомов МПС I, II и VI является нарастающая тугоподвижность в суставах, поэтому такие больные могут обращаться за помощью к ревматологам. Особенность поражения опорно-двигательного аппарата при МПС – отсутствие локальных (припухания суставов и болезненности при их пальпации) и системных (повышения температуры тела и/или СОЭ и уровня С-реактивного белка) признаков воспаления. Исключить остеоартроз позволяют молодой возраст пациента и отсутствие типичных факторов риска дегенеративных заболеваний суставов. Важное диагностическое значение имеют системные проявления, такие как пупочная и паховая грыжа, изменение черт лица, помутнение роговицы, низкий рост, увеличение печени и селезенки, рецидивирующие инфекции дыхательных путей и средний отит и др. Если заподозрен диагноз МПС, то необходимо определить экскрецию ГАГ с мочой, а также измерить активность лизосомных ферментов и провести молекулярно-генетическое исследование для подтверждения диагноза.
.gif)
.png)