Геморрагическим синдромом что это
Что такое геморрагическая лихорадка с почечным синдромом (ГЛПС)? Причины возникновения, диагностику и методы лечения разберем в статье доктора Александрова Павла Андреевича, инфекциониста со стажем в 13 лет.
Определение болезни. Причины заболевания
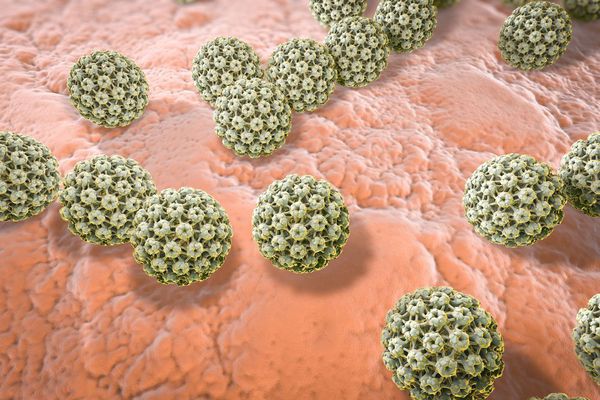
Геморрагическая лихорадка с почечным синдромом (ГЛПС) — это группа острых инфекционных заболеваний, вызываемых хантавирусами из семейства Bunyaviridae, которые поражают мелкие сосуды всего организма, вызывают расстройства свёртывающей системы, нарушают кровообращение и работу почек. Клинически проявляется в виде общей инфекционной интоксикации, воспаления соединительной ткани почек, не поддающегося лечению антибиотиками, и геморрагического диатеза (повышенной кровоточивости тканей). В зависимости от формы заболевания летальность колеблется от 1 % до 15 %.
Синонимы: дальневосточная или корейская геморрагическая лихорадка, геморрагический нефрозонефрит, скандинавская эпидемическая нефропатия и др.
Этиология
Таксономия возбудителя болезни:
Определение ГЛПС как вирусной болезни было предложено советским бактериологом, вирусологом и иммунологом А. А. Смородинцевым в 1944 году. Сам вирус был выделен от животных южно-корейским учёным Н. W. Lee в 1976 году, от человека — в 1978 году.
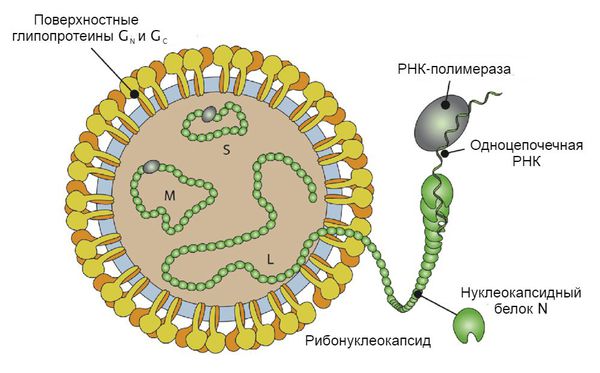
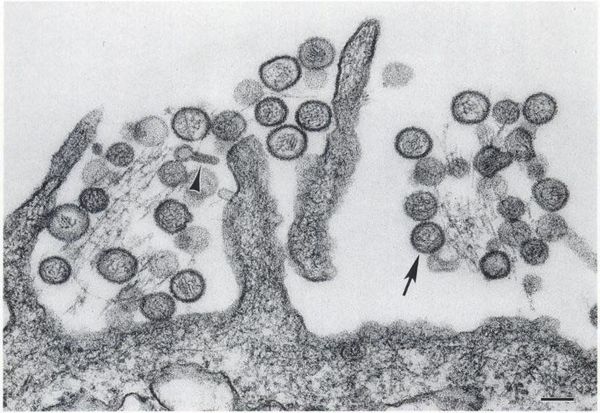
Вирусные частицы представляют собой образования округлой формы диаметром 90-130 нм. Они имеют липидную оболочку с выступами (гликопротеиновыми шипами), содержат одноцепочечную РНК. Геномом кодируются: РНК-зависимая РНК-полимераза, нуклеокапсидный белок N, поверхностные глипопротеины GN GC. В зависимости от вида вируса имеется различное количество открытых рамок считывания, кодирующих неструктурные белки. Проникновение вируса в клетку хозяина осуществляется путём прикрепления к её поверхности с помощью специфических белков G.
Интересен тот факт, что мутации хантавирусов при репликации проходят параллельно с эволюционными изменениями их природных носителей (грызунов).
Эпидемиология
Все перечисленные возбудители также могут циркулировать повсеместно в незначительной концентрации.
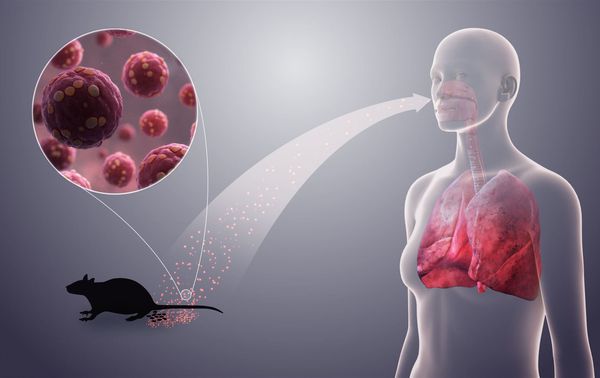
Заболевание является природно-очаговым зоонозом, т. е. встречается на определённых территориях, где есть основной источник инфекции — дикие мышевидные грызуны:
В городах незначительная роль отводится домовым мышам и крысам. Сами грызуны, как правило, являются бессимптомными вирусоносителями (вирусные частицы выявляются у них во всех средах организма, но больше — в лёгких).
Заражение грызунов происходит при контакте между собой, в основном через слюну воздушно-капельным путём. Человек в основном заражается через мочу и фекалии грызунов, содержащие вирус.
Механизмы передачи вируса :
Человек обычно не является источником инфекции, для окружающих не заразен (случаи заражения крайне редки и наблюдаются только в лаборатории).
К заболеванию восприимчивы все люди, чаще всего болеют мужчины активного возраста, связанные с определёнными профессиями или образом жизни (фермеры, ассенизаторы, трактористы, лесники, геологи, дачники, работники промышленных предприятий). Дети, женщины и пожилые люди болеют значительно реже в связи с меньшим контактом с источниками вируса в природной среде и особенностями иммунитета (если человек уже контактировал с вирусом).
Сезонность — летне-осенняя, раз в 3-4 года заболеваемость увеличивается из-за активизация грызунов, обитающих рядом с людьми.
Симптомы геморрагической лихорадки с почечным синдромом
Инкубационный период составляет от 4 до 49 дней. В среднем он длится 2-3 недели. Его продолжительность зависит от вида возбудителя, дозы попавшего в организм патогена, места проникновения, иммунореактивности организма и др.
Подавляющее большинство случаев протекает под маской лёгкого и среднетяжёлого ОРЗ в виде непродолжительной остролихорадочной формы и, как правило, не распознаются.
Начало заболевания (лихорадочный период) обычно острое, иногда наблюдается небольшая продрома в виде познабливания, ломоты в теле, повышения температуры тела до 37,5-38°С. Появляется лихорадка с быстрым нарастанием температурной реакции до максимальных цифр (38-40°С), которые держатся в течение 5-11 дней. Колебания температурной кривой не имеют каких-либо особенностей. Больных беспокоит озноб, выраженная головная боль, ломота и боли в мышцах и суставах, сухость во рту и жажда. Быстро нарастает слабость, потливость, адинамия. Может возникнуть небольшой кашель.
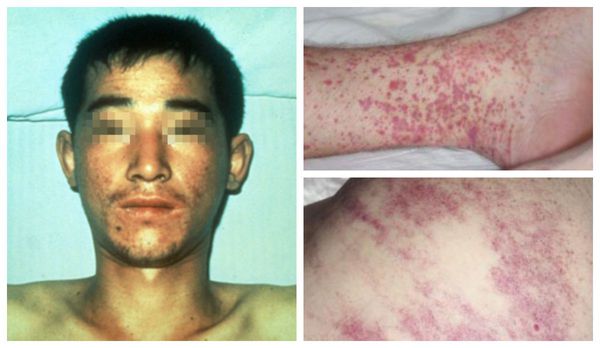
Внешний вид больных : гиперемированная (покрасневшая) верхняя половина тела, инъецированные красноватые склеры (белки глаз), возможна пятнистая энантема мягкого нёба (появление мелких пятен). При прогрессировании болезни появляется петехиальная сыпь (мелкие кровоизлияния) в области туловища, внутренней поверхности плеч и местах уколов, возможны небольшие носовые кровотечения. При сдавливании тканей и щипках в этих местах появляется геморрагическая сыпь.
Со стороны сердца отмечается относительная брадикардия, артериальное давление немного снижено. У чувствительных людей может возникнуть дискомфорт в поясничной области. К концу лихорадочного периода начинает снижаться количество отделяемой мочи (диурез) и частота мочеиспускания.
Внешний вид пациента изменяется : гиперемия лица и верхней части туловища сменяется бледностью, нарастает геморрагический синдром: возникают массивные кровоизлияния в склеры, длительные носовые кровотечения, любое прижатие ткани вызывает выраженную геморрагическую сыпь. Возможно развитие кишечного кровотечения.
Ведущим расстройством олигурической стадии является прогрессирующее снижение количества отделяемой мочи вплоть до анурии (полного её отсутствия). В это время наиболее часто развиваются осложнения и летальные исходы.
Признаки потенциального развития тяжёлой формы болезни :
ГЛПС у беременных
Заболевание протекает несколько тяжелее, чаще переходит в тяжёлую стадию и повышает риск осложнений. Оно способно привести к развитию дистресс-синдрома лёгких, тромбоцитопении и повышению уровня печёночных трансаминаз.
Патогенез геморрагической лихорадки с почечным синдромом
Входные ворота — эпителий дыхательных путей, желудочно-кишечный тракт и повреждённая кожа. В месте проникновения вируса никаких изменений не наблюдается. По кровеносным сосудам патоген распространяется в организме, накапливаясь в клетках макрофагальной ткани, не вызывая при этом никаких симптомов.
По истечению скрытого периода заболевания происходит массивная вирусемия — выход и циркуляция вируса в крови. Она сопровождается активацией иммунной и гормональной систем, которые запускают синтез провоспалительных цитокинов. В результате прямого повреждающего воздействия вируса и иммунопатологических сдвигов повреждается внутренний слой мелких сосудов («излюбленное» место поражения вируса), развивается повышенное слипание тромбоцитов и клеточных элементов, вследствие чего нарушается текучесть крови. Такие изменения приводят к нарушению микроциркуляции, спазму мелких сосудов и нарушению работы органов. Одновременно с этим начинается образование патологических иммунных клеток (аутоиммунная агрессия).
При прогрессировании болезни расстройства микроциркуляции усиливаются, что приводит к системному расстройству гемодинамики, нарушается кровоснабжение органов, нарастает гипоксия, увеличивается кислотность (ацидоз), повреждается структура и функции жизненно важных органов (отёки, кровоизлияния, дистрофия, некроз).
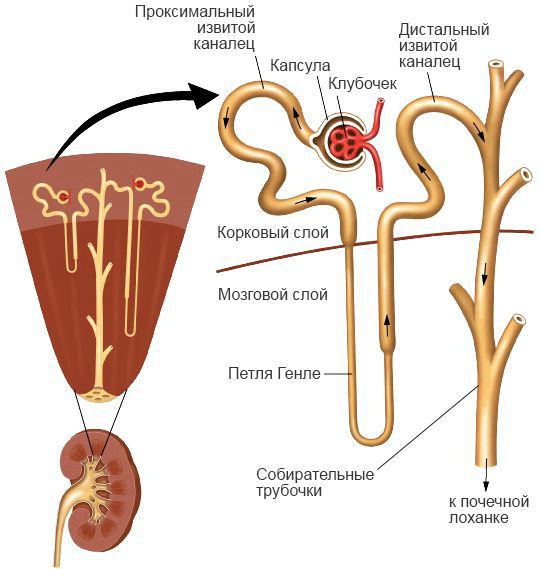
Наиболее выраженные поражения наблюдаются в почках — нарушается микроциркуляция, повышается проницаемость стенки сосудов, на базальной мембране клубочков осаждаются патологические иммунные комплексы. Это ведёт к отёку промежуточного вещества, дистрофии, пропотеванию фибрина и белка в просвет канальцев почек и их обтурацией (закупоркой) — нарушается фильтрация, нарастает ишемия ткани почек и возникает некроз. Это приводит к уменьшению количества отделяемой мочи, нарушению водно-электролитного баланса, уремической интоксикации и ацидозу. Чем тяжелее процесс, тем больше объёмы поражения, что может привести к летальному исходу.
Классификация и стадии развития геморрагической лихорадки с почечным синдромом
В Международной классификации болезней (МКБ-10), заболеванию присвоен код A 98.5.
Выделяют три степени тяжести:
Осложнения геморрагической лихорадки с почечным синдромом
Специфические осложнения ГЛПС :
Неспецифические осложнения ГЛПС — воспалительно-гнойные процессы:
Диагностика геморрагической лихорадки с почечным синдромом
К методам диагностики ГЛПС относятся:
Дифференциальная диагностика
Большинство случаев болезни проходят в лёгкой и среднетяжёлой форме, поэтому, как правило, не распознаются, ошибочно принимаясь за начальный период ОРЗ. Также ГЛПС можно спутать с другими заболеваниями:
Лечение геморрагической лихорадки с почечным синдромом
Лёгкие и многие формы среднетяжёлых случаев болезни лечат дома или в отделении ОРЗ стационаров как нераспознанные случаи. Часть среднетяжёлых и тяжёлых случаев подлежат госпитализации в инфекционные стационары с наличием отделения реанимации и интенсивной терапии (ОРИТ), при отсутствии инфекционного стационара — в общетерапевтический. Транспортировка должна осуществляться без тряски, так как есть риск разрыва почек.
Режим — постельный, до прекращения выраженной полиурии:
Показана механически и химически щадящая диета с достаточным количеством соли. Наиболее подходит диета № 4 по Певзнеру. Необходимо контролировать уровень потребляемой жидкости. В начале болезни, когда функция почек сохранена, показано обильное питьё. В фазу олигоанурии нужно строго следить, чтобы количество потреблённой жидкости не превышало объёма выведенной более чем на 700 мл. В разгар болезни нужно исключить продукты, богатые белком (мясо, рыбу, бобовые) и калием (овощи, фрукты, сухофрукты, картофель). В период выздоровления их нужно включить в рацион. Голодать нельзя, так как оно усиливает распада белка и увеличивает уровень мочевины в крови (азотемия).
Специфической противовирусной терапии прямого действия на сегодняшний день нет. В ранние сроки болезни при среднетяжёлых и тяжёлых формах возможно применение препарата общевирусного действия ( рибавирина ) коротким курсом.
В период выздоровления показано использование общеукрепляющих средств и адаптогенов: минеральных препаратов (например глюконат кальция ), витаминных комплексов и растительных экстрактов (например элеутерококка ).
Сроки выписки пациентов :
Прогноз. Профилактика
При лёгких формах и большей части среднетяжёлых форм прогноз благоприятный: через 3-6 недель наблюдается полное выздоровление. При части среднетяжёлых и тяжёлых формах процесс восстановления может занять месяцы, иногда годы, возможно стойкое нарушение функции некоторых органов (в основном почек). При развитии осложнений нередки летальные исходы (в основном при ГЛПС, вызванной вирусом Хантаан).
Профилактика ГЛПС на современном этапе включает в основном неспецифические мероприятия:
Геморрагические диатезы и синдромы
Геморрагические диатезы и синдромы — формы патологии, характеризующиеся склонностью к кровоточивости.
Этиология, патогенез. Различают наследственные (семейные) формы с многолетней, начинающейся с детского возраста кровоточивостью и приобретенные формы в большинстве своем вторичные (симптоматические). Большая часть наследственных форм связана с аномалиями мегакариоцитов и тромбоцитов, дисфункцией последних либо с дефицитом или дефектом плазменных факторов свертывания крови, а также фактора Виллебранда, реже — с неполноценностью мелких кровеносных сосудов (телеангиэктазия, болезнь Ослера-Рандю). Большинство приобретенных форм кровоточивости связано с синдромом ДВС, иммунными и иммунокомплексными поражениями сосудистой стенки (васкулит Шенлейна-Геноха, эритемы и др.) и тромбоцитов (большинство тромбоцитопений), с нарушениями нормального гемопоэза (геморрагии при лейкозах, гипо- и апластических состояниях кроветворения, лучевой болезни), токсикоинфекционным поражением кровеносных сосудов (геморрагические лихорадки, сыпной тиф и др.), заболеваниями печени и обтурационной желтухой (ведущими к нарушению синтеза в гепатоцитах факторов свертывания крови), воздействием лекарственных препаратов, нарушающих гемостаз (дезагреганты, антикоагулянты, фибринолитики) либо провоцирующих иммунные нарушения — тромбоцитопению (гаптеновая форма), васкулиты. При многих перечисленных заболеваниях нарушения гемостаза носят смешанный характер и резко усиливаются в связи с вторичным развитием синдрома ДВС, чаще всего в связи с инфекционно-септическими, иммунными, деструктивными или опухолевыми (включая лейкозы) процессами.
По патогенезу различают следующие группы геморрагических диатезов:
В особую группу включают различные формы так называемой невротической, или имитационной, кровоточивости, вызываемой у себя самими больными вследствие расстройства психики путем механической травматизации ткани (нащипывание или насасывание синяков, травмирование слизистых оболочек и т. д.), тайным приемом лекарственных препаратов геморрагического действия (чаще всего антикоагулянтов непрямого действия — кумаринов, фенилина и др.), самоистязанием или садизмом на эротической почве и т. д.
Реже встречаются близкие к ДВС-синдрому тромбогеморрагические заболевания, протекающие с выраженной лихорадкой — тромботическая тромбоцитопеническая пурпура (болезнь Мошкович) и гемопитико-уремический синдром.
Общая диагностика геморрагических заболеваний и синдромов базируется на следующих основных критериях:
Типы кровоточивости
Гематомный тип свойствен ряду наследственных нарушений свертываемости крови (гемофилии А и В, тяжелый дефицит фактора VII) и прибретенных коагулопатий — появлению в крови ингибиторов факторов VIII, IX, VIII + V, передозировке антикоагулянтов (забрюшинные гематомы). Характеризуется болезненными напряженными кровоизлияниями в подкожную клетчатку, мышцы, крупные суставы, в брюшину и забрюшинное пространство (со сдавлением нервов, разрушением хрящей, костной ткани, нарушением функций опорно-двигательного аппарата), в некоторых случаях — почечными и желудочно-кишечными кровотечениями, длительными анемизирующими кровотечениями из мест порезов, ран, после удаления зубов и хирургических вмешательств.
Капиллярный, или микроциркуляторный (петехиально-синячковый), тип свойствен тромбоцитопениям и тромбоцитопатиям, болезни Виллебранда, а также дефициту факторов протромбинового комплекса (VII, X, V и II), некоторым вариантам гипо- и дисфибриногенемий, умеренной передозировке антикоагулянтов. Часто сочетается с кровоточивостью слизистых оболочек, меноррагиями. Возможны тяжелые кровоизлияния в мозг.
Смешанный капиллярно-гематомный тип кровоточивости — петехиально-пятнистые кровоизлияния в сочетании с обширными плотными кровоизлияниями и гематомами. При наследственном генезе кровоточивости этот тип свойствен тяжелому дефициту факторов VII и XIII, тяжелым формам, болезни Виллебранда, а из приобретенных — характерен для острых и подострых форм ДВС-синдрома, значительной передозировке антикоагулянтов. При дифференциальной диагностике следует учитывать и большие различия в частоте и распространенности геморрагических диатезов, одни из которых исключительно редки, тогда как на другие приходится подавляющее большинство встречающихся в клинической практике случаев кровоточивости.
Геморрагические диатезы, обусловленные нарушениями в свертывающей системе крови. Среди наследственных форм подавляющее большинство случаев (более 95%) приходится на дефицит компонентов фактора VIII (гемофилия А, болезнь Виллебранда) и фактора IX (гемофилия В), по 0,3-1,5% — на дефицит факторов VII, X, V и XI. Крайне редки (единичные наблюдения) формы, связанные с наследственным дефицитом других факторов — XII СцефектХагемана), II (гипоп-ротромбинемия), I (гиподисфибриногенемия), XIII (дефицит фибринстабилизирующего фактора). Среди приобретенных форм, помимо ДВС синдрома, преобладают коагулопатии, связанные с дефицитом или депрессией факторов протромбинового комплекса (II, VII, X, V), — болезни печени, обтурационная желтуха, кишечные дисбактериозы, передозировка антикоагулянтов — антагонистов витамина К (кумарины, фенилин и др.), геморрагическая болезнь новорожденных; формы, связанные с появлением в крови иммунных ингибиторов факторов свертывания (чаще всего антител к фактору VIII); кровоточивость, обусловленная гепаринизацией, введением препаратов фибринолитического (стрептокиназа, урокиназа и др.) и дефибринирующего действия (арвин, анкрод, дефибраза, рептилаза, анцистрон-Н).
Гемофилии. Гемофилия А и В-рецессивно наследуемые, сцепленные с полом (Х-хромосомой) заболевания; болеют лица мужского пола, женщины являются передатчицами заболевания. Генетические дефекты характеризуются недостаточным синтезом или аномалией факторов VIII (коагуляционная часть) — гемофилия А или фактора IX — гемофилия В. Временный (от нескольких недель до нескольких месяцев) приобретенный дефицит факторов VIII, реже — IX, сопровождающийся сильной кровоточивостью, наблюдается и у мужчин, и у женщин (особенно в послеродовом периоде, у лиц с иммунными заболеваниями) вследствие появления в крови в высоком титре антител к этим факторам.
Патогенез. В основе крйвоточивости лежит изолированное нарушение начального этапа внутреннего механизма свертывания крови, вследствие чего резко удлиняется общее время свертывания цельной крови (в том числе параметр R тромбоэластограммы) и показатели более чувствительных тестов — аутокоагуляционного (АКТ), активированного парциального тромбопластинового времени (АПТВ) и т. д. Протромбиновое время (индекс) и конечный этап свертывания, а также все параметры тромбоцитарного гемостаза (число тромбоцитов и все виды их агрегации) не нарушаются. Пробы на ломкость микрососудов (манжеточная и др.) остаются нормальными.
Клиническая картина. Гематомный тип кровоточивости с раннего детского возраста у лиц мужского пола, обильные и длительные кровотечения после любых, даже малых, травм и операций, включая экстракцию зубов, прикусы губ и языка и т. д. Характерны повторяющиеся кровоизлияния в крупные суставы конечностей (коленные, голеностопные и др.) с последующим развитием хронических артрозов с деформацией и ограничением подвижности суставов, атрофией мышц и контрактурами, инвалидизирующих больных, заставляющих их пользоваться ортопедической коррекцией, костылями, инвалидными колясками. Возможны большие межмышечные, внутримышечные, поднадкостничные и забрюшинные гематомы, вызывающие иногда деструкцию подлежащей костной ткани (гемофилические псевдоопухоли), патологические переломы костей. Возможны упорные рецидивирующие желудочно-кишечные и почечные кровотечения. Тяжесть заболевания соответствует степени дефицита анти-гемофилических факторов: при крайне тяжелых формах их уровень чиже 1%, при тяжелых — 1–2%, средней тяжести — 3–5%, легкой — больше 5%. Однако при травмах и операциях угроза развития опасных для жизни кровотечений сохраняется и при легких формах гемофилии, и лишь поддержание уровня факторов VIII или IX выше 30–50% обеспечивает надежный гемостаз.
Диагноз. Гемофилию предполагают у больных мужского пола с гематомным типом кровоточивости и гемартрозами, возникающими с раннего детства. Лабораторные признаки: удлинение общего времени свертывания крови при нормальных показателях протромбинового и тромбинового тестов. Для дифференциальной диагностики гемофилии А и В используют тест генерации тромбопластина, коррекционные пробы в аутокоагулограмме: при гемофилии А нарушение свертываемости устраняется добавлением в плазме больного донорской плазмы, предварительно адсорбированной сульфатом бария (при этом удаляется фактор IX, но сохраняется фактор VIII), но не устраняется нормальной сывороткой, продолжительность хранения которой 1–2 сут (содержит фактор IX, но лишена фактора VIII); при гемофилии В коррекцию дает старая сыворотка, но не плазма. При наличии в крови больного иммунного ингибитора антигемофилического фактора («ингибиторная» форма гемофилии) коррекцию не дают ни плазма, ни старая сыворотка, мало нарастает уровень дефицитного фактора в плазме больного после в/в введения его концентрата или донорской плазмы. Титр ингибитора определяют по способности разных разведении плазмы больного нарушать свертываемость свежей нормальной донорской плазмы.
Кофакторная (компонентная) гемофилия — очень редкая форма. Тип наследования аутосомный. Низкая активность фактора VIII устраняется в тесте смешивания плазмы исследуемого с плазмой больного гемофилией А. Время кровотечения, адгезивность тромбоцитов, уровень в плазме фактора Виллебранда и его мультимерная структура не нарушены, что отличает кофакторную гемофилию от болезни Виллебранда.
Лечение. Основной метод — заместительная гемостатическая терапия криопреципитатом или концентратами фактора VIII (при гемофилии А) или фактор IX — препарат ППСБ (при гемофилии В). При отсутствии этих препаратов или неустановленной форме гемофилии — введение в/в струйно больших объемов свежей или свежезамороженной донорской плазмы, содержащей все необходимые факторы свертывания. При гемофилии А криопреципитат вводят в зависимости от тяжести геморрагии, травм или хирургического вмешательства в дозах от 10 до 30 ЕД/кг 1 раз в сутки, плазму — в дозах по 300–500 мл каждые 8 ч. При гемофилии В вводят концентраты фактора IX по 4–8 доз в сутки (под прикрытием 1500 ЕД гепарина на каждую дозу) либо донорскую плазму (до 3–4 дней хранения) по 10–20 мл/(кг • сут) ежедневно или через день. При анемизации прибегают также к трансфузиям свежей (1–2 дней хранения) одногруппной донорской крови или эритроцитной массы. Трансфузии крови и плазмы от матери больному ребенку нецелесообразны: у передатчиц гемофилии уровень антигемофильных факторов существенно снижен.
Показания к заместительной терапии: кровотечения, острые гемартрозы и гематомы, острые болевые синдромы неясного генеза (часто связаны с кровоизлияниями в органы), прикрытие хирургических вмешательств (от удаления зубов до полостных операций). Причины неудач: разведение и медленное (капельное) введение концентратов факторов или плазмы, дробное введение их малыми дозами, одновременные вливания кровезаменителей (5% раствор глюкозы, поли-глюкин, гемодез и т. д.), снижающих путем разведения концентрации антигемофильных факторов в крови больного. При «ингибиторных» формах сочетают плазмаферез (удаление антител к факторам свертывания) с введениями очень больших количеств концентратов факторов и преднизолона — до А-6 мг/(кг • сут).
Лечение гемартрозов. В остром периоде — возможно более ранняя заместительная гемостатическая терапия в течение 5–10 дней, при больших кровоизлияниях — пункция сустава с аспирацией крови и введением в его полость гидрокортизона или преднизолона (при строгом соблюдении асептики). Иммобилизация пораженной конечности на 3–4 дня, затем — ранняя лечебная физкультура под прикрытием криопреципитата; физиотерапевтическое лечение, в холодном периоде — грязелечение (в первые дни под прикрытием криопреципитата). При всех кровотечениях, кроме почечных, показан прием внутрь аминокапроновой кислоты по 4–12 г в сутки (в 6 приемов). Локальная гемостатическая терапия: аппликация на кровоточащую поверхность тромбина с гемостатической губкой и аминокапроновой кислотой. Викасол и препараты кальция неэффективны и не показаны.
Остеоартрозы, контрактуры, патологические переломы, псевдоопухоли требуют восстановительного хирургического и ортопедического лечения в специализированных отделениях. При артралгиях противопоказано назначение нестероидных противовоспалительных препаратов, резко усиливающих кровоточивость.
Профилактика
Болезнь Виллебранда — один из наиболее частых наследственных геморрагических диатезов. Аутосомно наследуемый дефицит или аномальная структура синтезируемого в эндотелии сосудов макромолекулярного компонента фактора VIII.
Патогенез. Нарушается взаимодействие стенок сосудов с тромбоцитами, вследствие чего повышается ломкость микрососудов (положительные пробы на ломкость капилляров), при большинстве форм резко возрастает время кровотечения, снижается адгезивность тромбоцитов к субэндотелию и их агглютинация под влиянием ристомицина. Одновременно в большей или меньшей степени снижается коагуляционная активность фактора VIII, что сближает болезнь Виллебранда с легкими формами гемофилии А (отсюда старое название болезни — ангиогемофилия).
Клиническая картина. У женщин с профузными меноррагиями болезнь часто протекает намного тяжелое, чем у мужчин. Тип кровоточивости в тяжелых случаях смешанный, в более легких — микроциркуляторный. При незначительной травматизации возникают геморрагии в кожу и подкожную клетчатку, носовые и маточные кровотечения, часто ошибочно расцениваемые как дисфункциональные, реже — желудочно-кишечные, внутричерепные. Гемартрозы редки и поражают лишь единичные суставы, не ведут к глубоким нарушениям функции опорно-двигательного аппарата. Наиболее мучительны изнуряющие и анемизирующие меноррагии, из-за которых иногда приходится прибегать к экстирпации матки. Во время беременности фактор Виллебранда при одних формах нормализуется и роды протекают нормально, при других — остается сниженным и роды осложняются при отсутствии адекватной терапими — опасными для жизни кровотечениями. Возможно сочетание болезни Виллебранда с различными мезенхимально-сосудистыми дисплазиями — телеангиэктазией (форма Квика), артериовенозными шунтами, пролабированием створок клапанов сердца, слабостью связочного аппарата и т.д.
Диагноз устанавливают по типичной форме пожизненной кровоточивости и выявлению в разных сочетаниях следующих признаков: положительных проб на ломкость капилляров; удлинения времени кровотечения, особенно в пробах с наложением манжеты (+ 40 мм рт. ст.) по Айви, Борхфевинку или Шитиковой, при нормальном содержании тромбоцитов в крови, нормальной их величине; снижения адгезивности тромбоцитов к стеклу и коллагену, снижения агглютинации их под влиянием ристомицина и одновременного нарушения начального этапа свертываемости крови (в аутокоагуляционном тесте, при исследовании активированного парциального тромбопластинового времени). При большинстве форм снижены активность фактора Виллебранда в плазме и (или) тромбоцитах, а также уровень связанного с ним антигена. Коагуляционная активность фактора VIII при одних формах снижена, при других — нормальна. После трансфузии свежей донорской плазмы или введений криопреципитата активность фактора VIII при болезни Виллебранда возрастает в большей степени и на более длительный срок, чем при гемофилии А. Ряд форм болезни Виллебранда связан с неправильным распределением этого факторы между плазмой и тромбоцитами (например, в тромбоцитах их мало, в плазме — много или наоборот) и нарушением его мультимерной структуры. Из-за этого разнообразия патогенетических форм каждый из перечисленных лабораторных признаков может отсутствовать, что затрудняет диагностику отдельных вариантов данного заболевания. Однако типичные формы диагностируют достаточно надежно.
Лечение. При кровотечениях и хирургических вмешательствах — введения криопреципитата и струйно-свежезамороженной плазмы. Дозы и частота их введения могут быть в 2–3 раза меньше, чем при гемофилии А. С первого и до последнего дня менструального цикла, а также при носовых и желудочно-кишечных кровотечениях назначают внутрь аминокапроновую кислоту (8–12 г/сут) либо осуществляют гормональный гемостаз
Профилактика. Избегать браков между больными (в том числе между родственниками) в связи с рождением детей с тяжелой гомозиготной формой болезни.
Дефицит фактора XI (гемофилия С) — редкое аутосомно наследуемое заболевание (чаще встречается у евреев), характеризующееся слабым нарушением внутреннего механизма начального этапа свертывания крови, отсутствием или незначительной выраженностью геморрагии.
Клиническая картина. Чаще всего болезнь протекает бессимптомно и случайно выявляется при исследовании свертывающей системы крови. Спонтанная кровоточивость отсутствует или незначительна. Травмы и операции в ряде случаев (не всегда даже у одного и того же больного) осложняются кровотечениями.
Диагностика основана на выявлении нарушения начального этапа свертывания крови (в аутокоагулограмме, АПТВ) при нормальном протромбиновом и тромбиновом времени. В коррекционных тестах нарушение исправляют добавлением как нормальной плазмы, так и нормальной сыворотки (отличие от легчайших форм гемофилии А и В).
Лечение. В большинстве случаев лечения не требуется. При операциях и родах, осложненных кровотечениями, — струйные трансфузии свежезамороженной плазмы.
Профилактика такая же, как при болезни Виллебранда.
Диспротромбии — геморрагические диатезы, обусловленные наследственным дефицитом факторов протромбинового комплекса — VII (гипопроконвертинемия), X (болезнь Стюарта-Прауэра), II (гипопротромбинемия) и
V (гипоакцелеринемия). Дефицит перечисленных факторов часто встречается как приобретенный дефект системы гемостаза, но редко (факторы VII, X, V) или крайне редко (фактор II) как наследственный дефект.
Клиническая картина. При легких формах — микроциркуляторный, при более тяжелых — смешанный тип кровоточивости. Гемартрозы редки (преимущественно при дефиците фактора VII).
Диагностика. При всех формах значительно удлинено протромбиновое время (снижен протромбиновый индекс) при нормальном тромбиновом времени. Внутренний механизм свертывания (аутокоагулограмма, активированное парциальное тромбопластиновое время) нарушен при дефиците факторов X,V и II, но остается нормальным при дефиците фактора VII. Разграничение дефицита факторов X, V и II проводят с помощью корригирующих проб, тестов со змеиными ядами, путем количественного определения каждого из факторов.
Приобретенные формы дефицита факторов протромбинового комплекса чаще всего обусловлены приемом антикоагулянтов непрямого действия (кумаринов — пелентана, синкумара и др., фенилина), К-витаминной недостаточностью при обтурационной желтухе и кишечном дисбактериозе, тяжелыми заболеваниями печени, системным амилоидозом, чрезмерной депрессией этих факторов (ниже 20% нормы) на 3–7-й день после рождения (геморрагическая болезнь новорожденных). Следует, однако, учитывать, что в указанных ситуациях кровоточивость часто возникает и вследствие одновременного развития ДВС-синдрома.
Клиническая картина. Комплексный приобретенный дефицит витамин-К — зависимых факторов первоначально проявляется петехиально-синячковой кровоточивостью (в частности, геморрагиями в местах инъекций, носовыми и десенными кровотечениями, гематурией), затем более обширными кровоподтеками и гематомами в области спины, в забрюшинном пространстве, геморрагиями в брюшину и стенку кишок, нередко имитирующими острый живот, меленой, иногда кровоизлияниями в мозг.
Лечение. При наследственном дефиците факторов яротромбинового комплекса — заместительная терапия (свежезамороженная плазма, введение препарата ППСБ в/в). При приобретенных формах — такая же терапия и введение водорастворимых препаратов витамина К (викасола) по 20–40 мг в/в повторно до купирования кровоточивости и нормализации протромбинового времени.
Дисфибриногенемии — наследственные молекулярные аномалии фибриногена, характеризующиеся либо замедлением свертывания этого белка под влиянием тромбина и тромбиноподобных ферментов, либо неправильной его полимеризацией, либо изменением чувствительности к фибринолизину (плазмину). Кровоточивость (как правило, легкая петехиально-синячковая) выявляется лишь при некоторых формах, тогда как при большинстве форм нет угрозы кровотечений или имеется наклонность к тромбозам.
Лечение в большинстве случаев не показано; при острых обстоятельствах (большие операции, множественные тромбозы) плазмаферез с заменой таким же объемом свежезамороженной или нативной донорской плазмы (по 800–1000 мл в день в течение 2–3 дней).
Геморрагические диатезы, обусловленные патологией тромбоцитов: тромбоцитопении и тромбоцитопатии.
Тромбоцитопеническая пурпура (идиопатическая, приобретенная) — сборная группа заболеваний, объединяемая по принципу единого патогенеза тромбоцитопении; укорочения жизни тромбоцитов, вызванного наличием антител к тромбоцитам или иным механизмом их лизиса. Различают аутоиммунную и гаптеновую иммунную тромбоцитопению. В свою очередь аутоиммунная тромбоцитопения может быть как идиопатической, первичной, так и вторичной. В происхождении гаптеновых (иммунных) форм тромбоцитопении ведущее значение имеют медикаменты и инфекции.
Клиническая картина. Нарушен тромбоцитарно-сосудистый гемостаз. Характерны синяки и геморрагии различной величины и формы на коже; кровотечения из носа, десен, матки, иногда из почек, желудочно-кишечного тракта. Кровотечения возникают спонтанно; появлению синяков способствуют ушибы. Спленомегапия отсутствует. Заболевание осложняется хронической железодефицитной анемией различной тяжести. Течение заболевания может быть легким, средней тяжести и тяжелым.
Диагноз тромбоцитопенической пурпуры предполагается при наличии геморрагии на коже в сочетании с носовыми и маточными кровотечениями. Лабораторная диагностика: тромбоцитопения в анализах периферической крови, удлинение времени кровотечения по Дьюку, Айви или Борхгревинку-Ваалеру, положительные пробы на ломкость капилляров, повышенное или нормальное содержание мегакариоцитов в костном мозге. Клинически диагноз аутоиммунной тромбоцитопении предполагают на основании отсутствия семейного анамнеза и других признаков наследственного дефицита тромбоцитов, а также положительного результата стероидной терапии.
Лечение. Консервативное лечение — назначение преднизолона в начальной дозе 1 мг/(кгсут). При недостаточном эффекте дозу увеличивают в 2–4 раза (на 5–7 дней). Продолжительность лечения 1–4 мес в зависимости от эффекта и его стойкости. О результатах терапии свидетельствует прекращение геморрагии в течение первых дней. Отсутствие эффекта (нормализации уровня тромбоцитов в крови через 6–8 нед лечения преднизолоном) или его кратковременность (быстрый рецидив тромбоцитопении после отмены стероидов) служит показанием к спленэктомии. Абсолютные показания к спленэктомии — тяжелый тромбоцитопенический геморрагический синдром, не поддающийся консервативной терапии, появление мелких множественных геморрагии на лице, языке, кровотечений, начинающаяся геморрагия в мозг, а также тромбоцитопения средней тяжести, но часто рецидивирующая и требующая постоянного назначения глюкокортикоидов. Терапию иммунных тромбоцитопении химиотерапевтическими препаратами — иммунодепрессантами (азатиоприн, циклофосфан, винкристин и др.) изолированно или в комплексе с преднизолоном назначают только при неэффективности стероидной терапии и спленэктомии в условиях специализированного стационара и лишь по жизненным показаниям. Гемостаз осуществляют путем тампонады (когда возможно, местного или внутривенного применения аминокапроновой кислоты, назначения адроксока, этамзилата (дицинона) и других симптоматических средств. Маточные кровотечения купируют приемом аминокапроновой кислоты (внутрь по 8–12 г в день), местранола или инфекундина.
Прогноз различен. При иммунологической редукции мегакариоцитарного ростка, а также при неэффективной спленэктомии прогноз ухудшается. Больные подлежат обязательной диспансеризации. Частоту посещений врача определяют тяжесть заболевания и программа лечения на данный момент.
Спленогенные тромбоцитопении — тромбоцитопении, обусловленные спленомегалией и гиперспленизмом.
Патогенез. Спленомегалии любого генеза могут сопровождаться повышенной секвестрацией и деструкцией тромбоцитов.
Диагноз основан на обнаружении тромбоцитопении при увеличенной селезенке и нормальном (или даже реактивно увеличенном) числе мегакариоцитов в костном мозге.
Лечение патогенетическое — спленэктомия.
Симптоматические тромбоцитопении, обусловленные нарушением, тромбоцитообразования, встречаются при неопластических, апластических и других заболеваниях костного мозга (острые и хронические лейкозы, аплазии кроветворения различного генеза, миелофиброз, остеомиелоскпероз, миелокарциноматоз, болезнь Педжета и некоторые другие заболевания костей).
Диагноз ставят при выявлении заболевания кроветворной системы с тромбоцитопенией, нарушении мегакариоцито- и тромбоцитообразования по данным морфологическою исследования костного мозга.
Лечение направлено на основное заболевание.
Тромбоцитопатии — заболевания, в основе которых лежит врожденная (чаще всего наследственная) или приобретенная качественная неполноценность тромбоцитов. При ряде Тромбоцитопатии возможна непостоянная вторичная тромбоцитопения (обычно умеренная), обусловленная укорочением продолжительности жизни дефектных тромбоцитов.
Тромбастения (болезнь Гланцманна) — наследственное заболевание, передаваемое по аутосомно-доминантному или неполному рецессивному типу, поражающее лиц обоего пола.
Патогенез. Первичный дефект коллаген- и АДФ-индуцированной агрегации тромбоцитов при сохранении реакции освобождения из тромбоцитов пластиночных компонентов: серотонина, АДФ, факторов III и IV и др. при воздействии коллагеном.
Дизагрегационные тромбоцитопатии — нарушение одной или нескольких агрегационных функций пластинок. В группу включают формы с нарушением реакции освобождения тромбоцитарных факторов и без него, а также с нарушением накопления в этих клетках АТФ, АДФ и серотонина.
Патогенез. Наследственно обусловленное или приобретенное снижение всех или отдельных адгезивноагрегационных свойств. Свойством провоцировать скрытую дисфункцию пластинок или вызывать ее обладает ряд лекарственных препаратов: ацетилсалициловая кислота, бутадион (фенилбутазон), индометацин (метиндол) и др.
Геморрагические диатезы, обусловленные патологией сосудов. Наследственная телеангиэктазия (геморрагический ангиоматоз, болезнь Ослера-Рандю) — наследственное заболевание, передаваемое по аутосомно-доминантному типу. Характеризуется истончением и недостаточным развитием на отдельных участках сосудистого русла субэндотелиального каркаса мелких сосудов, неполноценностью эндотелия.
Патогенез. В детском или юношеском возрасте образуются тонкостенные, легко кровоточащие и травмируемые малые ангиомы; в ряде случаев формируются артериовенозные шунты в легких и других органах, прочие признаки неполноценности мезенхимы — растяжимость кожи (резиновая кожа), слабость связочного аппарата (привычные вывихи, пролабирование створок клапанов сердца). Возможно сочетание, с болезнью Вилпебранда.
Клиническая картина. Преобладают рецидивирующие кровотечения из телеангиэктазий, расположенных чаще всего в носу. Реже кровоточат телеангиэктазы на кайме губ, слизистых оболочках ротовой полости, глотки, желудка. Число телеангиэктазий и кровотечений нарастает в период полового созревания и в возрасте до 20–30 лет. При наличии артериовенозных шунтов возникают одышка, цианоз, гипоксический эритроцитов; рентгенологически в легких обнаруживают единичные округлые или неправильной формы тени, ошибочно принимаемые нередко за опухоли. Возможно сочетание с пролабированием створок клапанов сердца (шумы, аритмия), гипермобильностью суставов, вывихами и другими мезенхимальными нарушениями (геморрагические мезенхимальные дисплазии по 3. С. Баркагану) и с дефицитом фактора Виллебранда (синдром Квика). Заболевание может осложниться циррозом печени.
Диагноз основан на обнаружении типичных телеангиэктазий, рецидивирующих кровотечений из них, семейного характера заболевания (возможны и спорадические случаи). Существенных нарушений системы гемостаза нет (кроме случаев сочетания с дефицитом фактора Виллебранда). При частых и обильных кровотечениях развивается постгеморрагическая анемия; при артериовенозных шунтах — эритроцитоз, повышенное содержание гемоглобина в крови.
Лечение. В периоды кровотечений используют средства местной и общей гемостатической терапии — орошения тромбином с 5% раствором аминокапроновой кислоты, тампонада носа масляными тампонами, прижигания и др.
Более эффективна криотерапия. В иных случаях приходится прибегать к хирургическому лечению (иссечение ангиом, пластика перегородки носа, перевязка артерий). Используют баротерапию, прижигания с помощью лазера. Все эти мероприятия часто дают лишь временный эффект. Введения викасола не показаны. При сопутствующем дефиците фактора Виллебранда показаны трансфузии нативной плазмы, введения криопреципитата. При анемизации — гемотрансфузии, введение препаратов железа.
Прогноз в большинстве случаев относительно благоприятный, но встречаются формы с неконтролируемыми кровотечениями.
Профилактика. Избегатьтравматизациислизистых оболочек в местах расположения ангиом, смазывание слизистой оболочки носа ланолином (с тромбином) или нейтральными маслами.
Геморрагический васкулит (анафилактоидная пурпура, иммунный микротромбоваскулит, болезнь Шенлейна-Геноха) — кровоточивость, обусловленная поражением сосудов малого калибра иммунными комплексами и компонентами системы комплемента (см. Васкулиты системные в главе «Ревматические болезни»).