Геморрагии в месте инъекции что это
Геморрагический синдром
Клиническая характеристика геморрагического синдрома
| I.Гематомный тип (нарушение внутреннего пути свертывания коагуляционного гемостаза) | II.Петехиально-пятнистый (микроциркуляторный) тип (нарушение тромбоцитаного звена гемостаза, внешнего пути свертывания коагуляционного гемостаза) | III.Смешанный (синячково-гематомный) тип (сочетанное нарушение и тромбоцитарного и коагуляционного звена гемостаза) |
(патология микрососудистого русла)
(локальная сосудистая патология)
Симптомы геморрагического синдрома
Характер и локализация кожных высыпаний при геморрагическом синдроме определяют симптоматику данной патологии.
Основной симптом – длительные кровотечения, возникающие как следствие травмы или изнуряющей физической нагрузки, сильного перенапряжения, переохлаждения или перегревания, которые могут также происходить самопроизвольно.
В каждом пятом случае патологии наблюдается сыпь различного характера, могут появляться как мелкие петехии, так и крупные гематомы некротических форм, возможно возникновение ангиэктазий.
Геморрагический синдром может стать следствием приема лекарственных препаратов, которые влияют на естественные процессы тромбоцитов и понижают свертываемость крови. Кроме того, у пациентов, страдающих болезнью Верльгофа, гемофилией и дефицитом протромбина также может наблюдаться данная патология.
Проявления геморрагического синдрома
Разновидности геморрагического синдрома
Нарушение внутреннего пути свертывания коагуляционного гемостаза (гематомный тип кровоточивости)
Врожденная и приобретенная афибриногенемия
Нарушение тромбоцитарного звена гемостаза, внешнего пути свертывания коагуляционного гемостаза (петехиально-пятнистый тип кровоточивости)
Тромбоцитопения
Тромбоцитопатия
Дефицит факторов II,V,VII,XI
Cочетанное нарушение тромбоцитарного и коагуляционного звена гемостаза (смешанный (синячково-гематомный) тип кровоточивости)
Диссеминированное внутрисосудистое свёртывание
Болезнь Виллебранда
Патология микрососудистого русла (васкулитно-пурпурный тип кровоточивости)
Кровоточивость петехиальная с эксудативно-воспалительными явлениями, очагами некроза, гематурия, артралгия, кровоточивость слизистых.
Геморрагический васкулит
Ангиоматозные кровотечения
Диагностика геморрагического синдрома
Вовремя установленный диагноз поможет специалисту назначить эффективное лечение, а вам – сделать свои сосуды здоровыми раз и навсегда. Подтвердить или опровергнуть диагноз можно, сдав ряд лабораторных анализов, направленных на получение детальной информации о состоянии крови. Также понадобится провести коагуляционные тесты, во время спорных ситуаций врач-диагност может взять стернальную пункцию для углубленной диагностики.
После получения полной картины заболевания, определения ее стадии, причин и степени тяжести геморрагического синдрома, будет назначено лечение.
Лечение геморрагического синдрома
Основой выбора метода лечения геморрагического синдрома является определение причины заболевания, однако существуют следующие ключевые принципы:
Профилактика геморрагического синдрома
Важнейшей и основополагающей частью предупреждения геморрагического синдрома является полное медицинское обследование для своевременного установления и устранения его возможных причин.
Новорожденным недоношенным детям необходимо введение подкожно витамина К и прикладывание ребенка к груди как можно скорее после рождения.
Диетическое питание пациентов, склонных в данной патологии, должно быть основано на усиленном потреблении витамина К, а также белков, овощей и фруктов. Кроме того, таким людям необходимо избегать физической активности, приводящей к возникновению травм и ранений.
Геморрагия
Содержание
Иными словами, это не что иное, как повышенная склонность организма к кровоточивости. Геморрагия бывает наследственного и приобретённого характера. Существует множество разновидностей этой аномалии в зависимости от того, на каком участке тела она проявляется.
Рассмотрим самые распространённые из них.
Геморрагии в месте инъекции
Это локальные кровотечения, которые происходят при внутримышечных и подкожных инъекциях. При внутривенных инъекциях они могут возникать в случае, если произошло сквозное прокалывание вены. Степень выраженности локальной геморрагии зависит от многих факторов: влияет вводимый препарат, ширина иглы, мастерство медика, проводящего процедуру.
Также оказывает влияние индивидуальное состояние организма и склонность тканей к регенерации. Внутримышечные инъекции дают более сильно выраженные геморрагии, чем подкожные, по причине большей васкуляризации мышечной ткани. Как правило, через некоторое время, образовавшееся кровяное пятно исчезает само, но в некоторых отдельных случаях может быть назначена заместительная терапия или же приём водорастворимых препаратов.
Геморрагии желудка
Геморрагии глаза
Гемморагиии подногтевые и кожные
Геморрагии на коже получаются при кровоизлияниях под кожу либо при проникновении эритроцитов через сосудистые стенки в кожные ткани. Имеют вид пятен на коже или точечных геморрагий в виде россыпей. Могут менять цвет, сливаться друг с другом. Поначалу, как правило, они ярко-красного цвета, затем изменяют цвет на багровый, синий, зеленоватый, потом становятся буро-жёлтым. Изменения цвета определяются изменением гемоглобина. По сути, это гематома. Лечение обычно не требуется, пятна через некоторое время исчезают самостоятельно.
Экспульсивная геморрагия
Довольно редкое и тяжёлое осложнение, возникающее после операций на глазном яблоке при катаракте и других заболеваниях. Может начаться уже в момент операции, но обычно развивается на ранних стадиях послеоперационного периода. При этом виде геморрагии происходит повреждение задних цилиарных артерий. Считается, что гипертония, атеросклероз, глазная гипертензия являются предрасполагающими факторами к этому виду кровоизлияний. Поэтому во время подготовки больного к операции подобные данные должны учитываться. Сопровождается тошнотой, рвотой, сильной болью в глазу и голове. В особо тяжёлых случаях возможно выталкивание содержимого глаза кровяным напором из раны. В качестве противодействующих методов применяют эвакуацию крови через разрез склеры. Также необходимо как можно быстрее и плотнее зашить рану после операции.
Субарахноидальная геморрагия
Различные виды геморрагии на фото выглядят весьма устрашающе, в чём можно убедиться, просмотрев их в интернете. Не стоит думать, что это просто синяк, который сам пройдёт. Хотя некоторые виды геморрагий не требуют лечения, тем не менее, существуют и довольно опасные разновидности, которые, если их не лечить, могут привести к самым разнообразным проблемам со здоровьем в будущем.
Невылеченные геморрагии могут стать причиной разных внутренних воспалительных процессов, поспособствовать развитию очагов инфекций в организме и привести к самым непредсказуемым и тяжёлым последствиям. В числе всех прочих осложнений может также быть и бесплодие – один из самых печальных диагнозов для человека. Поэтому при геморрагиях лучше всего не пускать дело на самотёк, а обратиться к врачу за помощью.
Автор: Мария Зотова, редактор портала «Пробирка»
Геморрагии в месте инъекции что это
Поэтому на сегодняшний день отсутствуют и стандарт лечения кровоподтеков и специальные лекарственные средства, предназначенные для лечения кожи и других мягких тканей в области кровоподтеков [4, 5].
В то же время, в судебной медицине кровоподтеки традиционно рассматриваются как бесспорные следы травм и повреждений мягких тканей [1,8].
Цель исследования – исследовать взаимосвязь между кровоподтеком и локальным воспалением кожи при механических повреждениях.
Материалы и методы исследования
В клинических условиях проведено исследование динамики цвета и локальной температуры кожи после внутрикожных, подкожных и внутривенных инъекций растворов лекарственных средств у взрослых пациентов и искусственных кровоизлияний и кровоподтеках у 2-х здоровых добровольцев. С помощью фото и видеосъемки в видимом и в инфракрасном спектрах излучения тканей проведено исследование динамики цвета и локальной температуры кожи в местах кровоизлияний, кровоподтеков и закрытых повреждений мягких тканей. Температура регистрировалась с помощью тепловизора марки Thermo Tracer TH9100XX (NEC, USA) в диапазоне температур +25 – +36°C по общепринятой методике [9,10]. Мониторинг цвета и температуры кожи проводился у них в области оголенного предплечья, бедра и спины. Все исследования на живых людях были проведены внутри помещений при рассеянном искусственном освещении и температуре воздуха +25°С.
Проведено 3 серии наблюдений. Первая серия наблюдений включала 60 пациентов (40 мужчин и 20 женщин терапевтического отделения и 20 родильниц родильного дома), у которых кровоподтеки возникали случайно после выполнения плановых внутривенных, подкожных и внутрикожных инъекций в области предплечий. Вторая серия наблюдений включала двух взрослых здоровых добровольцев в возрасте 21 и 24 лет и одного взрослого пациента в возрасте 52 лет, находящегося 2 часа в состоянии комы вследствие повреждений внутренних органов, несовместимых с жизнью. Кровоподтеки в этой серии вызывались путем внутрикожных инъекций по 0,1 мл их собственной венозной крови. Третья серия наблюдений включала двух добровольцев, которым в коже предплечий производились щипки кожи пальцами рук. При этом кожа прищипывалась пальцами рук в 4-х местах на расстоянии около 8 см друг от друга вплоть до кровоизлияния и появления яркого красного цвета из-за пропитывания кожи добровольцев кровью.
Статистическая обработка результатов была проведена с помощью программы BIOSTAT по общепринятой методике.
Результаты исследования и их обсуждение
Полученные результаты выявили наличие существенной разницы в динамике цвета и температуры кожи при кровоподтеках, вызванных пропитыванием кожи кровью до и после значительного повреждения мягких тканей. Показано, что при госпитальном лечении пациентов терапевтических отделений и родильных домов в городе Ижевске врачи ежедневно назначают пациентам в виде инъекций до 30 растворов лекарственных средств, многие из которых вводятся 3 раза в день. Подсчитано, что из всех лекарств, назначаемых врачами, 79 % лекарств вводится путем внутривенных инъекций и около 19 % – путем внутримышечных инъекций. Установлено, что в первый день госпитального лечения кожа пациентов в традиционных местах инъекций выглядит здоровой до первой инъекции у 97 % пациентов, а к концу госпитального лечения выглядит поврежденной у 100 % пациентов. При этом в местах инъекций на коже появляются участки воспалений и кровоподтеков различной величины и количества, вызванные проколами инъекционными иглами и различными колото-инфильтративными повреждениями кожи и подкожно-жировой клетчатки. Причем в день выписки пациентов из лечебных учреждений после госпитального лечения кровоподтеки в местах инъекций встречаются практически у каждого второго пациента.
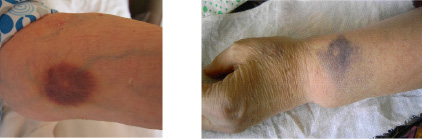
Установлено, что кровоподтеки у пациентов возникают чаще всего из-за проколов кровеносных сосудов, возникающих при введении в них инъекционных игл и внутрисосудистых катетеров. При этом выявленные нами постинъекционные кровоподтеки являлись по сути дела синяками в 2/3 случаев, поскольку кожа в их области имела синий или темно-вишневый цвет (рис. 1).
Рис. 1. Цвет кожи в предплечьях пациенток через 5 часов (1) и 5 дней (2) после внутривенных инъекций лекарственных средств
При исследовании динамики цвета и температуры кожи в области кровоподтеков у добровольцев и у одного пациента, находящегося в коме, удалось установить следующее. Оказалось, что в области кровоподтеков, вызванных инъекционным введением в кожу или под кожу венозной крови или кровоизлиянием из подкожной вены при прокалывании ее инъекционной иглой, кожа приобретает синий цвет, но ее температура остается нормальной.
С другой стороны, при исследовании у добровольцев динамики цвета и температуры кожи в области кровоподтеков, вызванных значительным повреждением мягких тканей, удалось установить, что кожа приобретает ярко красный цвет и нагревается.
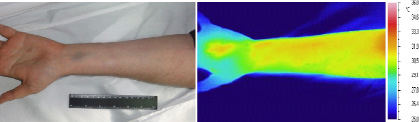
В частности, в результате исследования динамики цвета и температуры кожи у добровольцев установлено, что на месте кровоизлияний, вызванных проколами подкожных вен и внутрикожными инъекциями собственной венозной крови, кожа тут же приобретает синий цвет. Однако температура кожи в области кровоподтека остается нормальной и достоверно не отличается от температуры соседних участков, в которых кожа сохраняет естественный нормальный цвет (рис. 2).
Рис. 2. Предплечье добровольца через 10 минут после внутрикожной инъекции 0,5 мл его венозной крови в видимом (1) и в инфракрасном (2) диапазоне спектра излучения тканей
Иными словами, пропитывание кожи венозной кровью ведет к формированию «холодный» кровоподтек синего цвета. Кожа в области такого синяка с первых минут имеет синий цвет и сохраняет обычную температуру.
Аналогичные данные получены нами у добровольцев и у одного пациента после внутрикожных и подкожных инъекций их собственной венозной крови. Указанные исследования были проведены у добровольцев в области предплечий, а у пациента – в области бедра. Полученные нами данные показали, что синяки обычно имеют округлую форму и быстро увеличиваются в своих размерах. В частности, через 10 минут после инъекционного прокола вены в области предплечья синяки представляли собой пятна в форме эллипсов, расположенных своими длинными осями параллельно оси предплечья. При этом пятна синяков имели максимальную длину 9,2 ± 0,4 см и ширину 8,3 ± 0,2 см (Р ≤ 0,05, n = 5). Через 10 минут после внутрикожных инъекций 0,5 мл крови в области предплечья участки кожи синего цвета также имели форму эллипсов, расположенных параллельно оси предплечья, с максимальным значением длины 10,7 ± 0,5 см и ширины 9,7 ± 0,4 см (Р ≤ 0,05, n = 5).
Через 10 минут после 4-х внутрикожных инъекций по 0,1 мл венозной крови в бедро у пациента, находящегося в коме, кровоподтеки также имели синий цвет. Однако синяки имели форму кругов с величиной диаметра 0,9 ± 0,01 см (Р ≤ 0,05, n = 4). Причем, кожа в области всех этих кровоподтеков сохраняла обычную температуру с первой минуты и вплоть до полного исчезновения синяков.
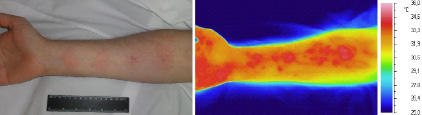
Совершенно иная динамика температуры оказалась при кровоподтеках, вызванных существенным механическим повреждением кожи и подкожно-жировой клетчатки. Кожа в области кровоподтеков, образованных щипками, теряла естественную окраску и приобретала ярко красный цвет. Кроме этого, температура кожи в области кровоподтека повышалась. В частности, через 2 и 5 минут после прищипывания кожи пальцами рук температура кожи в центре кровоподтеков превышала температуру кожи в здоровых участков на 1,23 ± 0,07°С и 3,65 ± 0,10°С (Р ≤ 005, n = 8) соответственно. Затем температура в зонах локальной гипертермии оставалась на этом уровне без существенных изменений в течение 30–60 минут (рис. 3).
Однако выраженная локальная гипертермия сохранялась в области закрытых повреждений мягких тканей недолго. Через 60 минут температура в области кровоподтеков, вызванных щипками кожи начинала медленно уменьшаться, приближаясь к нормальным значениям через 2 часа.
Другими словами, после внутрикожных инъекций или излияний в кожу венозной крови из проколотых вен появлялись синяки, поэтому казалось, что в области предплечья имеются ушибы мягких тканей. на глаз были четко видны кровоподтеки синего или темно-вишневого цвета и казалось, что они являются следствием повреждений кожи, подкожно-жировой клетчатки и других мягких тканей, поскольку кровоподтеки традиционно считаются в народе доказательством травм. Однако изображение этих участков на экране тепловизора показывало обратное, а именно – отсутствие участков локальной гипертермии
Рис. 3. Вид предплечья добровольца через 45 минут после прищипывания кожи пальцами рук в 4-х местах в видимом (1) и инфракрасном диапазонах спектра излучения тканей (2)
Парадоксально, но – факт. Наши результаты доказывают, что наличие кровоподтека не является однозначным диагностическим симптомом повреждения мягких тканей и критерием размера, выраженности и даже наличия их «ушиба твердым тупым предметом». Более того, кровоподтек (как и кровоизлияние) не относится к симптомам локального воспаления. Иными словами, кровоподтек и локальное воспаление – это два совершенно самостоятельных и независящих друг от друга процесса. Симптомами воспаления являются локальная гиперемия, гипертермия, припухлость, болезненность и нарушение функции воспаленного участка ткани. Поэтому отсутствие локальной гипертермии в области кровоподтека, вызванного инъекцией венозной крови, доказывает отсутствие симптомов раздражения, локального воспаления и, следовательно, отсутствие повреждения мягких тканей.
Следовательно, собственная венозная кровь является безопасным средством для внутрикожных инъекций. Инъекции собственной венозной крови внутрь кожи и под кожу не оказывают местное раздражающее действие.
Выражаю благодарность профессору РАЕ Касаткину Антону Александровичу и студентам Ижевской государственной медицинской академии Черновой Лейсан Вячеславовне, Фишеру Евгению Леонидовичу и Насырову Марату Ринатовичу за помощь в проведении научных исследований.
Причины геморрагических осложнений у пациентов стационара, получающих лечебные дозы антикоагулянтов
Широкое применение антикоагулянтов (АК) нередко сопровождается нежелательными явлениями, среди которых чаще всего встречаются геморрагические осложнения.
Оценить частоту и структуру кровотечений, связанных с использованием АК в многопрофильном стационаре, и разработать план мероприятий, направленных на снижение риска развития данных осложнений.
Материалы и методы
Ретроспективно проанализированы электронные истории болезни пациентов, госпитализированных в многопрофильный стационар с 01.01.2015 по 15.03.2018 и перенесших геморрагические осложнения (в том числе при поступлении в стационар) на фоне приема «лечебных»» доз АК, назначенных по следующим показаниям: фибрилляция предсердий, тромбоз глубоких вен, тромбоэмболия легочной артерии, механический протез сердечного клапана. Оценивали частоту, локализацию, тяжесть и предотвратимость кровотечений, а также их основные и дополнительные причины по методу Root Cause Analysis (RCA, анализ основных причин).
На протяжении 38 месяцев АК в «лечебных» дозах получали 2093 пациента. У 43 (2,1%) из них были зарегистрированы геморрагические осложнения. Частота назначения варфарина, низкомолекулярных гепаринов (НМГ) и прямых оральных антикоагулянтов (ПОАК) составила 28%, 32% и 46%, соответственно. Частота кровотечений при лечении разными АК достоверно не различалась и составила 2,8% при приеме варфарина, 1,6% – ПОАК и 2,2% – НМГ. Чаще всего встречались желудочно-кишечные кровотечения (33%) и гематурия (21%). Факторы пациента признаны основной причиной кровотечений в 83,7% случаев, факторы персонала – в 14,0%, организационные факторы – в 2,3%. С ошибками использования ЛС были связаны 16% кровотечений. Сопутствующие заболевания пациента были самой частой причиной кровотечений (63%). Потенциально предотвратимыми были 35% кровотечений.
По итогам RCA был составлен план устранения потенциально предотвратимых факторов кровотечений, связанных с пациентом, персоналом и организацией лечебно-диагностического процесса.
Широкое применение антикоагулянтов (АК) нередко приводит к нежелательным явлениям (НЯ), требующим обращения за медицинской помощью. Общее число обращений по поводу НЯ, развивающихся на фоне приема антикоагулянтных препаратов, в 2,4 раза превышает таковое при применении опиоидов [1]. По данным Института безопасной лекарственной практики (Institute for Safe Medication Practice), в 2016 году в США зарегистрировано 22 тыс сообщений о развитии НЯ при приеме АК, что составило примерно 10% от всех обращений за медицинской помощью пациентов, принимающих АК [2]. В США в 2013-2014 гг. антикоагулянты были самой частой причиной обращения за неотложной помощью по поводу НЯ; примерно в половине случаев (48,8%) пациенты нуждались в госпитализации [1]. Доля лекарственных нежелательных реакций среди всех осложнений, связанных с оказанием медицинской помощи в стационаре, составляет 39,6% [3]. Число НЯ в стационаре на 1000 выписанных пациентов, получавших нефракционированный гепарин (НФГ), составило 6,0, низкомолекулярные гепарины (НМГ) или прямые оральные АК (ПОАК) – 7,6, варфарин – 3,7 [3].
Основную долю НЯ, связанных с АК, составляют кровотечения (около 80%) различной локализации [1], которые возникают у 8-19% пациентов, длительно получающих препараты этой группы 6. У пациентов, принимавших АК для профилактики тромбоэмболических осложнений при фибрилляции предсердий, чаще развивались желудочно-кишечные кровотечения (8495 из 17218 случаев), а также внутримозговые кровоизлияния (1809 из 17218 случаев) [7].
Профилактика НЯ, связанных с приемом АК, в том числе кровотечений, способствует снижению расходов на медицинскую помощь. Например, внедрение программы «Saving Lives and Saving Money: Hospital-Acquired Conditions», разработанной Agency for Healthcare Research and Quality, привело к снижению частоты НЯ в стационарах США в 2010-2014 гг. и позволило съэкономить более 1 млрд долларов [3]. Затраты на лечение последствий НЯ, связанных с приемом АК, в США оцениваются в 40 640$ в расчете на одно событие (учитывая стоимость медикаментов и трудозатрат медперсонала) [8].
Эффективным инструментом анализа и управления риском возникновения НЯ является анализ основных причин (root cause analysis – RCA) [9]. Объединенная комиссия по аккредитации медицинских учреждений США (Joint Commission AHO) в 1997 году впервые использовала метод RCA для анализа ошибок локализации операционного поля (неверная сторона операции). Однако ряд исследователей указывают на низкую эффективность RCA при отсутствии активных действий по устранению выявленных причин события [10]. В настоящее время комплекс «анализ + действие» (RCA2) предполагает не только выявление причин НЯ, но и составление и реализацию плана мероприятий по их устранению [11].
Целью исследования была оценка частоты и структуры кровотечений, связанных с использованием АК в многопрофильном стационаре, с последующей разработкой плана мероприятий, направленных на снижение риска развития данных осложнений.
Материал и методы
В ретроспективное исследование включали пациентов, госпитализированных в Многопрофильный медицинский центр Банка России (Москва) с 01.01.2015 по 15.03.2018 и перенесших геморрагические осложнения на фоне применения «лечебных» доз АК, в том числе, при поступлении в стационар. Показания к применению АК в «лечебных» дозах включают в себя следующие: профилактика тромбоэмболий у пациентов с ФП и механическим клапаном сердца, лечение тромбоза глубоких вен, сопровождающегося или не сопровождающегося тромбоэмболией легочной артерии, лечение нестабильной стенокардии и инфаркта миокарда без зубца Q, лечение острого инфаркта миокарда с подъемом сегмента ST, профилактика тромбообразования в системе экстракорпорального кровообращения во время гемодиализа.
Критерии включения в исследование: развитие кровотечения на фоне применения «лечебных» доз АК; наличие в клиническом диагнозе заболевания (МКБ-10) следующих состояний: фибрилляция и трепетание предсердий (I48), протез сердечного клапана (Z95.2), флебит и тромбофлебит бедренной вены (I80.1), флебит и тромбофлебит других глубоких сосудов нижних конечностей (I80.2), флебит и тромбофлебит бедренной вены, других сосудов нижних конечностей в сочетании с легочной эмболией (I26).
Критерии невключения в исследование: анемия без документального подтверждения состоявшегося кровотечения; возникновение кровотечения на фоне применения «профилактических» доз АК; наличие в клиническом диагнозе заболевания (МКБ-10) следующих состояний: постфлебитический синдром (I87.0) (без указания даты тромбоза), флебит и тромбофлебит поверхностных сосудов нижних конечностей (I80.0), венозные тромбозы (I81-I82), легочная эмболия (I26) при отсутствии флебита и тромбофлебита бедренной вены, других сосудов нижних конечностей.
Тяжесть кровотечения оценивалась по классификациям GUSTO и TIMI [12].
Геморрагические осложнения были проанализированы с помощью методологии RCA по аналогии с формой выявления основной причины возникновения кровотечения при применении варфарина (Michigan Anticoagulation Quality Improvement Initiative) [13]. Итогом анализа RCA стало выявление основных причин возникновения кровотечений при применении «лечебных» доз АК (одна причина у каждого пациента). Основной причиной кровотечения эксперт называл фактор, который, предположительно, играл ключевую роль в развитии события (не зависит от прочих факторов, является «корневым» фактором при ответе на вопрос «почему возникло кровотечение?»). В описание результатов не вошли группы причин, не выявленных при анализе. Изза большого количества возможных факторов развития кровотечений определяли также дополнительные причины (несколько у одного пациента). У разных пациентов одни и те же причины развития кровотечений могли быть как основными, так и дополнительными. Такие группы причин, как «протоколы/процедуры организации», «управление информацией», «тех. и мат. обеспечение», относились к факторам организации, группа причин «коммуникация» не рассматривалась из-за ретроспективного анализа.
Среди основных/дополнительных причин развития кровотечений выявляли ошибки использования лекарственных средств (ЛС), для анализа которых использовали «Класси фи кацию ошибок, связанных с ЛС», разработанную Фон дом фармацевтической помощи Европы (Pharmaceutical Care Network Europe Foundation) [14].
Группы причин, в отношении которых можно применить профилактические меры, считались «потенциально предотвратимыми», остальные причины по умолчанию являлись «непредотвратимыми».
Статистическая обработка данных проведена непараметрическими методами с помощью прикладной программы «IBM SPSS Statistics v22». Для сравнения количественных показателей использовали U-тест Манна-Уитни, качественных – критерий X 2 Фишера. При ненормальном распределении применяли непараметрические методы описательной̆ статистики: медиана, интерквартильный размах (interquartile range – IQR). Различия считали достоверными при p
Результаты
Эпидемиология назначения «лечебных» доз АК. Из медицинской информационной системы ИНТЕРИН ретроспективно были отобраны случаи назначения пациентам «лечебных» доз» АК – 2093 (9%) из 23046 пациентов за 38,5 месяцев. Из 2093 электронных историй болезни с помощью поиска по ключевым словам «кровотечение», «-рагия», «геморраг-«, «гемма-» (в графе «клинический диагноз») были отобраны 64 случая кровотечений на фоне приема «лечебных» доз АК, из которых 43 соответствовали критериям включения и невключения в исследование. Показаниями к назначению АК в «лечебных» дозах (n=2093) были фибрилляция предсердий (71%), венозные тромбоэмболические осложнения (18%), острый коронарный синдром (8%), прочие тромбозы (2%) и механический протез клапана (1%).
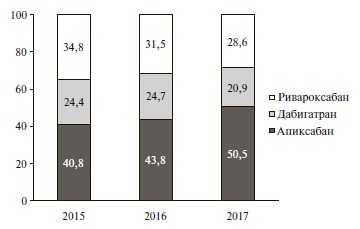
Структура назначений различных АК в 2015-2017 гг. представлена в табл. 1. Чаще всего назначали ПОАК, причем частота их назначения постепенно увеличи валась со временем (примерно на 9% в 2017 г. по сравнению с 2015 г.). Среди ПОАК наиболее распространенным препаратом был апиксабан (рис. 1).
| 2015 | 2016 | 2017 | Всего за 38 мес | |
|---|---|---|---|---|
| Примечание: разница между 2015 и 2016 гг. и между 2016 и 2017 гг. недостоверна | ||||
| Все АК, n (% от пролеченных за год) | 634 (8,8) | 629 (9,0) | 684 (9,3) | 2093(100) |
| АК, n (% от АК за год) | ||||
| Варфарин, | 153 (24,1) | 142 (22,6) | 137 (20,0) | 460 (21,9) |
| НМГ | 202 (31,9) | 195 (31,0) | 218 (31,9) | 670 (32,0) |
| ПОАК | 279 (44,0) | 292 (46,4) | 329 (48,1) | 963 (46,0) |
Характеристика пациентов и антикоагулянтной терапии. Общая характеристика включенных в исследование пациентов представлена в табл. 2. Самыми частыми сопутствующими заболеваниями были артериальная гипертония (95,0%) и сахарный диабет (39,5%). У 30 (90,5%) пациентов терапию АК назначали на неопределенно длительный срок. Девять (21,0%) пациентов ранее получали нестероидные противовоспалительные препараты регулярно в течение месяца и более, 10 (23,0%) – антиагреганты. Двадцать (46,5%) из 43 случаев кровотечений были выявлены при поступлении в стационар (в 19 случаях они послужили причиной госпитализации). У 30 пациентов текущая госпитализация была повторной: 17 (56,7%) из них госпитализировались в течение последних 6 месяцев, 8 (26,7%) – 6-12 месяцев назад и 5 (15,6%) – 1-5 лет назад. Хирур ги ческое вмешательство в течение последнего месяца было выполнено 23 (53,5%) пациентам; у 17 (74%) из них источник кровотечения находился в области послеоперационной раны.
| Показатели | Значения |
|---|---|
| Примечание: *метастазы, текущая химио- или лучевая терапия, отсутствие ремиссии в последние 6 мес | |
| Всего пациентов | 43 |
| Женщины, n (%) | 15 (35,0) |
| Возраст, медиана (IQR) | 73 (11,0) |
| Механический протез клапана, n (%) | 2 (4,5) |
| Фибрилляция предсердий, n (%) | 30 (70,0) |
| Тромбоз глубоких вен, n (%) | 11 (25,5) |
| Кровотечение в анамнезе, n (%) | 14 (32,5) |
| Индекс коморбидности Charlson, медиана (IQR) | 11,5 (6,0) |
| Сахарный диабет, n (%) | 17 (39,5) |
| Инсульт в анамнезе, n (%) | 10 (23,0) |
| Артериальная гипертония, n (%) | 41 (95,0) |
| Активная опухоль,* n (%) | 9 (21,0) |
Все пациенты на момент развития кровотечения получали АК в «лечебных» дозах: НМГ – 15 (34,9%), варфарин – 13 (30,2%) и ПОАК – 15 (34,9%), в том числе ривароксабан – 7, апиксабан – 5 и дабигатран – 3. Стандартные дозы АК принимали 18 (42,8%) пациентов, сниженные – 15 (34,9%) и повышенные – 10 (23,3%).
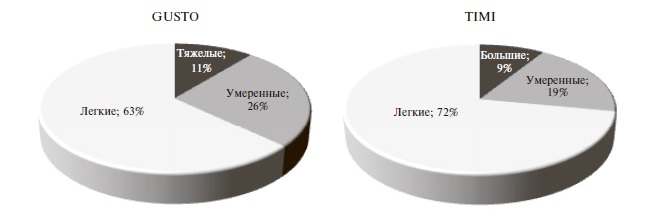
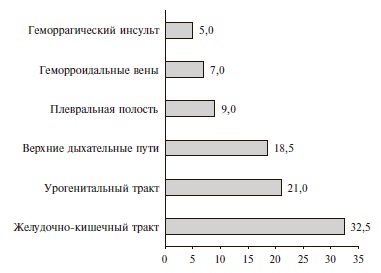
Частота и характеристика кровотечений. В целом частота кровотечений при применении «лечебных» доз АК составила 2,1%, или 18,5 случаев на 10 000 выписанных пациентов. Частота кровотечений на фоне приема варфарина, НМГ и ПОАК достоверно не отличалась: 2,8%, 2,2% и 1,6%, соответственно. Большинство кровотечений были легкими (63% – по классификации GUSTO и 72% – по классификации TIMI) (рис. 2). В 35 (81,5%) случаях после кровотечения терапия АК была приостановлена, а 14 (32,5%) пациентам потребовалось переливание крови. Структура кровотечений по локализации представлена на рис. 3.
Анализ основных и дополнительных причин развития кровотечений. Основные и дополнительные причины развития кровотечений распределяли на 3 категории – факторы пациента, персонала и факторы организации (системные факторы, связанные с организацией клинических процессов). Всего было выделено 169 причин, включая 43 основных и 126 дополнительных (рис. 4).
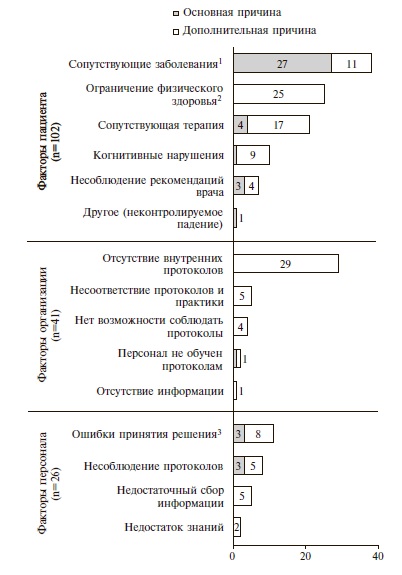
Факторы, связанные с пациентом, были признаны основной причиной кровотечений в 83,7% случаев (36 событий), факторы персонала – в 14,0% (6 событий) и факторы организации – в 2,3% (1 событие). Доля «потенциально предотвратимых» основных причин составила 35,0% (15 событий): факторы, связанные с пациентом, – 7, факторы персонала – 6, факторы организации – 1.
Среди дополнительных причин кровотечений при использовании «лечебных» доз АК факторы, связанные с пациентом, имелись в 52,5% случаев (66 событий), факторы организации – в 31,5% (40 событий), факторы персонала – в 16,0% (20 событий). Доля «потенциально предотвратимых» дополнительных причин составила 71,4% (90 событий): факторы, связанные с пациентом, – 30, факторы персонала – 20, факторы организации – 40. Среднее количество дополнительных причин возникновения кровотечений на одного пациента – 2,9.
Ошибки, связанные с использованием ЛС. Основной причиной 7 (16,3%) из 43 кровотечений были ошибки использования ЛС: отсутствие систематического пересмотра антикоагулянтной терапии при лабильном уровне МНО во время приема варфарина (2 случая), некорректный режим дозирования ривароксабана (повышение дозы) у пациентов с тромбозом глубоких вен (1), отсутствие коррекции дозы НМГ по массе тела пациента (1), превышение длительности лечения АК у пациента со спровоцированным тромбозом дистальных глубоких вен (1), неоправданное назначение антиагреганта на фоне терапии АК (1), неверная периоперационная тактика ведения пациента, принимающего варфарин (1).
Ошибки использования ЛС составили 20,6% от дополнительных причин, относящихся к факторам персонала и пациента (26 из 126): систематическое отсутствие пересмотра антикоагулянтной терапии при лабильном уровне МНО во время приема варфарина (4 случая), повышение/снижение дозы АК из-за отсутствия периодического пересмотра риска кровотечения пациента (7), несоблюдение пациентом рекомендаций врача (4), неоправданное назначение антиагрегантов при лечении АК (3), отсутствие пересмотра длительности терапии у пациентов с тромбозом глубоких вен в анамнезе, с существующим постфлебитическим синдромом (3), отсутствие расчета дозы НМГ в зависимости от массы тела пациента (3).
Профилактика кровотечений при лечении АК. По итогам анализа составлен план мероприятий по устранению потенциально предотвратимых причин кровотечений у пациентов, получающих «лечебные дозы» АК.
Обсуждение
Частота кровотечений у пациентов, принимающих «лечебные» дозы АК, в настоящем исследовании составила 18,5 на 10 000 выписанных пациентов. По данным Американского агентства по качеству и исследованиям в здравоохранении, частота кровотечений при приеме АК у пациентов в возрасте старше 65 лет в стационарах США в 2011 г. равнялась 16,4 на 10 000 выписанных пациентов [15]. Разница в частоте кровотечений может быть обусловлена высоким средним возрастом пациентов в нашем исследовании (73±11 лет), а также увеличением частоты назначения АК по сравнению с таковой в 2011 г. Таким образом, геморрагические осложнения были отмечены у 2% пациентов, которые в стационаре получали «лечебные» дозы АК. Для сравнения, кровотечения развиваются у 8-19% пациентов, длительно получающих терапию АК, в том числе амбулаторно [46]. Можно предполагать, что большая часть кровотечений при приеме АК возникает на амбулаторном этапе.
В нашем исследовании кровотечения развивались у пожилых пациентов с сопутствующими заболеваниями, которым АК назначали на неопределенно длительный срок (90,5%), преимущественно по поводу ФП (70%). Чаще всего у пациентов с ФП возникали желудочнокишечные кровотечения – в 37% случаев. В исследовании R. Hart и соавт. частота кровотечений этой локализации у пациентов с ФП составила 49% [7]. Высокая частота повторных госпитализаций (70%), кровотечений в анамнезе (32,5%), активных онкологических заболеваний (21%) свидетельствует о тяжести состояния пациентов, явившейся самой частой основной причиной возникновения кровотечений при приеме «лечебных доз» АК (63% всех основных причин). Факторы пациента были основной причиной 83,7%
кровотечений. Сходные данные приводят C. Graves и соавт. [16]. Доля тяжелых кровотечений составила 11,5% по классификации GUSTO и 9,5% по классификации TIMI. В аналогичном исследовании Gregory и соавт. доля тяжелых кровотечений по критериям GUSTO достигла 32% [8].
В нашем исследовании кровотечения развивались у 2,8% пациентов, получавших варфарин. В работе Daniels и соавт. частота кровотечений на фоне приема варфарина у пациентов терапевтического и хирургического профиля составила 1,5% и 13,5%, соответственно [17]. При лечении ПОАК мы зарегистрировали кровотечения у 1,6% пациентов. В Германии (German Claims Database) частота кровотечений у амбулаторных и стационарных пациентов с ФП, принимающих ПОАК, была выше (8%), что может свидетельствовать о более высоком риске кровотечений на амбулаторном этапе лечения [18]. Частота кровотечений у пациентов, которым назначали «лечебные» дозы НМГ, составила 2,2%. Следует отметить, что препараты этой группы получали около двух третей пациентов с внутрибольничными геморрагическими осложнениями (не при поступлении). Это может быть связано с назначением НМГ пациентам с высоким риском кровотечения или их применением в периоперационном периоде (около половины пациентов перенесли оперативное вмешательства в течение месяца до развития кровотечения). В 74% (17 из 23 пациентов) случаев источник кровотечения находился в области послеоперационной раны, что могло быть связано с несовершенством «хирургического» гемостаза (помимо высокого риска кровотечения пациента).
Низкая приверженность (несоблюдение рекомендаций врача, когнитивные нарушения) пациентов ассоциировалась с сокращением времени нахождения МНО в терапевтическом диапазоне при приеме варфарина. Тяжесть состояния пациентов в 27 случаях (63%) была ключевым фактором развития кровотечений, при этом 23 из 27 пациентов находились в периоперационном периоде.
У каждого пятого пациента среди основных и дополнительных причин кровотечений при применении «лечебных» доз АК были отмечены ошибки использования ЛС, в том числе связанные с выбором препарата (например, продолжение приема антагониста витамина К у пациентов, у которых МНО систематически находилось за пределами целевого диапазона), режима дозирования или длительности лечения АК, необоснованным назначением антиагрегантов на фоне приема АК. Отсутствие собственных внутренних протоколов терапии АК в ММЦ до конца 2017 г. могло быть причиной высокой частоты «факторов организации» (29%) среди дополнительных причин возникновения кровотечений.
Ограничения работы
Данное исследование проводилось ретроспективно путем анализа электронных историй болезни, поэтомуинформация о ряде факторов, способствующих возникновению кровотечений (например, ограничение передачи информации), отсутствовала. Ограничение выборки, в частности исключение из анализа «профилактических» доз» АК, могло повлиять на итоговую структуру результатов. Основные и дополнительные причины возникновения кровотечений определялись ретроспективно и носят вероятностный характер.
Заключение
Геморрагические осложнения развивались примерно у 2% стационарных пациентов, получавших «лечебные» дозы АК. Частота кровотечений была ниже всего при лечении ПОАК, хотя риск их развития достоверно не отличался при применении различных АК, в том числе НМГ и варфарина. Самыми частыми основными причинами развития кровотечений на фоне «лечебных доз» АК были факторы пациента (83,8%). Высокая доля «потенциально предотвратимых» событий (35,0%), а также большое количество «потенциально предотвратимых» дополнительных причин кровотечений (71,4%) у пациентов, получающих «лечебные» дозы АК, свидетельствует о необходимости разработки профилактических мер. Анализ структуры назначений АК и причин развития кровотечений по методу RCA позволяет составить целенаправленный план устранения «потенциально предотвратимых» нежелательных лекарственных реакций.