Генитофеморальный болевой синдром что это
Синдром хронической тазовой боли
Что такое?
Синдром хронической тазовой боли – это комплекс признаков, сигнализирующих о развитии заболеваний органов малого таза. Основным симптомом выступает боль ниже пупка, в надлобковой и подвздошной области, крестце и промежности. Синдром может возникать у женщин и мужчин. О женском СХТБ говорят, если дискомфортные ощущения в тазу сохраняются на протяжении полугода. У мужчин состояние диагностируют, если боли присутствуют на протяжении 3 месяцев за последние полгода.
В основе развития синдрома тазовой боли лежат воспалительные процессы в малом тазу. Метаболические, дистрофические и гемодинамические изменения в тканях провоцируют дисбаланс между веществами, которые активируют и подавляют воспаление. В результате этого в периферических нервных окончаниях симпатической нервной системы развиваются стойкие функциональные нарушения. В результате этого в центральную нервную систему посылается чрезмерное количество патологических импульсов.
В спинном мозге также происходят нарушения, повышается чувствительность структур. Любые, даже неболевые импульсы, начинают восприниматься, как болевые. Центральная нервная система неправильно на них реагирует, поддерживая застойные явления в малом тазу. В результате периферические нервные волокна претерпевают еще большие изменения. По сути, возникает замкнутый круг, который состоит из неадекватных нервных импульсов и неадекватных ответов на них.
СХТБ встречается почти у половины женщин в возрасте 20-50 лет. Заболевание выявляют у мужчин возрастной категории 45-50 лет. Патология оказывает негативное влияние на качество жизни больного. Кроме постоянного дискомфорта, она провоцирует развитие неврологических нарушений. У пациентов нередко появляется онкофобия, депрессия, сексуальная дисфункция.
Виды синдрома хронической тазовой боли (СХТБ)
Синдром хронической тазовой боли у мужчин классифицируют по системе UPOINT, опираясь на преобладающие симптомы:
У женщин СХТБ развивается в три стадии:
Симптомы синдрома хронической тазовой боли
Общим проявлением синдрома для женщин и мужчин признана боль. Характеристики дискомфорта при СХТБ отличаются от таковых при органическом поражении внутренних органов.
Особенностями хронических тазовых болей считаются:
Для СХТБ характерна вариативность симптомов. У мужчин чаще возникают дизурические расстройства, похожие на хронический цистит или простатит. Зачастую у больных снижается либидо, развивается эректильная дисфункция. Возможны нарушения пищеварения, отсутствие аппетита. В некоторых случаях наблюдаются нарушения чувствительности в области гениталий, ощущение покалывания или холода.
У женщин болевые ощущения часто отдают в ягодицы, бедра, промежность, половые губы. Усиливаются во время физических нагрузок, статичного положения, при поднятии тяжестей, во время полового акта, в период овуляции и менструации. На фоне хронических болей часто наблюдаются раздражительность, бессонница, снижение работоспособности. Постепенно развивается депрессия. Субъективное восприятие боли изменяется. Пациентки часто характеризуют ее, как нестерпимую, жгучую, изматывающую.
Причины синдрома хронической тазовой боли
Ученые заявляют, что синдром хронической тазовой боли у женщин и мужчин развивается при сочетании иммунных, неврологических и эндокринных дисфункций с психологическими факторами. Однако в преимуществе случаев предпосылкой для развития заболевания являются реальные патологии внутренних органов. Причинами СХТБ у женщин являются:
Негинекологическими причинами СХТБ могут быть заболевания мочевыводящей и пищеварительной системы, неврологические патологии, опухоли почек, поражения суставов и костей. Примерно у 2% пациенток выяснить объективную причину развития синдрома не удается.
У мужчин синдром тазовой боли чаще всего вызван с инфекционными заболеваниями, протекающими латентно (микоплазмоз, хламидиоз, трихомониаз, вирусные инфекции). В ряде случаев наблюдается асептическое воспаление простаты на фоне микроциркуляторных нарушений, обусловленных отсутствием регулярной сексуальной жизни, варикозом вен, запорами, лишним весом, малоподвижным образом жизни. Повреждение периферических нервов может быть следствием перенесенной хирургической операции или неврологической патологии. Ишемические изменения в тканях усугубляют нерациональное питание, злоупотребление алкоголем, кофе, ожирение.
Тазовые дисфункции и болевые синдромы в практике врача уролога
Содержание:
В последнее время, особенно во франко- и испано-язычных медицинских кругах, значительно изменился подход к патогенезу, диагностике и лечению заболеваний органов малого таза.
Прежде всего, он стал комплексным или, как говорят в Европе, «мультимодальным», поскольку органы малого таза тесно связаны между собой, часто имеют общую эфферентную и эфферентную иннервацию, кровообращение, мышечно-связочный аппарат. Таким образом, поражение одного органа часто вовлекает в патологический процесс другие.
Как пример можно привести возникновение синдрома болезненного мочевого пузыря (не интерстициального цистита – это разные вещи, ниже будет объяснено, почему), у пациенток с аденомиозом или СРК.
Связано это с феноменом т.н. перекрестной сенсибилизации. Большинство тазовых органов получают сенсорную и моторную инервацию через n.pudendus. Кроме того, в некоторых случаях эти органы имеют представительство в одних и тех же, или соседних центрах головного мозга. Подробнее этот вопрос также будет рассмотрен ниже.
Во-вторых, все более преобладает точка зрения о снижении роли воспалительных заболеваний в патогенезе синдрома хронической тазовой боли. В настоящее время основную роль, по мнению французских коллег, играют миофасциальные (спастические) синдромы мышц тазового дна и нейропатия полового нерва, который неофициально называют king of perineum – «король промежности». В-третьих, изменилась терминология: все чаще вместо термина «синдром хронической тазовой боли» используют термин «синдром хронической промежностно-тазовой боли и дисфункции».
Мы надеемся, что на I Международном конгрессе по тазовым болям и дисфункциям, который состоится в Амстердаме, будет принята единая терминология.
В рамках настоящей статьи не представляется возможным рассмотреть все болевые синдромы и дисфункции органов малого таза, поэтому предлагаем обратить внимание на синдромы органов женского малого таза, имеющие отношение к практике уролога, то есть, на урогинекологические синдромы.
Нарушения накопительной и эвакуаторной функции мочевого пузыря:
Что касается синдрома болезненного мочевого пузыря, то это, по мнению G. Amarenco, состояние, обусловленное как раз перекрестной сенсибилизацией мочевого пузыря, вследствие поражения соседних органов, например – толстой кишки (СРК) или матки при аденомиозе. В этом случае количество рецепторов С-волокон также увеличивается, происходит центральная сенсибилизация – но это следствие патологического процесса в другом органе. Патологические изменения в собственной пластинке уротелия могут вызвать повреждение зонтичных клеток, подобное ИЦ – но в этом случае оно будет вторично.
Клинический случай
Пациентка 38 лет, не рожавшая. Обратилась по поводу длительно существующей (3 года) дизурии, поллакиурии, ноктурии, болевого синдрома с локализацией в области уретры, иррадиацией в правую нижнюю конечность. Были проведены неоднократные курсы антибактериальной терапии по поводу U. urealitycum. Посевы мочи стерильны, общие анализы мочи – без изменений. Проведенная цистоскопия выявила визуальные признаки лейкоплакии в области треугольника Льето.
Патоморфологическое исследование: данных за лейкоплакию не выявлено.
Пациентке выполнена ТУР измененного участка в области треугольника Льето. После операции состояние несколько улучшилось, однако через месяц вернулось к ситуации, предшествовавшей вмешательству. На момент осмотра заполнение дневника мочеиспускания продемонстрировало 41 микцию в сутки, средний объем мочеиспускания – 37 мл.
Пациентка осмотрена совместно с профессором Э. Ботраном (L’Avancee Perinneal-Pain Clinic, Aixen-Provence).
Обследование выявило аденомиоз, повышение тонуса правой внутренней обтураторной мышцы, болезненность в триггерной точке m. obturatorius int.
По экспертному мнению профессора Ботрана, в данном случае имеет место синдром болезненного мочевого пузыря, вызванный перекрестной сенсибилизацией вследствие аденомиоза и отягощенный миофасциальной реакцией правой внутренней обтураторной мышцы. Кроме того, вследствие нейрогенного воспаления в lamina propria уротелия, вызванного перекрестной сенсибилизацией, у пациентки имеется повреждение уротелия.
Патогенез этого состояния может быть следующим. Аденомиоз, как и любое другое состояние, вызывающее хронический болевой синдром, приводит к снижению порога болевой чувствительности. Это хорошо продемонстрировано в эксперименте на крысах, названном pressure paw vocalization test.
Суть его в следующем: были взяты две группы крыс, у одной вызывался хронический болевой синдром введением химического реагента под кожу спины, другая группа оставалась интактна. Через месяц проводили тест, сдавливая специальным устройством крысам обеих групп лапку. Определялся порог вокализации, т.е. когда крысы начинали пищать. Так вот, до начала исследования порог у крыс обеих групп был одинаковый. Но через месяц, в группе крыс с хронической болью вокализация возникала при гораздо более слабом давлении на лапу, по сравнению с интактными крысами. Это представляется вполне логичным. Боль – сигнал о повреждении тканей. Если боль стала хронической, значит, головной мозг не предпринял действий, достаточных для ликвидации причины боли. Следовательно, необходимо снизить болевой порог, чтобы мотивировать ЦНС на более активные действия.
Следующий этап – периферическая сенсибилизация. В пораженном органе увеличивается продукция фактора роста нервов (ФРН, NGF). Это приводит к увеличению количества рецепторов, аффилированных с демиелинизированными С-волокнами. Основная роль С-волокон – передача хронических болевых импульсов. Соответственно, увеличение их количества приводит к усилению болевого синдрома в пораженном органе. Однако, как мы уже обсуждали, органы малого таза имеют перекрестную иннервацию и в данном случае, количество рецепторов к С-волокнам увеличивается не только в эндо- и миометрии, но и в уротелии.
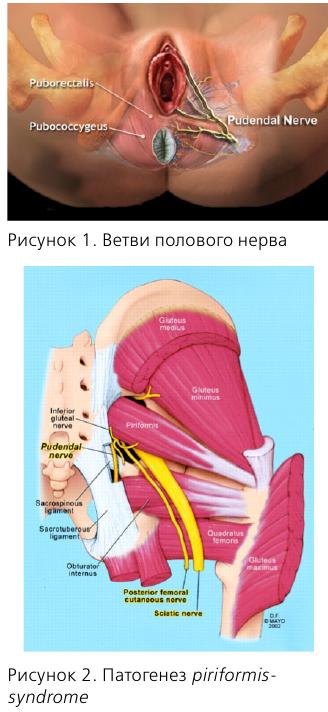
Кроме того, у этой пациентки диагностирована миофасциальная реакция m. obturatorius int. dext. Сокращение мышц – нормальная реакция на боль. Однако длительно существующая боль приводит к спастическим сокращениям, которые, в свою очередь, вызывают болевой синдром за счет накопления лактата в мышце и компрессии нервных волокон. Как пример, можно привести piriformis-syndrome, когда m. piriformis вызывает компрессию n. pudendus.
Возвращаясь к осмотренной пациентке – для лечения аденомиоза она была направлена к гинекологу. Кроме того, с целью терапии синдрома болезненного мочевого пузыря было рекомендовано:
Следует обратить внимание на эффективность, пусть и кратковременную, ТУР треугольника Льето. Как известно, основная афферентная иннервация мочевого пузыря локализована в области треугольника Льето – видимо ТУР временно вывела из строя окончания афферентных волокон.
Нейропатия полового нерва
Основным симптомом нейропатии полового нерва является боль в одной или более областях, иннервируемых n. pudendus или его ветвями.
Это области прямой кишки, заднего прохода, уретры, промежности и гениталий. Одним из типичных симптомов является усиление боли в положении сидя и прогрессирование в течение дня.
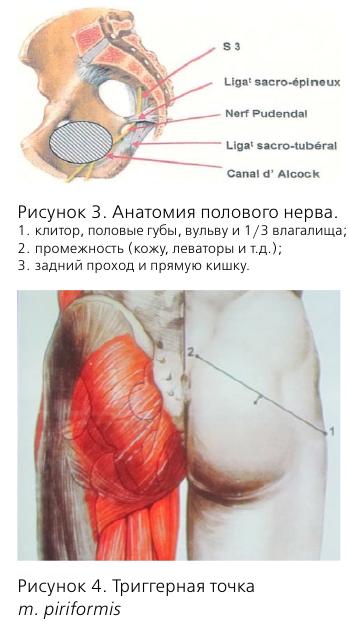
Причины нейропатии обсуждаются до сих пор, но наиболее известной является компрессия полового нерва в канале Алкока.
Другими причинами являются: piriformis-syndrome, повреждение полового нерва в процессе родов, травмы малого таза и злокачественные новообразования. Поэтому, при любых хронических тазовых болях желательно проведение МРТ.
Также активно обсуждается роль вируса герпеса – косвенным доказательством является эффективность ацикловира и валацикловира в некоторых случаях ПН.
Существуют т.н. Нантские критерии ПН, которые разработаны J.J. Labat, R. Robert, G. Amarenco. Выделено пять основных критериев:
Обычно пациенты описывают боль при ПН как нейропатическую, т.е. жжение, парестезии. Чаще всего боль локализуется с одной стороны. Весьма характерно ощущение инородного тела в прямой кишке.
Несколько слов об анатомии n. pudendus. В составе полового нерва имеются как афферентные, так и эфферентные волокна, что обусловливает сенсорные и двигательные нарушения соответствующих органов.
Половой нерв входит в малый таз на уровне S2-S4, проходит через f. piriformis, затем через канал Алкока и делится на 3 ветви.
Предполагается, что дисфункция полового нерва может привести к симптомам гиперактивного мочевого пузыря преимущественно сенсорного генеза, за счет повышения количества С-волокон в мочевом пузыре, а также за счет перекрестной сенсибилизации, о которой мы уже упоминали, в органах, получающих ту же иннервацию по причине конвергенции сенсорных путей в малом тазу.
Диагностика ПН основана на указанных выше Нантских критериях, кроме того, необходимо пальпировать триггерные точки m. piriformis и m. obturatorius для диагностики миофасциальных синдромов.
В диагностике компрессии полового нерва в канале Алкока может помочь трансвагинальное УЗИ с оценкой кровотока в a. pudenda и v. pudenda, т.к. при компрессии нерва эти сосуды также сдавливаются и скорость кровотока на стороне поражения снижается.
Лечение нейропатии полового нерва
Медикаментозное лечение обычно включает прегабалин, начиная с 75 мг два раза в сутки с титровкой дозы до 600 мг/сутки. Для расслабления мышц используют вагинальные суппозитории с диазепамом, инъекции локальных анестетиков с глюкокортикоидами в заинтересованные мышцы. В случае положительного эффекта вводится ботулинический токсин под ЭМГ-контролем.
Для диагностики и лечения используется блокада полового нерва под ентгенологическим или УЗ-контролем. Обычно вводится 5 мл 0,5% бупивакаина с 80 мг триамци-нолона – 3 инъекции.
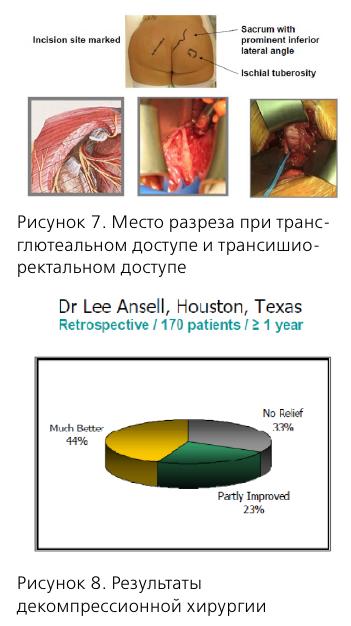
Хирургическое лечение проводится только при доказанной компрессии полового нерва, резистентной к медикаментозной терапии. Значительное улучшение достигается только в 44% случаев. Другие авторы сообщают о 62% эффективности (Э. Ботран), 70% (Р. Роберт).
Показания к декомпресии полового нерва, ее методика требуют дальнейшего обсуждения и изучения.
Миофасциальные синдромы малого таза
Миофасциальные синдромы или хроническая миофасциальная боль – это хронические болевые синдромы и дисфункции, вызванные хроническим спазмом мышечно-связочного аппарата малого таза.
Эти синдромы достаточно широко распространены, однако редко диагностируются в урологической практике. Например, Skootsky S. cообщает о 30% пациентов с хронической тазовой болью, у которых были диагностированы миофасциальные синдромы в специализированных клиниках по лечению болевых синдромов, при этом Bartoletti R. опубликовал данные о 5540 пациентах, страдающих СХТБ, обследованных в 28 итальянских урологических клиниках – миофасциальные синдромы выявлены только в 13,8% случаев.
Следовательно, необходимо более тщательно обследовать пациентов с хроническим циститом, хроническим простатитом, уретритом и т.д. с целью выявления нейропатических и миофасциальных синдромов.
Виды иофасциальных синдромов малого таза:
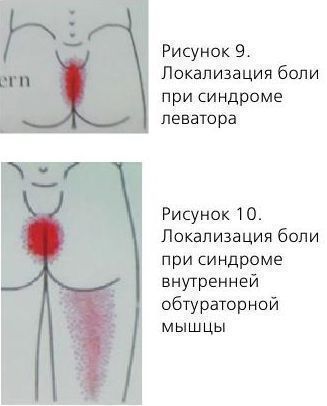
Синдром леватора
По данным J. Rigaud этот синдром встречается в 100% случаев у пациентов с СХТБ обоих полов.
Синдром внутренней обтураторной мышцы:
Гиперактивный мочевой пузырь с детрузорной гиперактивностью
Об этом виде ГАМПа написано достаточно, разработаны эффективные методы диагностики и лечения.
Препаратами выбора являются М-холинолитики, однако достаточно часто встречаются случаи недостаточной эффективности этих препаратов. Возможно, это обусловлено сочетанием ГАМП с ДО и ГАМП с повышенной чувствительностью мочевого пузыря, который будет рассмотрен ниже.
Гиперактивный мочевой пузырь с повышенной чувствительностью мочевого пузыря
Клинически этот вид ГАМП (который иногда называют «ГАМП без ГАМП») проявляется частым или даже постоянным ощущением позыва на мочеиспускание, но без императивных позывов и эпизодов ургентного недержания мочи у мужчин, как и у женщин. М-холинолитики, как правило, неэффективны.
Так же, как и при синдроме болезненного мочевого пузыря, происходит увеличение количества С-волокон и аффилированных с ними рецепторов. Причем иногда клинические и уродинамические проявления обоих состояний идентичны. Возможно, это различные по степени выраженности проявления одного и того же процесса.
Также большую роль играет центральная сенсибилизация. Именно поэтому эффективно применение тибиальной нейромодуляции – тибиальный нерв и половой нерв имеют одно и то же представительство в ЦНС.
Недержание мочи при напряжении (Стрессовая инконтиненция)
Патология и лечение недержания мочи заслуживает рассмотрения в отдельной статье, поэтому мы коснемся только ее взаимосвязи с тазовыми дисфункциями и болевыми синдромами.
Речь идет об осложнениях имплантации синтетических слингов трансобтураторным доступом. Достаточно часто (2-8%) после этой процедуры возникает болевой синдром, связанный с проведением и персистенцией импланта в обтураторной мышце, с компрессией веток обтураторного нерва и возникновением миофасциального обтураторного синдрома. Иногда, кроме болевого синдрома, возникает симптоматика ГАМП, которая весьма трудно купируется.
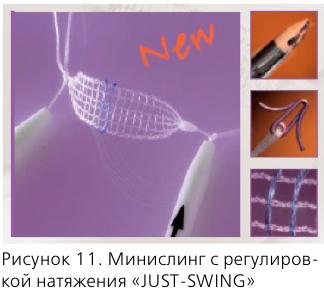
Возможным решением проблемы представляется использование новых видов слингов:
Для терапии болевых синдромов после TVT-O хирургии возможно использование инъекций в обтураторную мышцу смесей из анестетиков и глюкокортикоидов. При неэффективности – удаление импланта.
Заключение
Диагностика и лечение тазовых болевых синдромов и дисфункций представляется весьма актуальным и перспективным направлением в урологии. Активное внедрение современного подхода к тактике ведения пациентов с такими синдромами позволит улучшить качество оказания медицинской помощи и снизить затраты на лечение.
Следует также рассмотреть возможность организации специализированных кабинетов или отделений в составе ведущих урологических лечебных учреждений.
И.А. Аполихина, Я.Б. Миркин, Д.А. Бедретдинова, И.А. Эйзенах, О.Ю.Малинина.
Научный центр акушерства, гинекологии и перинатологии им. академика В.И. Кулакова, НИИ урологии Минздравсоцразвития РФ, Москва, NMTC International, ООО «Новые Медицинские Технологии».
Послеоперационное обезболивание. Часть 4. Современные средства обеспечения послеоперационной анальгезии
Основными задачами применения анальгетических средств в послеоперационном периоде являются: устранение страдания, причиняемого болью, создание психологического комфорта и повышение качества жизни пациентов в послеоперационном периоде; ускорение послеоперационной функциональной реабилитации; снижение частоты послеоперационных осложнений; сокращение сроков госпитализации и стоимости лечения.
Нужно отметить, что в настоящее время в большинстве развитых стран неадекватное послеоперационное обезболивание рассматривается как нарушение прав человека и осуществляется в соответствии с принятыми национальными и международными стандартами. В нашей стране во многих клиниках внедрена формулярная система использования лечебных препаратов тех или иных групп, целесообразность применения которых подтверждена данными доказательной медицины, а также обусловлена потребностями и особенностями конкретного лечебного учреждения. Многие авторы полагают, что все хирургические подразделения, а также отделения анестезиологии, реанимации и интенсивной терапии должны иметь в своем арсенале только те анальгетики и анестетики, эффективность и безопасность назначения которых подтверждена доказательствами I (систематизированные обзоры и метаанализы) и II (рандомизированные контролируемые исследования с определенными результатами) уровня (табл. 1).
Таблица 1. Препараты, применение которых для послеоперационного обезболивания обосновано данными доказательной медицины (Acute Pain Management: Scientific Evidence, 2-nd edition, 2005).
Группа
Препараты
Дозы, путь введения
Неопиоидные анальгетики, НПВП
Диклофенак
Кетопрофен (Кетонал ®)
Кеторолак (Кеторол ®)
75 мг (150 мг суточная), в/м
50 мг (200 мг), в/м
30 мг (90 мг), в/м
Неопиоидные анальгетики, прочие
1 г (4 г), в/в инфузия в течение 15 минут
Опиоидные анальгетики, сильные
5-10 мг (50 мг), в/в, в/м
20 мг (160 мг), в/в, в/м
Опиоидные анальгетики, слабые
100 мг (400 мг), в/в, в/м
Лидокаин 2%
Бупивакаин (Маркаин®) 0, 25%, 0, 5%
Ропивакаин (Наропин®0, 2%, 0, 75%, 1%
(800 мг суточная) *
(400 мг суточная) *
(670 мг суточная) *
*инфильтрация краев раны, интраплевральное введение, продленная блокада периферических нервов и сплетений, продленная эпидуральная анальгезия.
Мировой опыт послеоперационного обезболивания позволяет выделить следующие основные современные тенденции в борьбе с ПБС:
— широкое применение неопиоидных анальгетиков – нестероидных противовоспалительных препаратов (НПВП) и парацетамола; в различных европейских клиниках частота назначения данных препаратов в качестве базиса послеоперационного обезболивания составляет от 45 до 99%;
— ограничение использования опиоидных анальгетиков, особенно внутримышечного варианта их введения, что обусловлено низкой эффективностью и значительным количеством побочных эффектов данной методики;
— мультимодальный характер послеоперационного обезболивания, т. е. одновременное назначение нескольких препаратов или методов обезболивания, способных воздействовать на различные механизмы формирования болевого синдрома.
Длительность проведения послеоперационного обезболивания является достаточно вариабельной величиной и зависит как от интенсивности болевой афферентации и, следовательно, от травматичности хирургического вмешателсьтва, так и от индивидуальной толерантности пациента к боли. Необходимость целенаправленного купирования ПБС возникает, как правило, в течение первых 4 суток послеоперационного периода (табл. 2).
Таблица 2. Потребность в обезболивании после различных по объему операций.
Хирургическое вмешательство
Продолжительность обезболивания, часы
Вмешательства на верхнем этаже брюшной полости и диафрагме
Вмешательства на нижнем этаже брюшной полости
Операции на тазобедренном суставе
Операции на конечностях
Лапароскопические операции среднего объема
Таблица 3. Методы и средства послеоперационного обезболивания.
1. Традиционное введение опиоидов: внутримышечные инъекции по требованию.
2. Опиоидные препараты агонисты/антагонисты:
а) парентеральное введение опиоидов: внутривенно болюсно, длительная внутривенная инфузия, контролируемая пациентом анальгезия.
б) непарентеральное введение опиоидов: щечное/подъязычное, пероральное, трансдермальное, назальное, ингаляционное, внутрисуставное
3. Неопиоидные анальгетики с системным введением:
а) нестероидные противоспалительные препараты
б) ацетаминофен (парацетамол)
4. Методы регионарной анестезии:
а) эпидуральное введение опиоидов;
б) нестероидные противовоспалительные препараты;
5. Нефармакологические методы:
6. Сочетанное использование представленных методов
Ниже приводятся основные используемые в современной хирургической клинике средства и методы обезболивания с позиций баланса их эффективности и безопасности.
Опиоидные анальгетики.
Данная группа лекарственных препаратов десятилетиями считалась средством выбора для купирования ПБС. Однако в настоящее время опиоидные анальгетики отнюдь не являются «золотым стандартом» в лечени пациентов с острой болью. Тем не менее, по оценкам целого ряда отечественных и зарубежных специалистов, эффективность обезболивания при традиционном назначении опиоидов в качестве монотерапии не превышает 25-30%. Однако постепенное отчуждение от чрезмерной приверженности опиоидам в послеоперационном периоде связана не столько с их недостаточной эффективностью, сколько с целым рядом серьезных побочных эффектов, возникающих при их использовании (табл. 4).
С точки зрения фармакодинамики опиоидные анальгетики являются агонистами или антагонистами различных видов опиоидных рецепторов ЦНС (мю-, дельта-, каппа-). Препараты опиоидной группы активируют эндогенную антиноцицептивную систему (центральная анальгезия), однако не влияют на периферические и сегментарные неопиоидные механизмы ноцицепции и не предотвращают центральную сенситизацию и гиперальгезию. Попытки увеличения эффективности обезболивания и снижения частоты побочных эффектов опиоидных анальгетиков основаны на варьировании способов их введения (в том числе и у одного пациента): внутривенный, внутримышечный, эпидуральный, трансдермальный, сублингвальный, ректальный. Наиболее распространенным, но при этом наиболее небезопасным и наименее эффективным способом введения опиоидов является внутримышечная инъекция. Данная методика наиболее часто приводит к неадекватному обезболиванию – более 60% пациентов отмечают неудовлетворительное качество послеоперационной анальгезии. Причины этого кроются в том, что всем пациентам вводятся фиксированные дозы через стандартные временные интервалы, без учета индивидуальной вариабельности фармакокинетики; часто инъекции опиоидов производятся с большими перерывами, то есть тогда, когда болевой синдром уже выражен и его купирование по определению становится малоэффективным. Именно при внутримышечном введении опиоидов наиболее часто развивается депрессия дыхания, связанная, возможно, с кумуляцией препарата.
Таблица 4. Опиоидные анальгетики при купировании послеоперационного болевого синдрома.
Препарат
Дозировка и пути введения
Относительная анальгетическая активность
Побочные эффекты
Возможны выраженные угнетение дыхания, тошнота, рвота, высокая степень привыкания и максимальный наркогенный потенциал
Угнетение дыхания, тошнота, рвота, высокая степень привыкания и наркогенный потенциал
Угнетение дыхания, тошнота, рвота, наличие привыкания и наркогенного потенциала
Необходимо отметить еще один важный аспект, ограничивающий применение опиоидных анальгетиков в отечественной клинической практике. Использование опиоидных анальгетиков для послеоперационного обезболивания в Российской Федерации строго регламентировано существующими приказами руководящих органов здравоозранения. Например, приказом № 257 Департамента здравоохранения г. Москвы от 2004 г. определяется, в частности, норматив потребления опиоидных препаратов в ампулах на 1 койку различных отделений хирургического профиля в год. Назначение опиоидного препарата как в хирургическом отделении, так и в отделении интенсивной терапии в большинстве ЛПУ сопровождается колоссальным количеством формальных сложностей, что нередко приводит к отказу медперсонала от использования ланных препаратов даже при необходимости назначения опиоидов. По тем же причинам самый современный метод применения опиоидов – контролируемая пациентом аналгезия, в наибольшей степени ориентированная на индивидуальные потребности пациента в обезболивании – в России не получила широкого распространения.
Неопиоидные анальгетики.
Термином «неопиоидные анальгетики» обозначается группа различных по химическому строению, фармакодинамике и, соответственно, механизму обезболивания лекарственных препаратов, применяемых для купирования ПБС с парентеральным, реже пероральным путем введения. Препараты данной группы, используемые как в моноварианте, так и в качестве средства адъювантной терапии, обладают различными анальгетическим потенциалом и совокупностью побочных эффектов (табл. 5).
Таблица 5. Неопиоидные анальгетики для купирования послеоперационной боли.
Класс
Препараты
Особенности терапии
Побочные эффекты
Антагонисты NMDA-рецепторов
Применяется как адъювант при введении опиоидов.
Малые дозы кетамина характеризуются опиоидсберегающим эффектом, повышением качества обезболивания
При использовании в малых дозах – не выражены. Сохраняют побочные эффекты опиоидов.
Антиконвульсанты
Используется как адъювантный препарат в комплексной терапии острой послеоперационной боли. Снижает потребность как в опиоидных, так и внеопиоидных анальгетиках.
Головокружение, сонливость, периферические отеки.
Ингибиторы протеаз
Ингибирование синтеза медиаторов боли на этапе трансдукции, используются как средство адъювантной терапии ПБС
Нерушения в системе гемостаза (гипокоагуляция) – послеоперационные кровотечения.
Центральные α-адреномиметики
Воздействие на трансмиссию и модуляцию боли. Адъювант при опиоидной анальгезии.
Гипотензия, брадикардия, психические нарушения.
Бензодиазепины
Комбинированная терапия с применением феназепама и тизанидина снижает выраженность фантомных болей.
Сонливость, головокружение, психические расстройства
Из приведенных данных становится очевидным, что перечисленные в таблице неопиоидные анальгетики используются лишь как возможное дополнение к базисной терапии опиоидами, использование данных препаратов для купирования ПБС в моноварианте не практикуется.
Формально к группе неопиоидных анальгетиков относятся также нестероидные противовоспалительные препараты (НПВП) и ацетаминофен (парацетамол). Однако вследствие значительной востребованности в современной хирургической клинике данные препараты рассматриваются сейчас как отдельные подклассы средств для купирования ПБС.
Парацетамол.
Несмотря на то, что ацетаминофен (парацетамол) имеет более чем полувековую историю применения в качестве анальгетика и антипиретика, точный механизм действия этого препарата до сих пор не известен. Предполагается наличие центрального механизма действия парацетамола, включающего: подавление активности циклооксигеназы 2 типа в ЦНС, с чем связана профилактика развития вторичной гиперальгезии; подавление активности циклооксигеназы 3 типа, существование которой предполагается и которая, видимо, обладает селективной чувствительностью к парацетамолу; усиление активности нисходящих тормозных серотонинергических путей на этапе модуляции боли.
Потенциально опасным побочным свойством парацетамола является гепатотоксическое и нефротоксическое действие, которое может проявляться при превышении дозы 4 г/сут, особенно при наличии у пациента исходного нарушения функции печени и почек. Ограничениями к применению парацетамола являются: печеночно-клеточная недостаточность с лабораторными проявлениями (повышение уровня трансаминаз), почечная недостаточность, алкоголизм, алиментарная недостаточность, дегидратация.
Местные анестетики.
Важнейшей задачей мультимодальной анальгезии является прерывание афферентного потока ноцицептивных стимулов от периферических болевых рецепторов в органах и тканях к сегментарным структурам ЦНС (задним рогам спинного мозга). Эта задача может быть успешно решена при помощи различных методов регионарной и местной анальгезии. Важную роль в расширении применения методов региональной анальгезии сыграло появление современных местных анестетиков (бупивокаин, ропивокаин), а также детальная отработка методики регионарных блокад.
Эпидуральная анальгезия занимает ключевую позицию среди всех регионарных методов послеоперационного обезболивания. В ходе данной процедуры в эпидуральное пространство на уровне грудного или поясничного отделов позвоночника устанавливается катетер, через который болюсно или путем непрерывной инфузии вводятся местные анестетики. Эпидуральная анестезия является как средством обеспечения анальгезии в ходе операции (в том числе и в моноварианте), так и средством купирования ПБС. Многочисленными исследованиями была доказана принципиально более высокая эффективность продленной послеоперационной эпидуральной анальгезии по сравнению с системным введением опиоидных анальгетиков. Как указывалось выше сами опиоидные анальгетики также могут быть использованы для проведения эпидуральной анестезии. Известно, что эпидуральное введение местных анестетиков и опиоидов достоверно превышает анальгетический эффект использования данных препаратов в отдельности. Тем не менее само по себе эпидуральное введение опиоидов чревато возникновением серьезных побочных эффектов от угнетения дыхания до выраженного кожного зуда. На сегодняшний день принято считать, что преимущества эпидурального введения опиоидных анальгетиков в абдоминальной хирургии не перевешивают риска осложнений самой методики эпидуральной анестезии по сравнению с парентеральным назначением аналогичных препаратов.
Помимо собственно анальгетического эффекта позитивное влияние прослеоперационной продленной эпидуральной анальгезии заключается в прерывании нисходящих симпатических эфферентных импульсов, следствием чего являются улучшение висцерального кровотока (активизация репаративных процессов в зоне вмешательства), повышение активности парасимпатической нервной системы (разрешение пареза пищеварительной трубки).
С точки зрения доказательной медицины (Acute Pain Management: Scientific Evidence, 2-nd edition, 2005) преимущества продленной эпидуралной анальгезии включают: более высокое качество обезболивания в сравнении с парентеральным введением опиоидов; улучшение показателей газообмена и снижение частоты послеоперационных легочных осложнений по сравнению с опиоидной анальгезией; ускорение восстановления функции желудочно-кишечного тракта после абдоминальных операций и снижение частоты местных осложнений.
Тем не менее и у эпидуральной анестезии есть ряд существенных ограничений. Сама по себе эпидуральная анестезия является сложной инвазивной процедурой, потенциально опасной в плане развития как местных (инфекционный процесс, повреждение нервных корешков, сосудов паутинной оболочки, твердой мозговой оболочки), так и системных осложнений (депрессия дыхания, кардиотоксические эффекты, артериальная гипотензия). В этой связи проведение эпидуральной анестезии требует наличия специальных навыков у врача-анестезиолога и постоянного мониторинга состояния пациента в отделении интенсивной терапии, реже – в хирургическом отделении.
В последние годы все большую популярность получает методика длительной инфузии местных анестетиков в полость операционной раны. В ходе ряда исследований было показано, что длительная инфузия местных анестетиков в течение 24-48 часов через катетер, установленный в ране, способна повысить качество обезболивания и снизить потребность в опиоидных анальгетиках. Работами отечественных авторов показано, что пролонгированная местная анестезия операционной раны за счет резорбции местного анестетика и присутствия его в плазме в низких концентрациях способна оказывать системный противовоспалительный эффект. Как и в случае эпидуральной анальгезии эффект местных анестетиков при этом обусловлен блокадой не только ноцицептивных путей, но и симпатической иннервации. Говоря о применении пролонгированной местной анестезии операционной раны, следует заметить, что данная методика в настоящее время находится на стадии клинической апробации и ее широкое внедрение изначально ограничивают очевидный риск экзогенного инфицирования раны и реальная опасность системных токсических эффектов местных анестетиков (артериальная гипотензия, аритмии, угнетение дыхания) вследствие их резорбции тканями.
Мультимодальная периоперационная анальгезия.
Из приведенных выше характеристик и, что важнее, недостатков средств и методов купирования ПБС следует очевидное заключение о том, что в настоящее время не существует идеального анальгетика или метода лечения острой послеоперационной боли. Однако приблизиться к решению проблемы адекватности послеоперационного обезболивания вполне возможно, реализуя в клинике концепцию мультимодальной периоперационной анальгезии, предусматривающей одновременное назначение двух и более анальгетиков и/или методов обезболивания, обладающих различными механизмами действия и позволяющих достичь адекватной анальгезии при минимизации побочных эффектов до, во время и после хирургического вмешательства (см. рис. ).
Таблица 6. Варианты схем мультимодальной периоперационной анальгезии, ориентированных на травматичность хирургических вмешательств.