Гепатофугальный кровоток в воротной вене что значит
Доплер сосудов печени (лекция на Диагностере)
Кровоснабжение печени организовано через артерии, отводящие и приводящие вены. При доплерографии печеночную артерию, печеночные и воротные вены можно отличить по неповторимой форме спектра (подробнее смотри Доплер сосудов начинающим).
Доплер печеночной артерии
В печеночной артерии и воротной вене гепатопетальный кровоток (К печени). Печеночная артерия несет 20-30% объема крови, а воротная вена — 70-80%. После приема пищи кровоток в воротной вене нарастает, а артериальная фракция сокращается. При портальной гипертензии растет сопротивление в системе воротной вены, тогда печеночная артерия компенсаторно увеличивается.
Нажимайте на картинки, чтобы увеличить.
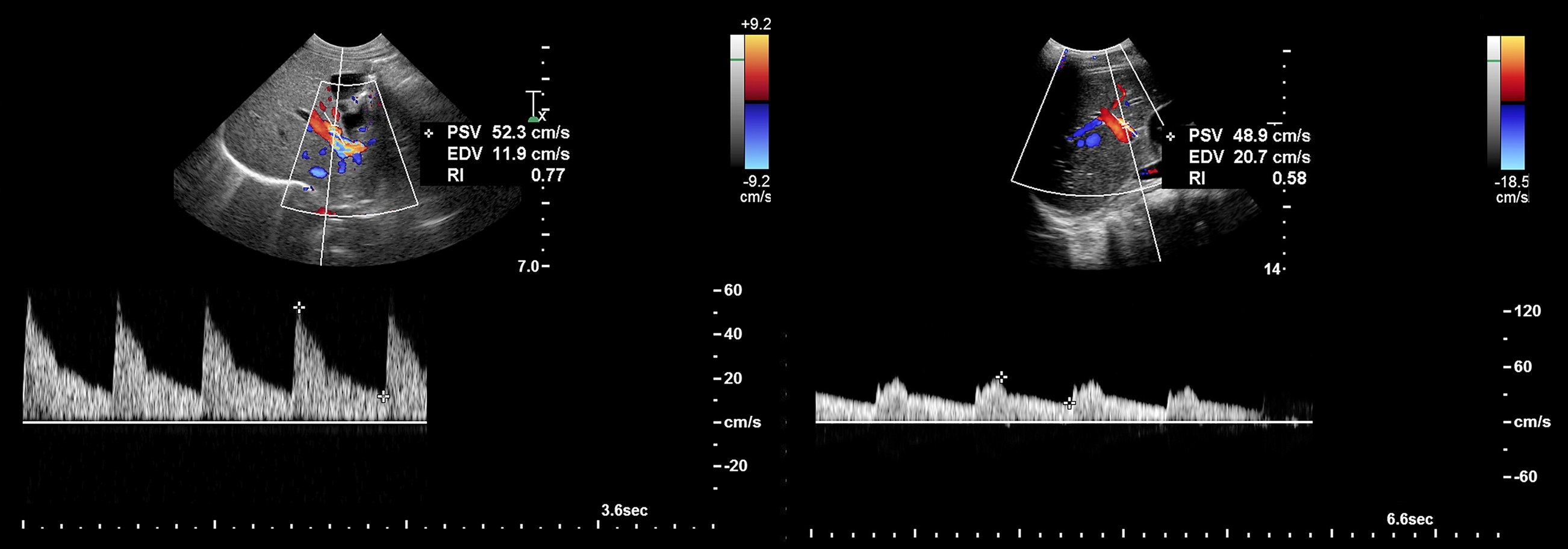
Рисунок. На УЗИ разные сегменты печеночной артерии у здоровых детей. В печеночной артерии кровоток К датчику — красный цвет при ЦДК и спектр выше базовой линии. Спектр с высоким диастолическим потоком и низким сопротивлением: общая печеночная артерия у новорожденного (1) — RI 0,77; левая печеночная артерия у мальчика 13-ти лет (2) — RI 0,58.
Рисунок. Печеночная артерия в норме имеет низкое сопротивление — RI 0,55-0,8 (2). RI>0,8 (1) вызывает настороженность. RI В воротных венах индекс пульсации PI=V2/V1, в отличие от артериального PI=(V1-V2)/Vmean. В норме PI>0,5.
Особенности портального кровотока при хронических гепатитах и циррозах печени
Опубликовано в журнале:
Визуализация в клинике »» N18, Июнь 2001 PORTAL BLOOD FLOW IN PATIENTS WITH CHRONIC HEPATITIS AND LIVER CIRRHOSIS
Б.H. Левитан, Б.А. Гринберг
Levitan В.N., Grinberg B.A.
Астраханская медицинская академия, г. Астрахань
strakhan Medical Academy, Astrakhan
У 43 больных хроническим гепатитом (ХГ) и 71 больного циррозом печени (ЦП) проведены импульсная допплерография и цветовое допплеровское картирование (дуплексный допплер) сосудов портальной системы на ультразвуковом сканере «Logic 500» (США). Обнаружены значительные нарушения допплерографических показателей венозного и артериального кровотока, выраженные в наибольшей степени у больных ЦП. Анализ характера изменений показателей допплерографии позволил выделить пять типов портального кровотока при ЦП: 1) нормокинетический (13% больных) без существенных изменений портального кровотока; 2) гиперкинетический с преимущественным увеличением параметров линейной скорости кровотока в воротной вене (ВВ) при незначительном нарастании ее диаметра (12%); 3) гиперкинетический с преимущественным увеличением диаметра ВВ (20% больных). Конгестивный индекс был увеличен. Объемный кровоток в ВВ возрастал, главным образом, за счет ее расширения. Линейная скорость кровотока по ВВ при этом была незначительно сниженной или оставалась неизмененной; 4) гипокинетический (40% больных), при котором значительно снижалась линейная скорость кровотока в ВВ без увеличения ее диаметра, что приводило к уменьшению объемного кровотока в ВВ; 5) псевдонормокинетический (15% больных), при котором объемный кровоток в ВВ оставался в нормальных пределах, а конгестивный индекс был значительно повышен; существенно снижалась линейная скорость кровотока в ВВ при увеличении ее диаметра. Полученные данные открывают дополнительные возможности диагностики и лечения больных ХГ и ЦП.
Forty-three patients with chronic hepatitis (СП) and 71 patients with liver cirrhosis (LC) were provided pulse Doppler and Color Doppler Imaging (duplex Doppler) of the portal vessels using an ultrasound «Logic 500» scanner (USA). Noticeable disorders in the Doppler parameters of the venous and arterial blood flow were discovered. They were pronounced in LC patients to the largest extent. Analysis of the character of changes in the Doppler parameters made it possible to distinguish five types of the portal blood flow in LC: 1) normokinetic (13% of patients) without appreciable changes in the portal blood flow; 2) hyperkinetic with a predominant increase in the parameters of the linear blood flow velocity in the portal vein (PV) at a negligible enlargement of its diameter (12% of patients); 3) hyperkinetic with a predominant enlargement of PV diameter (20% of patients). The congestive index was increased. The volume blood flow in the PV rose mainly because of its enlargement. The linear velocity of PV blood flow was lowered insignificantly or remained unchanged; 4) hypokinetic (40% of patients) marked by an appreciable decrease in the linear velocity of PV blood flow without PV diameter enlargement, which led to the reduction of the volume blood flow in the PV; 5) pseudonormokinetic (15% of patients): in this case the volume blood flow in the PV remained within normal whereas the congestive index was substantially higher; the linear velocity of the blood flow in the PV dropped substantially at its diameter enlargement. The data obtained have contributed much to the diagnosis and treatment of patients suffering from CH and LC. («Визуализация в клинике», 2001, 18: 16-20)
Ключевые слова: хронический гепатит, цирроз печени, портальный кровоток, допплерография.
Key words: chronic hepetitis, liver cirrhosis, portal blood flow, Doppler.
Хронические диффузные заболевания печени (ХДЗП) занимают одно из ведущих мест среди заболеваний желудочно-кишечного тракта, что связано с их широким распространением, тяжестью течения и часто неблагоприятным исходом [1, 7]. В последние годы среди неинвазивных методов диагностики ХДЗП и портальной гипертензии важное место отводится ультразвуковым исследованиям [2-5, 8, 9]. Данные мировой литературы свидетельствуют, что дуплексное сканирование сосудов портальной системы в сочетании с цветовым допплеровским картированием является золотым стандартом для выявления нарушений портального кровотока при заболеваниях печени [10].
Однако до настоящего времени в литературе сохраняются противоречивые данные о параметрах кровотока в сосудах портальной системы при ХДЗП. Не выделены основные типы портальной гемодинамики при циррозах печени.
Целью работы явились изучение допплерографических особенностей портального кровотока у больных хроническим гепатитом (ХГ) и циррозом печени (ЦП), выделение и характеристика основных типов портального кровотока у больных ЦП.
Материал и методы
Комплексное ультразвуковое исследование выполнялось строго натощак на ультразвуковом сканере «Logic-500» (США) конвексным датчиком частотой 3,5 МГц по методике Г.И. Кунцевич и соавт. [4] и включало ультразвуковое исследование в реальном масштабе времени в В-режиме, импульсную допплерографию и цветовое допплеровское картирование сосудов брюшной полости.
При исследовании оценивали ультразвуковые свойства печени и селезенки (контуры, структура, размеры). При импульсной допплерографии и цветовом допплеровском картировании сосудов брюшной полости изучались воротная и селезеночная вены, общая печеночная и селезеночная артерии. В каждом сосуде измеряли диаметр (D), определяли максимальную систолическую скорость кровотока (Vmах), конечно-диастолическую скорость кровотока (Vmin), максимальную линейную скорость кровотока, усредненную по времени (ТАМХ); рассчитывали объемную скорость кровотока (Q).
Для воротной вены рассчитывали конгестивный индекс (СI) по формуле:
Для интегральной оценки соотношения кровотока в воротной и селезеночной венах нами предложен воротно-селезеночный венозный индекс (ВСВИ), который рассчитывали по формуле:
Для оценки кровотока в артериальных сосудаx рассчитывали пульсационный индекс (РI) и индекс периферического сопротивления (RI). Для интегральной оценки соотношения артериального и венозного кровотока в печени рассчитывали индекс артериальной перфузии (ИАП) по формуле:
Для оценки соотношения параметров кровотока в воротной вене и общей печеночной артерии нами предложен печеночный сосудистый индекс (ПСИ), который рассчитывали по формуле:
Результаты и их обсуждение
Данные о параметрах кровотока в венах и артериях портальной системы приведены в табл. 1 и 2.
Как следует из табл. 1, у первой группы больных зарегистрировано достоверное увеличение диаметpa воротной и селезеночной вен, СI, а также снижение параметров линейной скорости кровотока в воротной вене (Vmах, Vmin, ТАМХ) по сравнению со второй (больные ХГ) и контролем. Показатели объемной скорости кровотока (Q) в воротной вене во всех трех группах достоверно не различались. В то же время Q в селезеночной вене у больных первой и второй групп была достоверно выше, чем в контроле. ВСВИ был достоверно ниже в первой группе больных по сравнению с больными второй группы и контролем.
У больных второй группы, по сравнению с контролем, выявлено снижение Vmах в воротной вене, a также увеличение СI, диаметра селезеночной вены и Q в селезеночной вене. Таким образом, уже у больных ХГ развивались изменения портальной гемодинамики: некоторое снижение линейной скорости кровотока в воротной вене, незначительное увеличение диаметра селезеночной вены и объемной скорости кровотока в ней.
У больных ЦП происходила значительная перестройка гемодинамики в венах воротной системы, выражавшаяся в увеличении диаметра воротной и селезеночной вен, а также в снижении показателей линейной скорости кровотока в воротной вене. При этом объемная скорость кровотока в ней сохранялась в нормальных пределах. В то же время у этой категории больных происходило увеличение объемного кровотока в селезеночной вене, т. е. перераспределение кровотока в венах воротной системы в направлении селезенки.
Таблица 1. Параметры кровотока в венах воротной системы у больных ХДЗП
Воротная вена
Поражения воротной вены
Выделяют следующие виды патологий.
Портальная гипертензия. Данное заболевание характеризуется увеличением внутреннего давления в воротной вене. Причинами развития данной патологии могут быть вирусные гепатиты, печеночный цирроз, нарушения обменных процессов, тяжелые сердечные заболевания, тромбы печеночных, селезеночных вен и другие. Симптоматика выражена диспепсией, снижением веса, тяжестью в правом подреберье, общей слабостью.
Тромбоз. Данная тяжелая патология развивается при формировании кровяных сгустков в просвете воротной вены, препятствующих оттоку крови. Основными причинами развития тромбоза являются следующие: воспаление и злокачественные образования органов пищеварения, травмы печени, желчного пузыря, селезенки, аномалии свертываемости крови, цирроз, различные инфекции и другие. Патология проявляется болевыми ощущениями в области живота, тошнотой с последующей рвотой, повышением температуры, диспепсическим синдромом и другими симптомами.
Кавернозная трансформация. Заболевание характеризуется образованием сосудистых полостей (каверном), заполненных кровью, и развивается вследствие генетического порока формирования вен, заключающегося в их значительном сужении, частичном или полном отсутствии. Кавернозная трансформация является врожденной аномалией. Если она не была выявлена в детстве, то обнаруженная в зрелом возрасте указывает на прогрессирующую портальную гипертензию, вызванную гепатитом или циррозом.
Пилефлебит. Эта патология характеризуется гнойным воспалением воротной вены, спровоцированным перитонитом, возникшим после перенесенного острого аппендицита. Симптомами пилефлебита являются: сильный жар, боли в животе с признаками отравления, желтуха, внутреннее кровоизлияние в венозной области пищевода, желудка и другие.
Диагностика и лечение
Диагностические мероприятия включают в себя следующие этапы и методы: осмотр, сбор анамнеза, ультразвуковое обследование, компьютерную и магнитно-резонансную томографию, портографию. Полученные инструментальными обследованиями данные дополняются показателями анализов крови. Лечение зависит от вида и тяжести поражения, сопутствующих симптоматических патологий и других факторов.
Допплеровские исследования при хронических болезнях печени у детей
УЗИ аппарат HM70A
Экспертный класс по доступной цене. Монокристальные датчики, полноэкранный режим отображения, эластография, 3D/4D в корпусе ноутбука. Гибкая трансформация в стационарный сканер при наличии тележки.
Введение
Материалы и методы
С января 1993 по декабрь 1997 гг. было обследовано более 300 детей в возрасте от 1 года до 16 лет: с внепеченочной формой портальной гипертензии (200), хроническим гепатитом с минимально выраженной активностью (40), выраженной активностью (48), циррозом печени (начальной 52 и сформированной стадиями 55), гликогенозом (27). Кроме этого были обследованы 23 ребенка также с хроническим гепатитом и циррозом печени в процессе терапии, заключающейся в подсадках фетальной ткани человека (ФТЧ). Дети с портальной гипертензией обследовались до проведения оперативного лечения, через 14-20 дн. и 5-6 мес. после него. Пациенты с хроническим гепатитом, циррозом печени и гликогенозом были обследованы однократно. В процессе терапии ФТЧ 23 ребенка с этой патологией были обследованы до подсадки, через 7 дн. и через 6 мес. после каждой подсадки. Максимальное количество подсадок было 4. Таким образом, эти пациенты наблюдались в течение двух лет. Всем детям было проведено допплеровское исследование сосудов портальной системы, когда определяли показатели кровотока по воротной, печеночным и селезеночной венам и печеночной и селезеночной артериям. Кроме этого, у пациентов с анастамозом проводили оценку его проходимости и функционального состояния. Для выяснения характера изменения кровотока в целом у детей с диффузными болезнями печени оценивалась центральная и церебральная гемодинамика. Используемыми показателями для оценки кровотока служили максимальная, средняя и минимальная скорости, индекс резистентности и величина объемного кровотока. Показателями центральной гемодинамики служили ударный и минутный объемы, фракция изгнания и скорость выброса крови в аорту. Все дети с заболеваниями печени проходили клинико-лабораторное исследование, а большинству детей с внепеченочной формой портальной гипертензии было проведено ангиографическое исследование.
Результаты
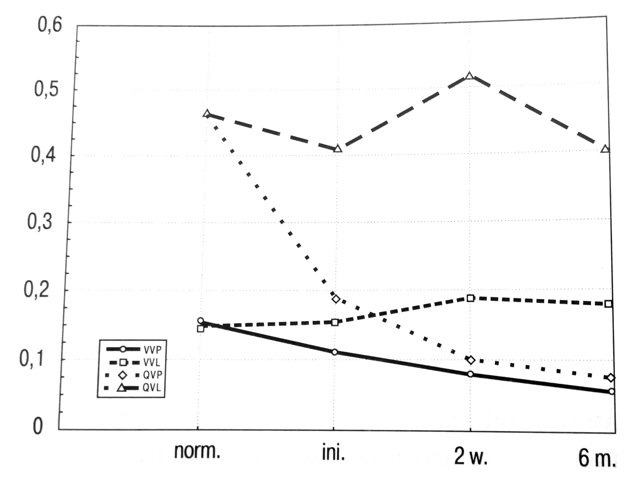
Рис. 1. Скорость и объемный кровоток по воротной и селезеночной венам у детей с внепеченочной портальной гипертензией до и после лечения.
Оценка кровотока у детей с хроническим гепатитом показала, что уже при минимальной степени активности определяется возрастание объемного кровотока по воротной и печеночным венам, причем за счет увеличения его скорости. Кровоток в селезенке оставался на нормальном уровне. По мере прогрессирования процесса линейная скорость потока замедлялась, но увеличение диаметра воротной вены приводило к нарастанию объемного кровотока. То же самое наблюдалось и в селезеночной вене (рис. 2). Кроме этого, увеличивалась и ригидность печеночной и селезеночной артерий. Показатели центральной и периферической гемодинамики практически не менялись.
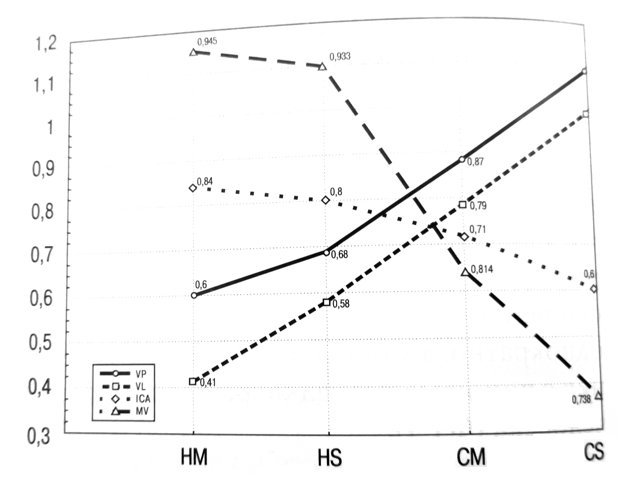
Рис. 2. Объемный кровоток, л/м, по воротной (VP), селезеночной (VL) венам, внутренней сонной артерии (ICA) и минутный объем крови (MV) у детей с хроническими болезнями печени.
По мере прогрессирования цирроза в сформированной стадии показатели объемного кровотока несколько увеличивались, как и индекс резистентности печеночной артерии (0,78±0,03), что говорило о возрастании периферического сопротивления паренхимы печени, на что косвенно указывала и линейная форма допплеровской кривой, полученная при оценке кровотока по печеночным артериям. Параллельно наблюдалось снижение объема крови, поступаемой в головной мозг, а также ударного и минутного объемов (см. рис. 2). Показатели портальной гемодинамики, полученные при исследовании детей с гликогенозом, находились в пределах контрольных цифр.
Конечные показатели, полученные через полгода после четвертой подсадки, т. е. примерно через 2 года после начала лечения, были несколько выше исходных данных, но эта разница статистически недостоверна. Характер изменения результатов гемодинамических показателей полностью соответствовал данным клинико-лабораторных исследований. При оценке контрольной группы детей с той же патологией, но находящихся на традиционном лечении, достоверных изменений показателей портальной гемодинамики по сравнению с исходными вообще не было (рис. 3).
Рис. 3. Объемный кровоток, л/м, по воротной вене у детей с хроническими болезнями печени на фоне лечения фетальной ткани человека.
Обсуждение
Увеличение объемного кровотока в селезенке указывает на развитие гиперкинетического типа циркуляции, как и у взрослого контингента больных [4, 5], и являющегося признаком портальной гипертензии. Нормальные показатели кровотока в сосудах портальной системы у детей с гликогенозом подтверждают, что основной причиной, определяющей его изменение, является разрастание соединительной ткани в печени, а не накопление гликогена или жира в гепатоцитах. В качестве объективной оценки состояния печени в процессе терапии с помощью подсадки фетальных тканей человека были использованы, кроме обычных клинико-лабораторных методов, эхо- и допплерографические методы исследования.
В результате было определено, что сразу после подсадки происходило сокращение размеров печени и селезенки и улучшение перфузии этих органов. Однако через 5-6 мес. все показатели практически возвращались к исходному уровню, чтобы затем снова положительно измениться после следующей подсадки. В результате после 4-5-й подсадки имело место незначительное улучшение кровоснабжения органов и сокращение их размеров. Сравнение этих же показателей с полученными при исследовании пациентов с той же патологией печени, но находившихся на традиционном лечении, продемонстрировало несколько лучший эффект при использовании фетальных тканей.
Выводы
В статье продемонстрированы три возможности использования допплерографии при патологии печени и ее сосудов. Можно сделать следующие выводы: метод допплерографии должен обязательно использоваться при оценке сосудов до и после шунтирующих операций; использование метода для оценки кровотока в портальной системе при хронических болезнях печени не имеет большого практического смысла; метод может быть использован для количественной оценки кровотока при динамических исследованиях в процессе терапии, что позволяет косвенно оценить эффективность проводимой терапии.
Литература
УЗИ аппарат HM70A
Экспертный класс по доступной цене. Монокристальные датчики, полноэкранный режим отображения, эластография, 3D/4D в корпусе ноутбука. Гибкая трансформация в стационарный сканер при наличии тележки.
Возможности эхографии в диагностике цирроза печени и портальной гипертензии
М.Г. ТУХБАТУЛЛИН, Г.Р. АХУНОВА, З.М. ГАЛЕЕВА
Казанская государственная медицинская академия, 420012, г. Казань, ул. Бутлерова, д. 36
Тухбатуллин Мунир Габдулфатович — доктор медицинских наук, профессор, заведующий кафедрой ультразвуковой диагностики, тел. (843) 233-30-17, e-mail: kafedra-uzi.kgma@mail.ru
Ахунова Гульнара Ринатовна — кандидат медицинских наук, ассистент кафедры ультразвуковой диагностики, тел. (843) 233-30-17, e-mail: gulnara-ahunova@mail.ru
Галеева Зарина Мунировна — кандидат медицинских наук, доцент кафедры терапии, тел. (843) 236-87-86, e-mail: zarina26@bk.ru
Статья посвящена диагностике цирроза печени и портальной гипертензии с применением эхографии в серошкальном и допплеровских режимах. В статье приведены данные о физиологии портального кровообращения, описана методика проведения ультразвукового исследования сосудов гепатобилиарной системы, изложена классификация цирроза печени, а также особенности портальной гемодинамики при циррозе печени, представлены эхографические критерии цирроза печени и портальной гипертензии на основании изучения литературных данных и собственных многолетних наблюдений.
Ключевые слова: цирроз печени, портальная гипертензия, ультразвуковая диагностика.
M.G. TUKHBATULLIN, G.R. AKHUNOVA, Z.M. GALEEVA
Kazan State Medical Academy, 36 Butlerova St., Kazan, Russian Federation 420012
Possibilities of sonography for the diagnosis of liver cirrhosis and portal hypertension
Tukhbatullin M.G. —D. Med. Sc., Professor, Head of the Department of Ultrasonic Diagnosis, tel. (843) 233-30-17, e-mail: kafedra-uzi.kgma@mail.ru
Akhunova G.R. —Cand. Med. Sc., Assistant of the Department of Ultrasonic Diagnosis, tel. (843) 233-30-17, e-mail: gulnara-ahunova@mail.ru
Galeeva Z.M. —Cand. Med. Sc.,Associate Professor of the Department of Therapy, tel. (843) 236-87-86, e-mail: zarina26@bk.ru
This article is devoted to the diagnosis of liver cirrhosis and portal hypertension with the use of sonography in the gray-scale and Doppler modes. The article presents data on the physiology of the portal circulation, describes a method of ultrasound investigation of vessels of the hepatobiliary system, gives a classification of liver cirrhosis and peculiarities of portal hemodynamics in case of liver cirrhosis. The article presents the sonographic criteria for liver cirrhosis and portal hypertension based on the study of literature data and personal long-term observations.
Key words: liver cirrhosis, portal hypertension, ultrasound diagnosis.
Цирроз печени — хроническое прогрессирующее полиэтиологическое заболевание, характеризующееся диффузным разрастанием соединительной ткани, патологической узловой регенерацией паренхимы с образованием пссвдодолек, уменьшением количества функционирующих полноценных гепатоцитов, а также перестройкой структуры паренхимы и сосудистой сети [1, 2].Цирроз печени занимает первое место среди причин смертности от болезней органов пищеварения (исключая опухоли). Распространенность составляет 2-3% (на основании данных аутопсий); наблюдают в 2 раза чаще у мужчин старше 40 лет по сравнению с общей популяцией [3].
Формирование при циррозе печени портальной гипертензии, варикозного расширения вен пищевода и желудка приводит к фатальным кровотечениям у половины больных, поэтому проблема своевременной диагностики циррозов и гепатитов как их предшественников является одной из самых острых в лучевой диагностике [4]. Скрытое течение гепатитов и цирроза и отсутствие конкретных жалоб в начальных этапах развития заболевания часто служит причиной поздней диагностики этих патологических состояний и приводит к формированию необратимой перестройки структуры печени [5].
Для постановки правильного диагноза и определения дальнейшей тактики ведения пациента, необходим комплексный анализ клинических, лабораторных исследований и данных, полученных методами медицинской визуализации. Среди наиболее информативных и доступных инструментальных методов исследования печени, ведущее место занимают ультразвуковые методы: зхография в B-режиме с допплерографией сосудистой системы [6].
Классификация цирроза печени
Всемирная ассоциация гепатологов (Акапулько, 1974) и ВОЗ (1978) рекомендовали простую морфологическую классификацию циррозов печени, основанную на минимуме критериев, согласно которой различают:
— мелкоузловую, или мелконодулярную (диаметр узлов от 1 до 3 мм);
— крупноузловую, или макронодулярную (диаметр узлов более 3 мм);
— смешанную (при которой наблюдаются различные размеры узлов) форму [7].
Большинство исследователей отмечают, что мелкоузловая форма характерна для ранней стадии процесса, а крупноузловая появляется на более поздних стадиях процесса. Смешанная форма диагностируется тогда, когда количество мелких и крупных узлов приблизительно одинаково [8].
В зависимости от этиологии различают цирроз печени: вирусный, алкогольный, лекарственный, вторичный билиарный, врожденный (гепатолентикулярная дегенерация, гемохроматоз, дефицит α1-трипсина, тирозиноз, галактоземия, гликогеноз), застойный (недостаточность кровообращения), болезнь и синдром Бадда — Киари, обменно-алиментарный (наложение обходного тонкокишечного анастомоза, ожирение, тяжелые формы сахарного диабета) и цирроз печени неясной этиологии (криптогенный, первичный билиарный, индийский детский) [7].
В 1986 г. Э. Чайльд и Дж. Пью предложили выделять цирроз трех степеней, стадий или классов, в зависимости от выраженности определенных параметров, неизменно претерпевающих нарушения (табл. 1).
Таблица 1.
Классификация цирроза печени по Чайльду — Пью
Параметр
(протромбиновое время или индекс)
где R — радиус сосуда (см); π — число «пи», равное 3,14
Печеночно-сосудистый индекс (ПСИ):
ПСИ = Vmean (ВВ) / PI (СПА);
где ВВ — воротная вена; PI — пульсационный индекс; СПА — собственная печеночная артерия
Индекс гиперемии (ИГ):
Общий печеночный объемный кровоток (ОПОК):
ОПОК = ОСК (ВВ) + ОСК (СПА)
Печеночно-портальное отношение (ППО):
ППО = ОСК (СПА) / ОСК (ВВ)
Допплеровско-перфузионный индекс (ДПИ):
ДПИ = ОСК (СПА) / ОПОК
Воротно-селезеночный индекс (ВСИ):
ВСИ = ОСК (ВВ) / ОСК (СВ);
где СВ — селезеночная вена
Систоло-диастолическое отношение (С/Д) и отношение средней скорости кровотока к минимальной в СПА (М/Д):
С/Д = Vmax (СПА) / Vmin (СПА);
М/Д = Vmean (СПА) / Vmin (СПА).
Классификация портальной гирпертензии
Цирроз печени является наиболее частой, но не единственной причиной портальной гипертензии. Портальная гипертензия — это клинический симптомокомплекс, который гемодинамически проявляется патологическим повышением портального градиента давления, что сопровождается формированием портосистемных коллатералей, через которые происходит сброс крови из воротной вены в обход печени. Портальный градиент давления — разница между давлением в воротной и нижней полых венах. В норме он составляет 1-5 мм рт. ст. Клинически значимой портальная гипертензия становится при повышении портального градиента давления >10 мм рт. ст.
Классификация портальной гипертензии основана на локализации портального блока:
— Тромбоз печеночных вен (синдром Бадда — Киари, инвазия опухолью).
— Обструкция нижней полой вены (мембрана в просвете нижней полой вены, инвазия опухолью).
— Заболевания сердечно-сосудистой системы (констриктивный перикардит, выраженная трикуспидальная регургитация).
o Болезнь Рандю — Ослера.
o Врожденный фиброз печени.
o Тромбоз ветвей портальной вены (тяжелый бактериальный холангит, злокачественные новообразования).
o Первичный билиарный холангит, первичный склерозирующий холангит.
o Гранулематозы (шистосомоз, саркоидоз, туберкулез).
o Хронический вирусный гепатит.
o Первичный билиарный цирроз.
o Миелопролиферативные заболевания.
o Нодулярная регенераторная гиперплазия.
o Идиопатическая (нецирротическая) портальная гипертензия.
o Болезнь Вильсона — Коновалова.
o Воздействие токсичных веществ (медь, мышьяк, 6-меркаптопурин).
o Все случаи цирроза печени.
o Острый алкогольный гепатит.
o Тяжелый вирусный гепатит.
o Острая жировая печень беременных.
o Интоксикация витамином А.
o Системный мастоцитоз.
o Печеночная пурпура.
o Цитотоксичные лекарственные препарты.
o Венооклюзионная болезнь.
o Алкогольный центрилобулярный гиалиновый склероз.
— Тромбоз воротной вены.
— Кавернозная трансформация воротной вены.
— Тромбоз селезеночной вены.
— Висцеральная артериовенозная фистула.
— Идиопатическая тропическая спленомегалия [2].
Эхографические признаки портальной гипертензии
Эхографические признаки портальной гипертензии представлены в табл. 4.
Таблица 4.
Эхографические признаки портальной гипертензии
или >15 см/сек
артериализация печени
+++
Для цирроза печени, сопровождающегося портальной гипертензией, характерны увеличение диаметра воротной вены и значительное снижение линейной скорости кровотока. Увеличение диаметра воротной вены обычно более выражено в период до развития портосистемных коллатералей. При появлении последних из-за сброса крови в систему нижней полой вены размер воротной вены может возвращаться к нормальному и скорость кровотока может увеличиваться. Впоследствии при нарастании степени печеночного блока возможно отметить вновь расширение просвета воротной вены, а также ее долевых ветвей, особенно левой [11, 23].Таким образом, показатели диаметра, линейной скорости кровотока по воротной вене зависят от количества и выраженности функционирующих портокавальных шунтов.
При допплерографическом исследовании (как в импульсноволновом, так и цветовом режимах) может отмечаться как замедление гепатопетального кровотока, так и его остановка или изменение направления тока крови на гепатофугальное. Гепатофугальный кровоток в основных ветвях, формирующих воротную вену, наблюдается постоянно у 8,3% больных и сочетается с уменьшением ее диаметра [11, 24].
Увеличение диаметра селезеночной вены является одним из ранних признаков портальной гипертензии. Однако расширение портальной и селезеночной вен не является достоверным признаком портальной гипертензии. Необходимо провести пробу Вальсальвы: отсутствие изменений диаметров вен, особенно портальной вены, значительно повышает диагностическую значимость (до 80%) увеличения их размеров [8]. Увеличение скорости кровотока по селезеночной венепроисходит по мере нарастания степени тяжести цирроза печени. У пациентов с циррозом печени класса В и С допплерографически может определяться гепатофугальный (по направлению к селезенке) кровоток.
Увеличение диаметра печеночной артерии происходит по мере развития портальной гипертензии. У больных циррозом печени наблюдается увеличение кровотока по печеночной артерии. Доля артериальной крови в общем печеночном кровотоке возрастает на 60-80%. Это связывают с падением внутрипеченочного сопротивления вследствие открытия на этом уровне артериовенозных анастомозов [25].
Спленомегалия также является одним из ранних признаков портальной гипертензии. Увеличение длины селезенки более 120 мм, толщины более 50 мм, ширины более 70 мм и площади максимального среза в сагиттальной плоскости сканирования более 40-50 см 2 расценивается как увеличение размера органа. Увеличение размеров селезенки происходит с нарастанием степени тяжести цирроза печени [11].
Портокавальные анастомозыпредставляют собой систему соустий между притоками воротной вены и притоками верхней и нижней полой веной. В норме они находятся в спавшемся состоянии и начинают раскрываться по мере нарастания портальной гипертензии. Обнаружение при ультразвуковом исследовании портокавальных анастомозов может быть достаточным для постановки диагноза латентно протекающей портальной гипертензии даже при отсутствии структурных изменений печени. С утяжелением стадии цирроза печени нарастает количество интраабдоминальных шунтов, преимущественно спленоренальных, и происходит реканализация пупочной вены. Формирование патологического сброса крови сопровождается асцитом[26, 27].
Однако обнаружение портокавальных анастомозов не является патогномоничным для цирроза печени. Портокавальные анастомозы могут наблюдаться и при синдроме Бадда — Киари, при венозной компрессии внутрипеченочными опухолями, а также при артериовенозных фистулах у пациентов с вено-окклюзионными заболеваниями [28].
При прогрессировании нарушения портального кровотока регистрируется нарастающее количество свободной жидкости в брюшной полости. При небольших количествах свободной жидкости ее удобнее выявлять в малом тазу, латеральных карманах брюшной полости, слева от печени и под ее висцеральной поверхностью, где визуализируется тонкая анэхогенная полоска, повторяющая контур органа [11, 29].
Портокавальные анастомозы (портосистемные коллатерали)
Рисунок 3.
Возможные коллатерали при портальной гипертензии
Портопеченочные: околоподжелудочные (а), желудочно-сальниковые, короткие желудочно-венечные (при тромбозе селезеночной вены). Портосистемные коллатерали к верхней полой вене: желудочно-пищеводные (b), околопищеводные вены (с). Портосистемные коллатерали к нижней полой вене: околоподжелудочные (а), желудочно-почечная (d), пупочная (е), селезеночно-почечная (f), селезеночно-забрюшинная (g), брыжеечно-нижнеполые (h), околотолстокишечные (j), тазовые (k). CV — венечная вена; GEV — желудочно-сальниковые вены; IMV — нижняя брыжеечная вена; IVC — нижняя полая вена; LRV — левая почечная вена; LV — поясничные вены; PV — воротная вена; SGV — короткие вены желудка; SMV — верхняя брыжеечная вена; SV — селезеночная вена
При нарушении оттока по воротной вене портальная кровь оттекает в центральные вены через венозные коллатерали (рис. 3), которые при этом значительно расширяются. Их можно распределить в 4 основные группы:
1-я группа: вены подслизистого слоя пищевода, желудка, прямой кишки;
2-я группа: вены серповидной связки, околопупочные вены;
3-я группа: вены в связках между органами, внутрипеченочные ПКА;
4-я группа: вены, перераспределяющие кровь в левую почечную вену.
При прогрессировании цирроза печени и нарастании внутрипеченочного сосудистого сопротивления возникает допеченочный сброс крови по естественным портокавальным анастомозам, что в совокупности с внутрипеченочными портопортальными шунтами обуславливает уменьшение объема портальной крови в кровообращении печени [8, 30].
Цирроз печени является конечной стадией процесса фиброзирования и до настоящего времени считается необратимым состоянием. Непременными атрибутами этого заболевания являются печеночная недостаточность и портальная гипертензия, которая может привести к летальному исходу от кровотечения из варикозно расширенных вен желудочно-кишечного тракта. Важным является, как быстро компенсируется избыточное портальное давление. Это зависит прежде всего от скорости развития (состоятельности) портокавальных анастомозов.
Допплерографическое исследование сосудов печени позволяет проследить динамику развития (раскрытия) портокавальных анастомозов и прогнозировать течение цирроза печени. Использование комплексной эхографии у больных с циррозом печени с определением скорости, объема кровотока в сосудах воротной системы и портокавальных анастомозах, позволяет вывести оптимальные дифференциально-диагностические критерии для ранней диагностики портальной гипертензии.
1. Клиническая гастроэнтерология: Руководство для врачей / И.И. Дегтярев. — М.: Медицинское информационное агентство, 2004. — 616 с.
2. Лечение осложнений цирроза печени: методические рекомендации для врачей / В.Т. Ивашкин, М.В. Маевская. — М.: Литтера. — 2001 — 64 с. (Серия «Практические руководства»)
3. Клинические рекомендации. Гастроэнтерология / под ред. В.Т. Ивашкина. — М.: ГЭОТАР-Медиа, 2008. — 208 с.
4. Афукова O.A., Юдин A.JI. Лучевая диагностика цирроза печени (обзор литературы) // Медицинская визуализация. — 2005. — № 5. — С. 32-44.
5. Митьков В.В., Садоков В.М., Хитрова А.Н. и др. Неинвазивная допплерографическая диагностика цирроза печени на основе анализа времени поступления эхоконтрастного вещества в печеночные вены // Ультразвуковая и функциональная диагностика. — 2001. — № 2. — С. 14-18.
6. Seitz К., Wermke W., Haag К. Sonography in Portal Hypertension and TIPS. — Freiburg, 1998. — 64 р.
7. Садовникова И.И. Циррозы печени. Вопросы этиологии, патогенеза, клиники, диагностики, лечения // Русский медицинский журнал. — 2003. — № 2. — С. 37-42.
8. Тухбатуллин М.Г., Баширова Д.К., Раимова Р.Ф. Особенности комплексной эхографии при портальной гипертензии. Учебно-методическое пособие. — 2001. — 23 с.
9. Эхография в диагностике цирроза печени / М.К. Михайлов, М.Г. Тухбатуллин. — Москва: МЕДпресс-информ, 2003. — 96 с.
10. Vogt W. Value of ultrasound and doppler sonography in chronic hepatitis and liver cirrhosis Schweiz Rundsch Med Prax. 2005 Apr 20;94(16):639-43.
11. Практическое руководство по ультразвуковой диагностике. Общая ультразвуковая диагностика / под ред. В.В. Митькова. — 2-е изд. — М.: Видар-М, 2011. — 712 с.
12. Клиническое руководство по ультразвуковой диагностике / Ю.А. Брюховецкий, В.В. Митьков — М.: Видар-М., 2000. — 521 с.
13. Абдоминальная эхография: Справ. / А.И. Дергачев, П.М. Котляров — М.: ЭликсКом, 2003. — 352 с.
14. Зубарев A.B., Шипов О.Ю., Сюткин В.Е. Портальная гипертензия: диагностические возможности допплеровских ультразвуковых методик // Эхография. — 2001. — Т. 2, № 1. — С. 6-13.
15. Ультразвуковое исследование сосудов / В. Цвибель, Дж. Пеллерито — М.: Видар-М, 2008. — 656 с.
16. Наглядная гастроэнтерология: Учеб. пособ. / Пер. с англ. С.В. Демичева / Под ред. В.Т. Ивашкина. — М.: ГЭОТАР-Медиа, 2005. — 136 с.
17. Анатомия человека. В двух томах / Под ред. М.П. Сапина. — Изд. 5-е, перераб. и доп. — М.: Медицина. — 2001. — 640 с.
18. Сергиенко В.И., Петросян Э.А., Фраучи И.В. Топографическая анатомия и оперативная хирургия: В 2 т. / Под общ. ред. акад. РАМН Ю.М. Лопухина. — М.: ГЭОТАР-МЕД, 2001. — Т. 1. — 832 с.
19. Атлас анатомии человека: Учеб. пособие. — 2-е изд., стереотипное. — В 4 томах. Т.3. / Р.Д. Синельников, Я.Р. Синельников. — М.: Медицина, 1996. — 232 с.
20. Ультразвуковая диагностика. Базовый курс. Второе издание, перераб. и доп.: Пер. с нем. / М. Хофер. — М.: Мед. лит., 2013. — 128 с.
21. Цветовая дуплексная сонография. Практическое руководство / М. Хофер. — М.: Мед. лит., 2007. — 108 с.
22. Тухбатуллин М.Г., Раимова Р.Ф., Зиганшина Л.Ф. Гемодинамические нарушения в воротной системе при портальной гипертензии // Эхография. — 2002. — Т. З, № 3. — С. 331.
23. Акопян Н.Э., Хачатрян Г.Г. Количественная оценка комплексной диагностики диффузных заболеваний печени // Радиология-практика. — 2009. — № 3. — С. 18-20.
24. Ультразвуковая диагностика. Практическое руководство / Г. Шмидт / Пер. с англ. / Под общ. ред. проф. А.В. Зубарева. — М.: МЕДпресс-информ, 2009. — 560 с.
25. Koda M., Murawaki Y., Kawasaki H. Renovascular resistance assessed by color Doppler ultrasonography in patients with chronic liver diseases // I Gastroenterol Hepatol. — 2000 Dec. — 15(12). — Р. 1424-9.
26. Кунцевич Г.И., Белолопатко Е.А., Сидоренко Г.В. Оценка состояния портального кровообращения у больных циррозом печени по данным дуплексного сканирования // Визуализация в клинике. — 1994. — № 5. — С. 33-39.
27. Villar F., Goria O., Herve S. et al. Intrahepatic portocaval shunt: review of the literature, apropos of 1 case // Gastroenterol. Clin. Biol. — 2000 May. — 24 (5). — P. 582-584.
28. Martinoli C. et al. Doppler US of the hepatic veins // Europ. Radiology. — 2000. — Vol. 15. — P. 349.
29. Ультразвуковое исследование. Иллюстрированное руководство / Дж. Олти, Э. Хоуи, С. Вульстенхульм, М. Вестон / Пер. с англ. / Под ред. В.А. Сандрикова. — М.: ГЭОТАР-Медиа, 2010. — 256 с.
30. Цирроз печени и его осложнения. Трансплантация печени / Ю.Р. Шифф, М.Ф. Соррел, У.С. Мэддрей / Пер. с англ. — М.: ГЭОТАР-Медиа, 2012. — 592 с.
1. Degtyarev I.I. Klinicheskaya gastroenterologiya: Rukovodstvo dlya vrachey [Clinical Gastroenterology: A Guide for Physicians]. Moscow: Meditsinskoe informatsionnoe agentstvo, 2004. 616 p.
2. Ivashkin V.T., Maevskaya M.V. Lechenie oslozhneniy tsirroza pecheni: metodicheskie rekomendatsii dlya vrachey [Treatment of the complications of cirrhosis: guidelines for physicians]. Moscow: Littera, 2001. 64 p. (Seriya “Prakticheskie rukovodstva”)
3. Klinicheskie rekomendatsii. Gastroenterologiya, pod red. V.T. Ivashkina [Clinical guidelines. Gastroenterology, ed. by V.T. Ivashkin]. Moscow: GEOTAR-Media, 2008. 208 p.
4. Afukova O.A., Yudin A.JI. Radiation diagnosis of cirrhosis (review). Meditsinskaya vizualizatsiya, 2005, no. 5, pp. 32-44 (in Russ.).
5. Mit’kov V.V., Sadokov V.M., Khitrova A.N. et al. Non-invasive Doppler sonography diagnosis of cirrhosis based on an analysis time of receipt echocontrast substance in hepatic veins. Ul’trazvukovaya i funktsional’naya diagnostika, 2001, no. 2, pp. 14-18 (in Russ.).
6. Seitz K., Wermke W., Haag K. Sonography in Portal Hypertension and TIPS. Freiburg, 1998. 64 r.
7. Sadovnikova I.I. Cirrhosis of the liver. The etiology, pathogenesis, clinical manifestations, diagnosis, treatment. Russkiy meditsinskiy zhurnal, 2003, no. 2, pp. 37-42 (in Russ.).
8. Tukhbatullin M.G., Bashirova D.K., Raimova R.F. Osobennosti kompleksnoy ekhografii pri portal’noy gipertenzii. Uchebno-metodicheskoe posobie [Features integrated ultrasound in portal hypertension. Teaching aid]. 2001. 23 p.
9. Mikhaylov M.K., Tukhbatullin M.G. Ekhografiya v diagnostike tsirroza pecheni [Sonography in the diagnosis of cirrhosis]. Moscow: MEDpress-inform, 2003. 96 p.
10. Vogt W. Value of ultrasound and doppler sonography in chronic hepatitis and liver cirrhosis Schweiz Rundsch Med Prax. 2005, Apr., 20; 94(16):639-43.
11. Prakticheskoe rukovodstvo po ul’trazvukovoy diagnostike. Obshchaya ul’trazvukovaya diagnostika, pod red. V.V. Mit’kova [A practical guide to ultrasound. General ultrasound. Edited by V.V. Mitkov]. Moscow: Vidar-M, 2011. 712 p.
12. Bryukhovetskiy Yu.A., Mit’kov V.V. Klinicheskoe rukovodstvo po ul’trazvukovoy diagnostike [Clinical guidelines for ultrasound]. Moscow: Vidar-M., 2000. 521 p.
13. Dergachev A.I., Kotlyarov P.M. Abdominal’naya ekhografiya [Abdominal sonography]. Moscow: EliksKom, 2003. 352 p.
14. Zubarev A.B., Shipov O.Yu., Syutkin V.E. Portal hypertension: Doppler ultrasonic diagnostic capabilities methods. Ekhografiya, 2001, vol. 2, no. 1, pp. 6-13 (in Russ.).
15. Tsvibel’ V., Pellerito Dzh. Ul’trazvukovoe issledovanie sosudov [Ultrasonography vessels]. Moscow: Vidar-M, 2008. 656 p.
16. Naglyadnaya gastroenterologiya: ucheb. posob., per. s angl. S.V. Demicheva, pod red. V.T. Ivashkina [Transparent Gastroenterology: Textbook. benefits. Transl. from English by S.V. Demichev. Edieted by V.T. Ivashkin]. Moscow: GEOTAR-Media, 2005. 136 p.
17. Anatomiya cheloveka. V dvukh tomakh, pod red. M.P. Sapina [Human Anatomy. In two volumes. Edited by M.P. Sapin]. Moscow: Meditsina, 2001. 640 p.
18. Sergienko V.I., Petrosyan E.A., Frauchi I.V. Topograficheskaya anatomiya i operativnaya khirurgiya: V 2 t. [Topographic Anatomy and Operative Surgery: In 2 volumes]. Moscow: GEOTAR-MED, 2001. Vol. 1. 832 p.
19. Sinel’nikov R.D., Sinel’nikov Ya.R. Atlas anatomii cheloveka: Ucheb. posobie. V 4 tomakh [Atlas of Human Anatomy: Textbook. allowance. In four volumes] Vol. 3. Moscow: Meditsina, 1996. 232 p.
20. Khofer M. Ul’trazvukovaya diagnostika. Bazovyy kurs. Per. s nem. [Ultrasound diagnosis. Basic Course. Transl. from German]. Moscow: Med. lit., 2013. 128 p.
21. Khofer M. Tsvetovaya dupleksnaya sonografiya. Prakticheskoe rukovodstvo [The color duplex sonography]. Moscow: Med. lit., 2007. 108 p.
22. Tukhbatullin M.G., Raimova R.F., Ziganshina L.F. Hemodynamic changes in the portal system in portal hypertension. Ekhografiya, 2002, vol. Z, no. 3, pp. 331 (in Russ.).
23. Akopyan N.E., Khachatryan G.G. Quantitative evaluation of complex diagnosis of diffuse liver disease. Radiologiya-praktika, 2009, no. 3, pp. 18-20 (in Russ.).
24. Shmidt G. Ul’trazvukovaya diagnostika. Prakticheskoe rukovodstvo [Ultrasound diagnosis. How]. Moscow: MEDpress-inform, 2009. 560 p.
25. Koda M., Murawaki Y., Kawasaki H. Renovascular resistance assessed by color Doppler ultrasonography in patients with chronic liver diseases. I Gastroenterol Hepatol., 2000, Dec., no. 15(12), pp. 1424-9.
26. Kuntsevich G.I., Belolopatko E.A., Sidorenko G.V. Assessment of portal blood flow in patients with liver cirrhosis according to duplex scanning. Vizualizatsiya v klinike, 1994, no. 5, pp. 33-39 (in Russ.).
27. Villar F., Goria O., Herve S. et al. Intrahepatic portocaval shunt: review of the literature, apropos of 1 case. Gastroenterol. Clin. Biol., 2000, May, 24 (5), pp. 582-584.
28. Martinoli C. et al. Doppler US of the hepatic veins. Europ. Radiology, 2000, vol. 15, pp. 349.
29. Olti Dzh., Khoui E. et al. Ul’trazvukovoe issledovanie. Illyustrirovannoe rukovodstvo [Ultrasonography. Illustrated Guide]. Moscow: GEOTAR-Media, 2010. 256 p.