Герпетическая экзема что это
Герпетиформная экзема Капоши
Герпетиформная экзема Капоши – это форма герпесвирусной инфекции, которая осложняет течение хронических заболеваний кожи ребенка. Основные клинические проявления – повышение температуры тела, увеличение лимфатических узлов, специфическая кожная сыпь, переходящая в кровоточащие эрозии. Диагностика базируется на сборе анамнестических данных, физикальном обследовании и результатах специфических лабораторных исследований – проба Тцанка, ИФА и ПЦР. Лечение включает в себя применение противовирусных препаратов, дезинтоксикационных средств, витаминов, иммуномодуляторов, проведение местной обработки кожи и симптоматической терапии.
Общие сведения
Герпетиформная экзема Капоши, или вариолиформный пустулез Юлиусберга – это осложнение хронических дерматозов у детей, спровоцированное вирусом простого герпеса. Зафиксированы случаи возникновения экземы у подростков и взрослых с иммунодефицитными состояниями. Заболевание впервые описано в 1887 г. венгерским дерматологом М. Капоши. В 1898 г. Юлиусберг описал схожую клинику, возникающую как при герпесвирусной инфекции, так и в ответ на вакцину от натуральной оспы. На данный момент доказано, что причиной в обоих случаях является вирус простого герпеса, а патологии объединены под одним названием – «герпетиформная экзема Капоши». Основная часть больных (95%) герпетиформной экземой Капоши – дети с атопическим дерматитом, реже – другими хроническими дерматозами. Отмечается сезонное обострение заболеваемости, возникающее поздней осенью, зимой и ранней весной.
Причины герпетиформной экземы Капоши
Основной возбудитель герпетиформной экземы Капоши – вирус простого герпеса (Herpes simplex). Чаще всего заболевание вызывает вирус типа А (typus 1), значительно реже – тип В (typus 2). Болеют дети в возрасте от 6 месяцев до 2 лет, пик заболеваемости – 7 месяцев-1,5 года. Это обусловлено тем, что до полугодовалого возраста ребенка защищают антитела к вирусу герпеса, полученные трансплацентарно в утробе матери. Собственные антитела начинают формироваться только с 2-3 лет. Герпетиформная экзема Капоши чаще возникает у детей с атопическим дерматитом, развившимся до 8 недель жизни. В группу риска входят младенцы, получающие глюкокортикостероиды или иммуносупрессивные препараты, а также находящиеся на искусственном вскармливании.
Источник заражения – инфицированный человек. Для детей это – родители, имеющие остаточные явления перенесенной инфекции на губах, коже лица и руках. Основные механизмы заражения – воздушно-капельный и контактно-бытовой. Наиболее частым путем считается непосредственная передача во время контакта с кожей, слизистыми оболочками или слюной носителя вируса. Вирус простого герпеса способен сохранять жизнеспособность на протяжении 10 часов при температуре 22-26°С, чем объясняется возможность реализации воздушно-капельного и бытового механизмов передачи.
Симптомы герпетиформной экземы Капоши
Инкубационный период герпетиформной экземы Капоши составляет от 1 до 10 дней, в среднем 4-5 суток. Возможно наличие продромального периода, который характеризуется возникновением общей слабости, сонливости и вялости ребенка. Его длительность составляет не более 3 суток. После этого периода резко возникают симптомы заболевания: значительное ухудшение общего состояния, гипертермия до 40°С, повышение ЧД и ЧСС, кожная сыпь. У всех детей наблюдается увеличение затылочных, подчелюстных и шейных лимфоузлов. При тяжелом течении развивается интоксикационный синдром, включающий в себя выраженную тахикардию и одышку, реже – судороги, истощение и гиперрефлексию. При легком варианте температура тела не поднимается выше 38°С, общее состояние практически не нарушено. Независимо от тяжести, гипертермия носит стабильный характер, дневные колебания температуры тела не превышают 1°С. Жаропонижающие средства малоэффективны.
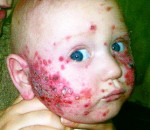
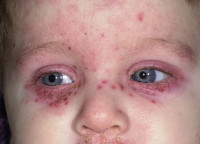
Одновременно с гипертермией возникают специфические кожные высыпания. Основные локализации сыпи: кожа лица, волосистая часть головы, кисти и предплечья. Реже поражаются стопы, ягодицы и туловище. На фоне тяжелых хронических дерматозов сыпь может приобретать генерализованный характер. Первично на фоне подъема температуры свыше 37,5°С возникает отечность и эритема кожи лица. Спустя 8-15 часов проявляются папулы, которые быстро трансформируются в везикулы и пустулы. Кожные элементы имеют округлую форму, выступают над уровнем прилегающих кожных покровов, в центре имеют углубление. Диаметр – от 1 до 4 мм. От окружающей кожи они отделены валиком воспаленного эпидермиса.
Высыпания, как правило, обильные, объединены в группы, редко распространенны диффузно. На коже лица сыпь сливается, формируя очаги, часто вызывает зуд. Во время развития кожных элементов происходит их спонтанное вскрытие. На месте везикул или пустул формируются эрозии, склонные к кровотечению и слиянию между собой. Образуются большие пораженные участки, которые покрываются темно-коричневой геморрагической коркой. Спустя 1-2 недели корки отпадают, температура тела нормализуется. Общая продолжительность заболевания – до 3-х недель. Рецидивы протекают в легкой форме, общее состояние не страдает.
При герпетиформной экземе Капоши у части больных возникает диарея с дегидратацией. Возможно развитие гнойного отита, гнойничковых заболеваний кожи, менингита, сепсиса. Группа риска – дети с тяжелым течением и/или возрастом до 12 месяцев. В редких случаях возникают смертельно опасные осложнения в виде сдавливания гортани вследствие отека тканей шеи, тяжелых аритмий, пневмоний, почечной и печеночной недостаточности. Летальность при таких осложнениях составляет порядка 15-45%.
Диагностика герпетиформной экземы Капоши
При герпетиформной экземе Капоши диагноз устанавливается на основе данных анамнеза, физикального обследования, результатов специфических и неспецифических лабораторных методов диагностики. Анамнестические данные могут указывать на недавно перенесенную герпесную инфекцию родителями или другими контактирующими с ребенком лицами, острое начало заболевания, наличие хронических дерматозов. При физикальном обследовании выявляется кожная сыпь и ее характерная локализация, увеличение лимфатических узлов, гепатомегалия, редко – спленомегалия. В ОАК определяется гипохромная анемия, лейкоцитоз или лейкопения, эозинопения. У 1/3 детей с герпетиформной экземой Капоши в ОАМ можно выявить протеинурию, лейкоциты.
Специфическая диагностика включает в себя пробу Тцанка, ПЦР и ИФА. Проба Тцанка позволяет установить наличие герпесвирусных включений в клетках из дна везикул или пустул. Методом ИФА можно зафиксировать увеличение титра IgM в сыворотке крови более чем в 4 раза. ПЦР определяет наличие ДНК вируса простого герпеса в организме ребенка. Дифференциальная диагностика герпетиформной экземы Капоши проводится с простым герпесом, опоясывающим лишаем, ветряной оспой, стафилококковым, стрептококковым импетиго и другими пиодермиями.
Лечение герпетиформной экземы Капоши
Герпетиформная экзема Капоши лечится сугубо в условиях детского инфекционного стационара под постоянным мониторингом педиатра. Для таких детей выделяется отдельная палата, т.к. они могут стать источником инфекции для других детей с дерматозами.
С первого дня госпитализации проводится этиотропное лечение противовирусными средствами. Препарат выбора – ацикловир. Также в/м вводится противогерпетический иммуноглобулин. В комплексе могут использоваться иммуномодуляторы. Показано применение витаминов группы В, А, С. С целью уменьшения зуда используются антигистаминные средства (клемастин, хлоропирамин). Для профилактики гнойничковых заболеваний назначаются антибактериальные средства – цефалоспорины II и III поколений (цефуроксим, цефтриаксон). При тяжелом состоянии ребенка проводится инфузионная терапия (5% раствор глюкозы, 0,9% раствор NaCl). При выраженных признаках интоксикации используют свежезамороженную плазму, 10% раствор альбумина. При развитии опасных для жизни ребенка аритмий показаны сердечные гликозиды (дигоксин).
Местное лечение герпетиформной экземы Капоши зависит от стадии развития кожных элементов. До вскрытия везикул и пустул их обрабатывают 1% спиртовым раствором бриллиантового зеленого и противогерпетическими мазями (5% ацикловир). На уже образовавшиеся корки наносится 3% дерматоловая или 2% борно-нафталановая мазь. Для ускорения процесса отхождения их накрывают марлевыми салфетками с цинковым маслом. С целью заживления кожи после полного отделения геморрагических корок используют кератопластические средства (салицилово-цинковая паста).
Прогноз и профилактика герпетиформной экземы Капоши
Прогноз тяжелой формы герпетиформной экземе Капоши сомнительный. Общая летальность составляет 10-30%. Без своевременного лечения исход неблагоприятный. При легкой форме или рецидиве прогноз благоприятный. Специфических мер по профилактике герпетиформной экземы Капоши не разработано. Неспецифическая профилактика заключается в изоляции людей, инфицированных вирусом герпеса, и предотвращении их контакта с ребенком, страдающим дерматозами на срок не менее 3-х недель.
Герпетическая экзема что это
Герпетическая экзема – это диссеминированная герпесвирусная инфекция, осложняющее течение хронических дерматозов с эрозивно-язвенными поражениями кожи у детей младшего возраста, реже – у подростков.
Развивается на фоне нарушения иммунитета. Источником заражения детей является больной простым герпесом, чаще всего это ближайший родственник (мама, папа и т.д.). Часто при осмотре можно заметить остаточные явления перенесенного простого герпеса у родственников на губах, крыльях носа, конъюнктиве глаз.
Путь передачи – воздушно-капельный или прямой контактный, то есть при соприкосновении с пораженной кожей, слизистой оболочки ротовой полости, слюной.
Герпетическая экзема осложняет течение хронических дерматозов в 90% случаев, эрозивно-язвенные поражения кожи развиваются у больных с атопическим дерматитом. Возбудителем герпетической инфекции является ДНК-содержащий вирус простого герпеса тип-1. По наблюдениям, герпетическая экзема чаще развивается у детей, у которых атопический дерматит возник в более ранние сроки – на 2-м месяце жизни, которые находились на искусственном вскармливании.
Заболеваемость герпетической экземой выше у детей от 6 мес. и до 2-х лет, у подростков и взрослых встречается редко. Это обусловлено резким падением внутриутробно переданных антител к вирусу простого герпеса к 6 мес. и появлению собственных антител к вирусу герпеса только к 2-3 годам.
Симптомы
Заболевание может начаться остро, возможно на фоне ОРВИ с повышением температуры тела и совпадает с периодом высыпаний, который длится в среднем от 7 до 10 дней. Наиболее частая локализация очагов поражений – это кожа лица, волосистая часть головы, шея, верхние конечности. Высыпания напоминают проявления ветряной оспы.
Лечение и профилактика
Детей, больных герпетической экземой, необходимо изолировать от других детей, при тяжелом течении – госпитализация. Детей грудного возраста продолжать кормить грудным молоком, а также принимать противовирусные и иммуностимулирующие препараты. Во избежание осложнений необходимо своевременно обратиться к врачу для проведения обследования и постановки правильного диагноза, чтобы уже на начальном этапе ребенок получил рациональное лечение.
В целях профилактики герпетической экземы нужно исключить контакт ребенка с детьми с атопическим дерматитом или другими дерматозами, с больными герпетической инфекцией. Помните – лучше заболевание предупредить, нежели его лечить.
Герпетическая экзема что это
Уральский научно-исследовательский институт дерматовенерологии и иммунопатологии Минздравсоцразвития России, Екатеринбург
ФГУ Уральский научно-исследовательский институт дерматовенерологии и иммунопатологии Минздравсоцразвития РФ, Екатеринбург
ФГБУ «Уральский НИИ дерматовенерологии и иммунопатологии» Минздрава России, Екатеринбург, Россия, 620076
ФГБУ «Уральский научно-исследовательский институт дерматовенерологии и иммунопатологии» Минздрава России, Екатеринбург, Россия, 620076
Герпес-вирусная инфекция в дерматологии: проблемы и современный подход к лечению
Журнал: Клиническая дерматология и венерология. 2015;14(5): 117-124
Кунгуров Н. В., Кохан М. М., Кениксфест Ю. В., Бакуров Е. В., Пазина М. В. Герпес-вирусная инфекция в дерматологии: проблемы и современный подход к лечению. Клиническая дерматология и венерология. 2015;14(5):117-124.
Kungurov N V, Kokhan M M, Keniksfest Iu V, Bakurov E V, Pazina M V. Herpes virus infection in dermatology: problems and modern approach to treatment. Klinicheskaya Dermatologiya i Venerologiya. 2015;14(5):117-124.
https://doi.org/10.17116/klinderma2015145117-124
Представлены современные данные литературы об особенностях клинических проявлений герпесвирусной инфекции в дерматологии: рецидивирующего фациального и лабиального герпеса, опоясывающего лишая, герпетической экземы, герпес-вирусассоциированной полиморфной экссудативной эритемы. Изложены основные принципы и схемы противовирусной терапии, представлен собственный опыт эффективной терапии заболеваний, вызванных вирусом простого герпеса, препаратом валацикловира (Валвир).
Уральский научно-исследовательский институт дерматовенерологии и иммунопатологии Минздравсоцразвития России, Екатеринбург
ФГУ Уральский научно-исследовательский институт дерматовенерологии и иммунопатологии Минздравсоцразвития РФ, Екатеринбург
ФГБУ «Уральский НИИ дерматовенерологии и иммунопатологии» Минздрава России, Екатеринбург, Россия, 620076
ФГБУ «Уральский научно-исследовательский институт дерматовенерологии и иммунопатологии» Минздрава России, Екатеринбург, Россия, 620076
В настоящее время герпес-вирусная инфекция (ГВИ) крайне широко распространена в человеческой популяции в связи с пантропностью вирусов и их высокой инвазивностью [1, 2]. Среди всех герпес-вирусов наиболее часто встречаются члены подсемейства Alphaherpesvirinae: вирус простого герпеса 1-го и 2-го типов (ВПГ-1 и ВПГ-2; Herpes simplex virus-1 и Herpes simplex virus-2), вызывающие фациальные (лабиальные, орофациальные) и генитальные поражения кожи и слизистых, а также вирус Varicella zoster (Human herpesvirus-3), являющийся этиологическим фактором ветряной оспы и опоясывающего лишая [2—4].
По данным ВОЗ, до 95% жителей планеты инфицированы ВПГ-1 и ВПГ-2, причем имеющиеся данные указывают на прогрессирующий рост заболеваемости в большинстве стран Европы и Америки, опережающий темпы прироста населения. Эпидемиологические и серологические исследования показывают, что распространенность инфицированности ВПГ-2 в мире достигает 400 млн человек, из них около 267 млн женщин и до 150 млн мужчин [3].
В прошлом существовало мнение об избирательном поражении ВПГ-1 исключительно области лица, а ВПГ-2 — наружных половых органов, однако в последние десятилетия были получены новые данные: ВПГ-1 вызывает оролабиальный герпес лица в 80—90% случаев, а ВПГ-2 — в 10—20%. Результаты проведенных исследований показали, что к 18 годам более 90% жителей городов инфицируются одним или несколькими штаммами вируса герпеса [1].
Пациенты с кожными проявлениями герпетической инфекции часто встречаются в практике дерматовенеролога, при этом основными нозологическими формами являются простой герпес кожи и слизистых, в том числе и с рецидивирующим течением; опоясывающий лишай, вызванный вирусом герпес зостер; реже — вирусные осложнения у больных атопическим дерматитом и другими дерматозами, именуемые герпетиформная экзема Капоши или варицеллеформный пустулез, острый оспенновидный пустулез Юлиусберга.
Рецидивирующие формы лабиального герпеса
Рецидивирующими формами герпеса страдают от 10 до 20% населения, а ежегодный прирост составляет 15—17%. По данным зарубежных исследований [5, 6], только у 20% инфицированных вирусом герпеса установлено это заболевание, у 60%, несмотря на явные симптомы, герпес остается нераспознанным, а у 20% лиц он протекает бессимптомно.
По данным S. Pierre и соавт. [6], рецидивирующий простой герпес (РПГ) встречается у 57,7% пациентов, инфицированных ВПГ в возрасте 14—49 лет. Большинство пациентов с РПГ имеют менее двух эпизодов в год, но у 5—10% больных высыпания рецидивируют более 6 раз в год. Частые рецидивы герпетических высыпаний на коже лица и шеи, боль, зуд, ознобы и слабость в продромальном периоде снижают качество жизни пациентов с РПГ. При проведении параллельного наблюдательного исследования у больных РПГ в США и Франции установлено, что при возникновении в течение года не более чем четырех эпизодов РПГ 67,0—68,0% больных отмечали снижение параметров качества жизни, а в подгруппах с более частым рецидивированием заболевания (6 раз год и более) такие изменения фиксировали уже 78,0—90,0% пациентов. Авторы [7] отмечают, что лечение по рекомендации врачей получают в США 63% пациентов с РПГ с обострениями более 6 раз в год, а во Франции — только 46,0%, остальные больные следуют советам фармацевтов или прибегают к самолечению.
Современные рекомендации по лечению РПГ с фациальной и лабиальной локализацией указывают на рациональность эпизодической терапии короткими курсами системными противовирусными препаратами и назначения пролонгированных курсов терапии (супрессивная терапия) при частоте рецидивов более 6 раз в течение 1 года [7, 8].
Герпетиформная экзема Капоши (варицеллеформный пустулез)
Герпетиформная экзема (ГЭ) — это диссеминированная ГВИ, вызванная ВПГ и осложняющая течение атопического дерматита (АтД) или экземы, а также буллезных хронических дерматозов, ожогов II—III степени тяжести, болезни Дарье, грибовидного микоза, синдрома Сезари [9, 10].
При ГЭ высыпания дебютируют в области кожи лица, но быстро диссеминируют, часто присоединяется пиодермия, нарушается общее состояние больных до среднетяжелого и тяжелого, развивается гипертермия, лимфаденопатия. ГЭ, как правило, возникает у пациентов с АтД в возрасте 10—30 лет преимущественно на фоне распространенного кожного процесса. Установлено, что ГЭ чаще развивается у больных, недостаточно активно и правильно лечившихся по поводу АтД. Пациенты с ГЭ чаще страдают рецидивирующими вторичными пиодермиями и контагиозным моллюском по сравнению с лицами, не имеющими экземы Капоши: 78% против 8% [11]. Показано, что у ГЭ-позитивных больных АтД наблюдаются более значимые изменения в системном иммунитете, значимо высокое содержание в сыворотке крови иммуноглобулина Е, более супрессированы антимикробные пептиды эпидермиса [9, 10, 12].
Герпес и полиморфная экссудативная эритема
Герпес у спортсменов
Герпетическая инфекция кожи — частая проблема у спортсменов, в особенности в тех видах спорта, где присутствует тесный телесный контакт: у борцов — «herpes gladiatorum», у игроков в регби — «herpes rugbiorum». Баскетболисты, футболисты, а также лыжники и конькобежцы, подвергающиеся воздействию низких температур и ультрафиолетового солнечного излучения, также составляют группу риска рецидивирующего лабиального герпеса [16]. ГВИ среди спортсменов занимает 4-е место по частоте встречаемости среди других заболеваний и составляет 47,0% от всех инфекционных поражений кожи, при этом локализация высыпаний в области лица и шеи составляет до 71,0—73,0%, на коже конечностей — 18—42%, в области туловища — 11,0—28,0% [17]. Течение ГВИ у спортсменов может быть рецидивирующим с легкой и умеренной тяжестью каждого эпизода, однако специалистами разработаны рекомендации по обязательному лечению заболевания с использованием системных противовирусных препаратов в различных режимах, в том числе для лечения эпизодов, а также профилактическое назначение противовирусных препаратов и длительная пролонгированная (супрессивная) терапия в течение всего соревновательного периода [18].
Опоясывающий герпес
Опоясывающий герпес (ОГ), или опоясывающий лишай — спорадическое заболевание, представляющее собой реактивацию латентной вирусной инфекции, вызванной вирусом герпеса 3-го типа, поражающее преимущественно кожный покров и нервную систему, в отдельных случаях — конъюнктиву и роговицу [19]. Заболеваемость О.Г. увеличивается среди лиц старших возрастных групп (после 60 лет), рецидивы заболевания возникают примерно у 5,0% переболевших, часто сопровождаются формированием постгерпетической нейропатии (ПГН). Риск возникновения ОГ увеличен у пациентов с хроническими заболеваниями, такими как ревматоидный артрит и другие аутоиммунные поражения, обструктивные заболевания легких, заболевания почек, сахарный диабет 1-го типа, лимфопролиферативные заболевания, причем сочетание нескольких факторов риска особенно значимы для пациентов более молодого возраста. Наиболее часто ОГ развивается у больных с онкопатологией, иммунокомпроментированных субъектов, инфицированных ВИЧ, пациентов, получающих системную иммунодепрессивную терапию [20]. Данные исследований показали, что среди дерматологических больных частота верификации ОГ (на 1000 пациенто-лет) составляет 8,03%, тогда как у больных раком и системной красной волчанкой — 11,7 и 15,2% соответственно. По данным S. Chen и соавт. [21], к числу контингента лиц с высоким риском развития ОГ относятся и больные псориазом, для которых характерны девиации клеточно-опосредованного и гуморального звеньев иммунитета, а также пациенты, использующие иммунодепрессивные и цитостатические препараты, фотохимиотерапию. Значимым является факт более частого развития ОГ у больных псориазом, получавших иммунодепрессивную терапию, с повышением показателя до 10,8%. Отмечено нарастание частоты ОГ у пациентов с псориазом в старшей возрастной группе и, как следствие, при увеличении длительности заболевания. Так, в группе больных псориазом старше 65 лет частота диагностирования ОГ достигает 15,4% [20—22]. В работе G. Shalom и соавт. [22] представлены результаты оценки риска развития ОГ у больных псориазом, получающих системную терапию. Авторы отмечают увеличение такого риска при сочетании генно-инженерных биологических препаратов с метотрексатом. Рекомендации по лечению ОГ у больных с другой патологией кожи однозначно указывают на необходимость проведения системной противовирусной терапии, с момента установления диагноза и желательно в первые 72 ч. Выбор противовирусного препарата и пути его введения, госпитальный или амбулаторный режим лечения, длительность терапии определяются клиническими особенностями процесса, тяжестью заболевания [23, 24].
Подходы к терапии герпес-вирусной инфекции кожи
В настоящее время для лечения больных ГВИ общепризнана необходимость противовирусной химиотерапии с использованием ациклических нуклеозидов — высокоспецифичных препаратов, обладающих доказанным противовирусным эффектом. В группу ациклических нуклеозидов входят ацикловир, валацикловир и фамцикловир. Первым из противовирусных препаратов был синтезирован ацикловир, модифицированный аналог компонента ДНК вируса. Для приобретения биологической активности в организме ацикловир проходит три этапа фосфорилирования, в результате которых образуется ацикловир-трифосфат, конкурентно подавляющий вирусную ДНК-полимеразу.
Однако недостатком ацикловира является низкая биодоступность и вытекающая отсюда необходимость многократного приема в течение суток — строго через каждые 4—5 ч. В поиске способов повышения биодоступности ацикловира был создан препарат валацикловир, представляющий собой L-валиновый эфир ацикловира. Валацикловир представляет собой «пролекарство», которое гидролизуется в кишечнике и печени под действием фермента валацикловир-гидролазы и освобождается от эфирной «надстройки», полностью (около 99%) превращаясь в ацикловир, который далее встраивается в полинуклеотидную цепочку ДНК вируса и блокирует дальнейшие удлинения молекулы ДНК. L-валиновый эфир повышает биодоступность препарата при приеме внутрь в 3,3—5,5 раза по сравнению с ацикловиром (биодоступность в зависимости от дозы составляет 50—70 и 15–30% соответственно) [25, 26]. Преимущество валацикловира в сравнении с ацикловиром заключается в том, что при оральном приеме первого достигаемые концентрации вещества в сыворотке крови и других внутренних средах эквивалентны таковым при внутривенном введении ацикловира. Это позволяет уменьшить количество приемов препарата до 2 раз в день при рецидиве и до 1 раза в день — при супрессивной терапии (курс пролонгированной терапии), а также определяет возможность однодневной терапии большими дозами [24, 26].
Для этиотропной терапии герпетической инфекции используют следующие схемы назначения валацикловира:
— терапию первичной герпетической инфекции, направленную на купирование острых проявлений и предотвращение распространения процесса;
— терапию рецидива (эпизодическая терапия), позволяющую предупреждать рецидивы инфекции и купировать уже возникшее обострение;
— терапию межрецидивную, эпизодическую супрессивную (пролонгированную) терапию, проводимую для предотвращения рецидива при воздействии известного и ожидаемого триггера обострения ГВИ;
— терапию межрецидивную, профилактическую супрессивную длительную, назначаемую при крайне частых рецидивах заболевания, эффективно снижающую частоту рецидивов и предотвращающую передачу ВПГ партнеру;
— однодневную терапию, обеспечивающую радикальное купирование проявлений лабиального герпеса в течение 1 сут.
В последние годы, после завершения 30-летнего срока действия патента валацикловира (препарат валтрекс), на мировом фармацевтическом рынке появилось более 30 генерических препаратов валацикловира (в России таких препаратов 11). Из числа фармацевтических средств, действующим началом которых является валацикловир, следует отметить препарат Валвир — аналог валацикловира (производство компании «Actavis», регистрационный №ЛП-001723 от 02.07.12).
Препарат Валвир, в отличие от оригинального валацикловира, выпускается в форме таблеток, покрытых пленочной кишечно-растворимой оболочкой, которая защищает действующее вещество от разрушения в кислой среде желудка. Валвир выпускается в дозировке 500 и 1000 мг, при этом новая дозировка в 1000 мг выпущена в 2014 г., и в настоящее время препарат Валвир в дозе 1000 мг — единственный на рынке.
Опыт лечения больных различными формами ГВИ кожи с использованием препарата Валвир (рис. 1, а, б; рис. 2, а, б; рис. 3, а, б; рис. 4, а, б).



В клинике ФГБУ «Уральский НИИ дерматовенерологии и иммунопатологии» Минздрава России обобщен опыт лечения больных различными формами ГВИ кожи с использованием препарата Валвир. Под нашим наблюдением находились 17 пациентов (12 женщин и 5 мужчин) в возрасте от 16 до 83 лет с ГВИ кожи, из них 7 больных — с рецидивирующим лабиальным, фациальным герпесом, 1 пациент — с первичным аффектом лабиального герпеса; 6 — с ОГ, 2 — с АтД и герпетиформной экземой Капоши и 1 пациентка с рецидивирующей полиморфной экссудативной эритемой.
Клинико-анамнестические данные о группе пациентов с ГВИ представлены в табл. 1.

Пациентам с РПГ (лабиальные, фациальные локализации) в случае умеренного количества рецидивов было назначено лечение препаратом Валвир в дозе 500 мг 2 раза в день в течение 5 дней, пациенту с выраженными первичными проявлениями герпеса (отек, гиперемия, везикулы на коже губы и в углах рта) была проведена однодневная экспресс-терапия в дозе 2000 мг, разделенные на 2 приема.
При ОГ пациентам назначали Валвир в дозе 1000 мг 3 раза в сутки в течение 7—14 дней, больным герпетиформной экземой — по 500 мг 2 раза в день в течение 7—10 дней. Лечение герпес-ассоциированной ПЭЭ проводили в режиме длительной супрессивной терапии по 500 мг в день в течение 4 мес. Все пациенты в процессе лечения и после его окончания находились под наблюдением, проходя ежемесячные клинические осмотры.
В табл. 2 представлены клинико-катамнестические данные результативности проведенной терапии.

Приведенные результаты мониторирования пациентов с различными формами ГВИ, получавшими терапию препаратом Валвир, свидетельствуют о его высокой клинической эффективности: отмечалось быстрое купирование остроты процесса и эпителизации вторичных эрозивных проявлений, значимое уменьшение субъективных симптомов, а также отсутствие ПГН, уменьшение частоты и тяжести последующих рецидивов.
Клинические наблюдения
Больная С., 60 лет, с диагнозом: рецидивирующий простой герпес (рис. 1). Больна в течение 3 лет, отмечает рецидивы ежемесячно. Методом ПЦР обнаружен ВПГ-1. Проведено лечение препаратом Валвир по 1000 мг в сутки в течение 5 дней. После курса лечения рецидивов в течение 6 мес не отмечали.

Больная В., 72 лет, с диагнозом: опоясывающий герпес (рис. 2). Больна более 6 мес: впервые высыпания появились после офтальмологической операции, сопровождались ярко выраженным болевым синдромом. После постановки диагноза пациентке было проведено лечение препаратом Фамвир в дозе 500 мг ежедневно в течение 21 дня. Женщина отмечала регулярное появление единичных пузырьков и выраженную болезненность. Больной был назначен 7-дневный курс лечения препаратом Валвир в суточной дозе 1000 мг. После терапии отмечен полный регресс высыпаний, отсутствие ПГН.
Больная Н., 69 лет, с диагнозом: опоясывающий герпес (рис. 3). Дебют заболевания произошел на фоне ОРВИ, отита правого уха (сохранялся субфебрилитет). Лечение препаратом Валвир (по 1000 мг 3 раза в день) было начато на 3-й день и продолжалось 7 дней.
Больная К., 58 лет, с диагнозом: опоясывающий герпес (см. рис. 4). Пациентка страдает хроническим лимфолейкозом. Лечение препаратом Валвир (по 1000 мг 3 раза в день) по поводу ОГ было начато на 7-й день от первых признаков заболевания и продолжено в течение 7 дней. Отрицательной динамики в общем состоянии и показателях гемограммы не отмечалось.
Заключение
Тяжелые и рецидивирующие формы ГВИ кожи распространены и часто встречаются в практике дерматолога.
Частые рецидивы заболевания значимо влияют на качество жизни пациентов, требуют обоснованной патогенетической противовирусной терапии.
Препарат валацикловир (Валвир) является особой транспортной формой ацикловира, содержит L-валин и лучше усваивается в желудочно-кишечном тракте, чем ацикловир.
Валацикловир (Валвир) блокирует размножение вируса, предотвращая появление новых герпетических высыпаний на коже.
Апробированы дифференцированные схемы терапии заболеваний кожи, вызванных ВПГ-1 и ВПГ-2 и Varicella zoster, препаратом валацикловира (Валвир), в том числе терапии в течение 1 дня. Собственные клинические наблюдения свидетельствуют о хорошей клинической эффективности и переносимости препарата Валвир в терапии различных форм герпес-вирусных инфекций.