Гестагенная активность что это
Ниша гестагенных контрацептивов: виды, названия и механизм действия
Марина Поздеева о формах и особенностях гестагенных контрацептивов
Все гестагенные контрацептивы показаны при кормлении грудью и непереносимости или противопоказаниях к эстрогенам.
ВМС с левоноргестрелом рекомендована для лечения меноррагии: менструальная кровопотеря через 6 месяцев уменьшается – на 71-95 %
После использования ДМПА фертильность восстанавливается достаточно медленно: 20 % женщин не овулируют в первый год после отмены
Мини-пили в первый год использования дают семипроцентную вероятность забеременнеть
Гестагенные контрацептивы нашли широкое применение благодаря хорошей переносимости
Гестагенные противозачаточные широко используются уже более 40 лет. Они имеют несколько форм выпуска: традиционные таблетки (мини-пили), пролонгированные растворы для инъекций (ДМПА), современные имплантаты и внутриматочные терапевтические системы, высвобождающие левоноргестрел. Действие прогестиновых препаратов заключается в ингибировании выброса лютеинизирующего (ЛГ) и фолликулостимулирующего гормона (ФСГ), подавлении овуляции, повышении вязкости и уменьшении объема цервикальной слизи, а также предотвращении роста эндометрия. Гестагенные контрацептивы нашли широкое применение благодаря хорошей переносимости, в том числе и ввиду отсутствия эстрогена, а также выраженного противозачаточного и терапевтического эффектов.
Гормональные имплантаты
Гормональный имплантат представляет собой гестагенсодержащий препарат в форме рентгеноконтрастного имплантата, помещенного в стерильный аппликатор. Имплантат не подвергается биологическому распаду и сохраняет эффективность на протяжении трех лет со дня введения. Гормональный имплантат вводят подкожно, на внутренней стороне плеча.
Преимущества
Длительность эффекта, быстрое восстановление фертильности после извлечения.
Недостатки
Сложности при введении и извлечении имплантата (при слишком глубоком или неправильном введении возможно повреждение нерва, кроме того, и введение, и выведение достаточно травматичны); побочные эффекты: нарушения менструального цикла, головные боли, изменения настроения, гирсутизм, галакторея, акне.
Инъекционный депонированный медроксипрогестерона ацетат (ДМПА)
ДМПА — это суспензия микрокристаллов синтетического прогестина для внутримышечного введения (обычно в ягодицу). Фармакологически активный уровень гормона достигается в течение 24 часов после введения, а концентрация медроксипрогестерона ацетата в сыворотке крови на уровне 1 нг/мл сохраняется в течение всего срока действия одной инъекции ДМПА (3 месяца). Через 7–9 месяцев после введения гормон не определяется в крови.
Разовая доза 150 мг подавляет овуляцию у большинства женщин на 14 недель, приводит к относительной гипоэстрогении.
Преимущества
Уменьшение выраженности дисменореи, снижение риска развития рака яичников и эндометрия, возможность применения для женщин, которым противопоказаны препараты эстрогенов. Безопасность для кормящих матерей.
Недостатки
Нарушение менструального цикла (у 50 % женщин в течение первого года использования возникает аменорея), персистирующие нерегулярные кровотечения, увеличение веса [2]. Возможно медленное восстановление фертильности вследствие длительного выведения из организма: около 70 % женщин беременеют в течение 12 месяцев после отмены ДМПА и почти 90 % — в течение 24 месяцев. Побочные эффекты (повышение массы тела, депрессия и нарушения менструального цикла) могут продолжаться в течение года после введения ДМПА. У 20 % женщин овуляция не возобновляется в течение 12 месяцев после применения препарата [3]. Кроме того, применение ДМПА ассоциируется с потерей плотности костной ткани, однако эти изменения обратимы после отмены препарата [4].
Из истории гестагенных контрацептивов
В середине 60‑х годов прошлого века уже было достоверно известно, что низкие дозы гестагенов могут предотвращать беременность. В 1967 году компания «Апджон» представила первый гестагенный контрацептив — гормональный противозачаточный препарат длительного действия ДМПА. Его ждала непростая судьба: на протяжении двух десятилетий периодически «всплывала» информация о возможном канцерогенном действии. И хотя предположения о повышении риска развития рака на фоне приема опровергались в клинических испытаниях, в США ДМПА долгое время оставался вне закона.
Только в 1992 году, когда контрацептив покорил 90 стран мира, Американское управление по контролю за качеством лекарств FDA одобрило заявку на его регистрацию в США.
В то время как в лабораториях «Апджон» создавался инъекционный противозачаточный гестаген, мексиканец Джош Мартинез-Манатоу изучал противозачаточную активность перорального низкодозированного гестагена хлормадинона ацетата. В 1966 году он опубликовал работу, доказывающую эффективность приема per os хлормадинона ацетата в качестве контрацептива. Однако первый мини-пили был зарегистрирован FDA только в 1972 году. Им стал препарат, содержащий 0,35 мг норэтистерона. Уже через год появился низкодозированный препарат, в состав которого входил норгестрел в дозировке 0,075 мг.
Следующей новинкой в ряду гестагенных контрацептивов оказалась ВМС. Мало кто знает, что прототипом современной системы с левоноргестрелом была ВМС, высвобождающая прогестерон. Препарат под названием «Прогестасерт» предложил финский врач Джоуни Валтери Тапани в 1976 году. Основанием для его разработки стали исследования американца Антонио Скомменга, открывшего, что внутриматочное введение прогестерона оказывает противозачаточный эффект. Срок жизни этого препарата оказался недолгим — через год после выхода на рынок Прогестасерт исчез с рынка. Замена ему появится лишь в 2000 году, когда FDA зарегистрирует ВМС с левоноргестрелом.
В 1983 году в аптеках Финляндии впервые в мире начал продаваться имплантат с левоноргестрелом — «Норплант».
После подкожного введения имплантат сохранял эффективность на протяжении пяти лет. Производство «Норпланта» было остановлено только в 2008 году.
Внутриматочная терапевтическая система
Препарат представляет собой ВМС, которая высвобождает левоноргестрел в дозировке 20 мкг в сутки. Гестаген обнаруживается в крови уже через час после установки ВМС, а максимальная концентрация достигается через 2 недели. Длительность действия — 5 лет со дня установки.
Индекс Перля внутриматочной терапевтической системы составляет 0–0,2.
Преимущества
FDA рекомендует применять ВМС с левоноргестрелом для лечения меноррагии: менструальная кровопотеря на фоне применения препарата через 3 месяца уменьшается на 62–94 %, а через 6 — на 71–95 %. После удаления системы фертильность быстро восстанавливается: 89 из 100 женщин в возрасте до 30 лет беременеют в течение 1 года [5].
Недостатки
Побочные эффекты: головная боль, боль в животе, мажущие кровянистые выделения, олигоменорея, аменорея, вульвовагинит.
Противопоказания
К противопоказаниям, общим для всех гестагенсодержащих ГК, присоединяются еще несколько заболеваний: ВЗОМТ, цервицит, дисплазия шейки матки, аномалии матки (в том числе фибромиомы, деформирующие полость матки), а также состояние после септического аборта в течение последних 3 месяцев.
Пероральные гестагены (мини-пили)
Гестагенные оральные контрацептивы подавляют овуляцию (в разных циклах неравномерно), блокируют выработку ФСГ и ЛГ, увеличивают вязкость шеечной слизи; сокращают число и размер желез эндометрия, что приводит к его атрофии; уменьшают подвижность ресничек в маточных трубах, замедляя скорость передвижения яйцеклетки (с последним связан повышенный риск внематочной беременности).
Максимальный уровень прогестина в сыворотке достигается через два часа после приема препарата. В течение суток действующее вещество полностью метаболизируется.
Наибольшая эффективность мини-пили достигается при регулярном применении. Вероятность наступления беременности в течение первого года использования может достигать 7 %.
Преимущества
Отсутствие побочных эффектов, свойственных препаратам эстрогена; эффективность при дисменорее, снижение менструальной кровопотери, уменьшение выраженности предменструального синдрома (ПМС), возможность быстрого восстановления фертильности после отмены.
Недостатки
Существенная зависимость эффекта от комплаентности: пропуск или поздний прием очередной таблетки значительно снижает эффективность. Если временной разрыв между приемом таблеток составляет 27 часов или больше, необходимо использовать дополнительные меры контрацепции. Возможны межменструальные кровотечения, кровянистые выделения, аменорея, головная боль, чувствительность груди.
Все гестагенные контрацептивы показаны при кормлении грудью и непереносимости или противопоказаниях к эстрогенам. Они могут применяться уже через шесть недель после родов у кормящих матерей и сразу после родов у тех пациенток, которые не кормят грудью. Прогестиновые контрацептивы не снижают лактации и не влияют на развитие ребенка.
Нашли ошибку? Выделите текст и нажмите Ctrl+Enter.
Роль гестагенов в клинико-фармакологических эффектах гормональных контрацептивов
*Пятилетний импакт фактор РИНЦ за 2020 г.
Читайте в новом номере
Российский государственный медицинский факультет МЗ РФ
В настоящее время врачами-гинекологами общепризнаны достоинства метода гормональной контрацепции для планирования семьи и улучшения здоровья женщины, продолжаются исследования механизмов действия гормональных контрацептивов и внедрение новых препаратов, создаваемых как путем синтеза новых гормональных соединений, так и с помощью поиска новых комбинаций и дозировок уже известных гестагенов и эстрогенов. [11, 13].
Разработка первых гормональных контрацептивов началась в Германии, в 50-х годах на основании имевшихся в то время сведений о подавлении овуляции во время беременности и о том, что данный эффект обусловлен прогестероном. В 1952 году были получены синтетические гестагены и в конце пятидесятых годов начались клинические испытания этих препаратов в аспекте их способности ингибировать овуляцию и предотвращать беременность. Все современные гормональные контрацептивы можно разделить на чисто гестагенные и комбинированные гестаген-эстрогенные препараты. Комбинированные оральные контрацептивы (КОК) более надежны, лучше контролируют менструальный цикл по сравнению с гестагенными препаратами и поэтому применяются чаще.
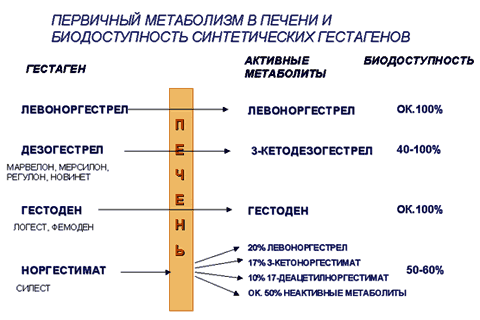
Рис.1 Первичный метаболизм в печени и биодоступность синтетических гестагенов
Существует большое количество исследований in vitro связывания гестагенов с различными стероидными рецепторами [15, 29]. В работе U. Fuhrmann, E. Slater [15] показано, что гестоден и 3-кетодезогестрел могут связываться с андрогенными рецепторами простаты и глюкокортикоидными рецепторам тимуса сильнее, чем прогестерон (табл. 3). Гестоден и 3-кето-дезогестрел отличаются в отношении тропности к минералокортикоидным рецепторам; в этом случае гестоден имеет сходство с прогестероном. Но, как уже отмечалось, сам по себе факт связывания еще не говорит о том, будут ли рецепторы активированы или ингибированы. О результате взаимодействия гормона с рецептором можно судить, оценивая индукцию транскрипции ДНК, зависящую от данного рецептора. Показано, что по способности инициировать транскрипцию в результате связывания с андрогенными рецепторами гестагены расположились в порядке убывания следующим образом: 3-кетодезогестрел > гестоден > прогестерон (заметим, что, именно эти данные лучше отражают андрогенную активность стероидов, в отличие от данных по связыванию с рецепторами). При оценке андрогенной активности гестагенов в целом организме (мыши) не найдено различий между гестоденом и дезогестрелом в их способности стимулировать активность андрогензависимого фермента [8]. Хотя сами по себе дезогестрел и гестоден имеют небольшую остаточную адрогенную активность, их комбинация с этинилэстрадиолом в составе КОК in vivo характеризуется выраженным антиандрогенным действием. Это связано с тем, что КОК подавляют выработку ЛГ, стимулирующего синтез андрогенов в яичниках, и этинилэстрадиол стимулирует синтез в печени транспортного белка крови, переносящего половые стероиды (ГСПС). Это приводит к уменьшению свободной фракции андрогенов в крови. По разным данным, КОК, содержащие 20-30 мкг этинилэстрадиола, вызывают увеличение содержания ГСПС в крови примерно в 1,5-3 раза. Значимых различий увеличения ГСПС при приеме КОК с разными гестагенами нет [20, 26].
Рассматривая другие свойства современных гестагенов, следует отметить, что гестоден и 3-кето-дезогестрел примерно одинаково активируют рецепторы глюкокортикоидов человека. Несмотря на заметное сродство 3-кето-дезогестрела и гестодена к глюкокортикоидным рецепторам, их глюкокортикоидная активность in vivо, определяемая по инволюции тимуса у крыс, была пренебрежимо мала (в 3000 раз слабее дексаметазона). Подобно прогестерону, гестоден ингибирует индукцию альдостероном транскрипции в клетках COS-1, содержащих минералокортикоидные рецепторы человека, а 3-кето-дезогестрел в этом отношении неактивен [15]. При этом сам гестоден не активирует минералокортикоидные рецепторы. В сродстве 3-кетодезогестрела и гестодена к гестагенным рецепторам человека, кроликов и грызунов существуют видовые различия. Таким образом, приведенные данные свидетельствуют о наибольшем сходстве фармакологических свойств гестодена из исследуемых синтетических гестагенов производных 19-нортестостерона с прогестероном. Наличие у гестодена антиминералокортикоидного действия может объяснить меньшую частоту возникновения таких побочных эффектов, как напряжение молочных желез, головные боли, по сравнению с дезогестрелсодержащими контрацептивами [18].
В клинике современный контрацептив должен обеспечивать высокую контрацептивную надежность, хороший контроль менструального цикла, быть хорошо переносимым и безопасным при длительном применении. Безопасность и высокая эффективность гестоденсодержащих препаратов была доказана в многочисленных доклинических и клинических испытаниях [6, 7, 9, 17, 25, 26, 28]. Важно подчеркнуть, что снижение дозы этинилэстрадиола до 20 мкг в комбинации с гестоденом не снижает контрацептивной надежности [11]. Благодаря 100% биодоступности гестоден имеет стабильную фармакокинетическую кривую, что обеспечивает хороший контроль менструального цикла даже в комбинации с низкой дозой эстрогена. В клинических исследованиях показана низкая частота «мажущих» и «прорывных» межменструальных кровянистых выделений при назначении препарата, содержащего 20 мкг этинилэстрадиола в комбинации с 75 мкг гестодена.
В клинических исследованиях показано, что гестоденсодержащие контрацептивы не оказывают клинически значимого влияния на метаболизм липидов, углеводов и систему гемостаза, имеют мало побочных эффектов и хорошо переносятся при длительном применении [10, 12, 13, 16, 26].
Гормональная контрацепция. Часть II. Механизм действия
Поделиться:
Выбрать подходящий конкретной пациентке препарат бывает очень непросто. Простого пути — посмотреть, чего не хватает, и досыпать — не существует, поэтому придется разбираться, чем и куда мы внедряемся, чтобы обеспечить не только эффективную контрацепцию, но и хорошую переносимость.
Даже неудачно подобранная гормональная контрацепция при регулярном применении обеспечит пациентке надежную, почти абсолютную защиту от нежелательной беременности, поэтому индивидуальный подбор ведется ради единственной цели — минимизировать побочные эффекты и получить неконтрацептивные преимущества.
Принцип действия и возможности КОК
Комбинированные оральные контрацептивы называют комбинированными, потому что они содержат два компонента — эстрогенный и гестагенный. Основная задача комбинации — предотвратить овуляцию и обеспечить хороший контроль цикла.
С эстрогенами в составе КОК все просто. Подавляющее большинство КОК содержат один и тот же эстрогенный компонент — ЭЭ (этинилэстрадиол). Он входит в состав контрацептивных таблеток вот уже 50 лет и обеспечивает подавление овуляции. В самом начале эры контрацепции таблетки содержали огромные дозы эстрогенов, которые удалось постепенно снизить и довести до минимальных.
Сегодня мы выделяем три группы КОК в зависимости от содержания ЭЭ:
Высокодозные КОКи ушли в историю и больше не применяются. Среднедозные препараты назначаются по строгим лечебным показаниям или в случаях, когда не удается обеспечить хороший контроль, используя меньшие дозировки эстрогенов.
Микронизированные КОК врачи традиционно рекомендуют юным девушкам. В возрасте 25+ лучше подойдут препараты с 30 мкг ЭЭ.
Не так давно на наш рынок вышло два препарата с эстрогенами, идентичными природным, — Клайра и Зоэли. Клайра содержит эстрадиола валерат, а Зоэли — эстрадиола гемигидрат. Такие препараты значительно снижают риск развития эстрогенных осложнений и побочных эффектов. «Натуральные» эстрогены особенно хороши у старшей возрастной группы пользовательниц.
С гестагенным компонентом сложнее. Гестагены в составе КОК делают вид, что работают прогестероном, только вместо подготовки эндометрия к беременности контролируют его рост и трансформацию. Работают они, соединяясь с рецепторами, с которыми мог бы взаимодействовать прогестерон.
Именно от гестагенного компонета зависит — появятся прыщи или, наоборот, исчезнут, ухудшится настроение или улучшится, исчезнут боли в дни менструации или останутся, уменьшится объем менструальных кровотечений или останется прежним.
Если мы выбираем гестаген с антиандрогенной активностью (ципротерона ацетат в составе Диане-35, дроспиренон в составе Джес, диеногест в составе Жанин), то вправе рассчитывать, что у пациентки улучшится состояние кожи и волос, уйдут прыщи. Если выбираем препарат с антиминералокортикоидным эффектом (дроспиренон в составе Джес и Ярины), то надеемся, что не будет задержки жидкости, а значит, не будут появляться отеки, нагрубать молочные железы, болеть голова и беспокоить ПМС.
Некоторые гестагены, входящие в состав КОК, сохраняют андрогенную активность. С этой проблемой исследователи столкнулись еще в 1970–1980-е годы, когда женщины массово начали жаловаться на появление прыщей, жирность кожи и волос, увеличение массы тела. В мире современной контрацепции не осталось препаратов, в состав которых входят такие «жесткие» вещества. Гестоден и дезогестрел обладают остаточной андрогенной активностью, но в большинстве случаев она не имеет клинического значения.
Существуют специальные таблицы в помощь гинекологам для уточнения эффектов того или иного препарата.
Активность стероидных рецепторов отдельных прогестинов *
прогестагенная
андрогенная
антиандрогенная
антиминералкортикоидная
глюкокортикоидная
Увы, для индивидуального подбора контрацептивной комбинации недостаточно просто держать табличку перед глазами. Не всегда совпадает то, что ученые получили в эксперименте, с тем, что будет происходить в организме конкретной пациентки.
Можно ли подобрать КОК «по внешности»?
Попытки систематизировать методику подбора КОК по фенотипу предпринимались и предпринимаются. Идея звучит очень заманчиво. Грудь большая и пышная — значит, эстрогенов много. Бюстом «пошла в папу» — значит, эстрогенов маловато. Вот, казалось бы, уже и решили, какой препарат назначить.
Выделены различные фенотипы у женщин — с преобладанием эстрогенного, андрогенного или прогестеронового компонента. В зависимости от того, к какому типу принадлежит пациентка, предлагают подбирать стартовую дозировку эстрогенов и оптимальный гестаген.
Возможно, это имеет какой-то смысл ( хотя серьезных доказательных данных такая точка зрения не имеет: все работы проводились на сравнительно небольших группах пациенток). Но гораздо важнее для практического врача — понимать, чтó именно содержит конкретный препарат и зачем это содержимое конкретной пациентке.
Именно поэтому у нас много врачей, предпочитающих назначать одни и те же 2-3 препарата. Они их достаточно изучили, уверены в своих знаниях и накопили приличный опыт собственных наблюдений.
Подбор препарата, исходя из индивидуальных проблем
Беседуя с пациенткой и проводя осмотр, доктор «цепляет» мелкие детали, проблемы, особенности, которые можно устранить, сгладить или нивелировать использованием конкретного препарата.
Важно понять, что речь здесь не идет о недостаточной квалификации вашего гинеколога и, конечно, никто не ставит на вас эксперименты. В любом случае врач старается как можно скорее найти оптимальный вариант контрацепции. И с большой вероятностью его поиск увенчается успехом.
Товары по теме: [product](Клайра), [product](Зоэли), [product](Ярина), [product](Джес), [product](Диане-35), [product](Жанин), [product](Марвелон), [product](Фемоден), [product](Белара), [product](Мерсилон), [product](Логест)
Гестагенная активность что это
Согласно современным представлениям, к гестагенам (лат. gesto – носить, быть беременной + греч. genes – порождающий, производящий) относят группу природных гормонов и их синтетических аналогов, обладающих биологической активностью прогестерона. История открытия гестагенов включает проведенные более ста лет назад эксперименты по удалению или деструкции яичников, приводившие к атрофии матки, прерыванию беременности или потере половых функций у животных, а также по их восстановлению с помощью трансплантации яичников или введения их экстрактов. G.W. Corner и W.M. Allen (1929) выделили из желтого тела яичников млекопитающих стероид, названный прогестероном, благодаря которому реализуется физиологическая регуляция функции матки. В последующем было синтезировано большое число его аналогов и изучена их способность влиять на матку, яичники и молочные железы, а также на другие органы и системы. В процессе изучения механизмов действия гестагенов (прогестинов) были получены данные о характере их влияния на созревание и выход яйцеклетки, имплантацию оплодотворенной яйцеклетки, поддержание и сохранение беременности, развитие лобулярно-альвеолярного аппарата молочной железы, на центральную регуляцию секреции гонадотропинов и полового поведения. На основании этих исследований были разработаны различные гестагенные препараты, предназначенные не только для гормонозаместительной терапии (ГЗТ) при дефиците эндогенного прогестерона, но и лечения нарушений менструального цикла, дисменореи, меноррагии, гормонозависимых опухолей, а также предупреждения нежелательной беременности [1,3,55].
Прогестерон – естественный стероидный гормон желтого тела, плаценты и коры надпочечников. В период половой зрелости при нормальной функции яичников прогестерон поступает в организм женщины во второй фазе менстурального цикла (яичниковый цикл), когда после овуляции формируется желтое тело. По мере нарастания функциональной активности желтого тела выработка им прогестерона увеличивается, а к концу менструального цикла, в связи с обратным развитием желтого тела, снижается. Это способствует периодическому отторжению слизистой оболочки матки (эндометрий). Наступление беременности, сопровождающееся сохранением функциональной активности желтого тела, характеризуется постепенно повышающейся выработкой прогестерона. Начиная с 4 месяца беременности, местом образования прогестерона становится плацента, из которой он поступает в организм женщины в возрастающих количествах, и лишь незадолго до родов высвобождение его снижается.
Прогестерон выполняет в организме следующие функции:
Основное физиологическое действие прогестерона в женском организме проявляется только в половозрелом возрасте. Он обеспечивает сохранение беременности (нарушает переход возбуждения от одного мышечного волокна к другому и тормозит сократительную активность матки), создает необходимые условия для развития плодного яйца, стимулирует развитие концевых элементов молочных желез.
При избыточном количестве эстрогенов прогестерон уменьшает чувствительность матки к ацетилхолину, адреналину, эстрогенам, усиливает трофические процессы в маточных трубах, стимулирует рост и развитие железистой ткани молочных желез, способствуют подготовке их к лактации в послеродовом периоде.
В разные периоды жизни женщины прогестерон оказывает неодинаковое действие на репродуктивную систему, поскольку количество гестагенных рецепторов зависит от уровня эстрогенов, который также подвержен возрастным колебаниям. Недостаток прогестерона в организме является одной из частых причин бесплодия, нарушения менструального цикла и спонтанного прерывания беременности.
Номенклатура и классификация гестагенов
В 1996 г., в Германии, на европейской конференции, посвященной гестагенам, была принята классификация и номенклатура гестагенов, утверждены основные показания к их клиническому использованию, а также дано их определение [42]. Согласно этому определению к гестагенам (прогестинам) относятся вещества, которые подобно прогестерону способны трансформировать эндометрий, подвергнутый воздействию эстрогенов, в секреторное состояние (тест Клауберга). Все химические соединения, которые соответствуют этому определению, имеют стероидную структуру. Они сходны по своему действию на эндометрий, но отличаются между собой по действию на другие органы-мишени и различные метаболические процессы.
Все гестагены на основании их химической структуры разделяют на следующие группы:
(A) Прогестерон и его производные
(1) Медрогестон
(В) Ретропрогестины
(2) Дидрогестерон
(С) Производные 17альфа-гидроксипрогестерона
(3) Гидроксипрогестерона капроат
(4) Медроксипрогестерона 17-ацетат
(5) Ингестрола ацетат
(6) Хлормадинона ацетат
(7) Ципротерона ацетат
(D) Производные норпрогестерона
(8) Демегестон
(9) Промегестон
(10) Тримегестон
(Е) Производные 17альфа-гидроксинорпрогестерона
(11) Гестенорона капроат
(12) Номегестрола ацетат
Производные андростана и эстрана
(F) Производные тестостерон
(13) Этистерон
(H) Производные 19-нортестостерона
(14) Норэтистерон (или норэтинодрон)
(15) Основное пролекарство норэтестрона – норэтистерона ацетат
(16) Линестренол
(17) Этинодиола диацетат
(18) Норэтинодрел
(19) Тиболон
(20) Квингестранола ацетат
(21) Левоноргестрел
(22) Гестоден
(23) Дезогестрел
(24) Норгестимат
(25) Диеногест
(26) Норгестринон
(27) Гестринон
В последующие годы были получены новые стероиды с гестагенной активностью, часть из которых проходит доклинические или клинические испытания, а некоторые уже внедрены в практику. В частности появилась еще одна группа гестагенов:
(H) Производные спиронолактона
(28) Дроспиренон
Новые оригинальные отечественные гестагены – мецигестон и бутагест – следует отнести, исходя из их химического строения, к производным циклогексанпрогестерона и прогестерона соответственно.
Молекулярные механизмы действия гестагенов
В организме гестагены взаимодействуют с целым рядом органов-мишеней и метаболических систем, чувствительных к их воздействию, к числу которых относятся:
На клеточном уровне механизм действия гестагенов, как и других стероидных гормонов, включает несколько этапов. На первом из них в области плазматической мембраны компетентных клеток происходит специфическое узнавание и передача сигнала к мембранным ферментам и каналам [2].
Для реализации своей специфической активности все гестагены должны взаимодействовать с гестагенными рецепторами [6]. Для этого обязательным является присутствие С3-кето-группы и двойной связи между С4 и С5 углеродными атомами кольца А. В клетках тканей-мишеней имеются участки связывания на плазматической мембране и внутри клетки (цитозоль/ядро), которые опосредуют быстрые (миллисекунды) и медленные (около часа) специфические биологические эффекты гестагенов. Следует отметить, что все гестагены оказывают даун-регулирующее действие на эстрогенные рецепторы в тканях-мишенях и стимулируют метаболизм эстрадиола.
Для прогестерона обнаружены две изоформы внутриклеточных рецепторов [2]. У человека А-рецепторы отличаются от В-рецепторов отсутствием N-концевого участка, состоящего из 164 аминокислотных остатков. Если изоформы А и В присутствуют в эквимолярных соотношениях, может происходить их димеризация с образованием гомодимеров А/А, В/В и гетеродимеров А/В. Функция В-рецепторов состоит в активации специфических прогестерон-стимулируемых генов. А-рецепторы могут ингибировать активность В-рецепторов, причем не только прогестероновых, но и других стероидных гормонов, в частности, рецепторов эстрогенов, андрогенов, глюко- и минералокортикоидов [11]. Соотношение А- и В-рецепторов в тканях-мишенях определяет характер ответа при воздействии прогестерона и может объяснять вариабельность эффектов гестагенов.
Экспрессия гестагенных рецепторов имеет место в эндометрии, миометрии, гранулезных клетках и желтом теле яичника, в матке самок и семенниках самцов. Кроме того, гестагенные рецепторы найдены в ткани молочной железы (в норме и при опухолевом росте), в головном мозге (гипофиз, гипоталамус – преоптическая и вентромедиальная области), сосудистом эндотелии, тимусе, легких, островках поджелудочной железы, остеобластах [18,51].
Экспрессия гестагенных рецепторов повышается в присутствии эстрогенов и уменьшается в присутствии гестагенов. В период преэструса или после введения экзогенного эстрадиола количество гестагенных рецепторов увеличивается, а во вторую половину менструального цикла, когда повышается уровень прогестерона в сыворотке, число гестагенных рецепторов уменьшается. Прогестерон противодействует индукции гестагенных рецепторов эстрогенами. Разные клетки неодинаково чувствительны к регулирующему воздействию эстрогенов и прогестерона. Во время фолликулярной фазы цикла высокий уровень гестагенных рецепторов зарегистрирован в ядрах клеток эпителия и стромы эндометрия, в гладкомышечных клетках миометрия. В средней и поздней стадиях лютеальной фазы происходит снижение числа гестагенных рецепторов в люминальном и гландулярном эпителии. В клетках стромы и миометрия, несмотря на высокое содержание прогестерона в крови и отсутствие эстрогенных рецепторов, имеет место низкое содержание рецепторов гестагенов. В отличие от матки, уровень гестагенных рецепторов в молочной железе одинаков в фолликулярную и лютеальную фазы менструального цикла.
В результате активации специфических генов прогестерон-рецепторным комплексом происходит стимуляция гликогенеза, метаболизма циклических нуклеотидов, повышение уровня простагландинов, пролактина, активатора плазминогена, а также биосинтеза ферментов, метаболизующих эстрогены, альфа-фукозидазы, цАМФ-зависимой киназы типа II, гидролазы и фосфатазы [18,43]. В регуляции овуляции прогестероном принимает участие релаксин, который, в свою очередь, стимулирует секрецию коллагеназы, протеогликазы, бета-глюкоронидазы и активатора плазминогена. Прогестерон облегчает имплантацию яйцеклетки, стимулируя синтез ферментов, ответственных за лизис зоны пеллюцида (блестящая оболочка яйцеклетки). Индукция прогестероном пролиферации клеток матки при беременности опосредована стимуляцией секреции факторов роста и повышением синтеза рецепторов к этим факторам. Кроме того, прогестерон стимулирует в матке синтез утероглобина, который принимает участие в связывании и транспорте прогестерона и его основного метаболита 5-альфа-прегна-3,20-диона, защищающего бластоцист от большого количества прогестерона. Полагают, что утероглобин, ингибируя фосфолипазу А2, играет важную роль в защите эмбриона от иммунных воздействий и воспалительных реакций. Прогестерон подавляет сокращение матки вследствие регулирующего влияния на внутриклеточную концентрацию кальция (ингибирование экспрессии калиевого транспортера кальбиндина-Д9к), снижения уровня простагландинов (индукция синтеза простагландин-15-дегидрогеназы) и числа рецепторов окситоцина, индукции выработки релаксина. Увеличение прогестероном транскрипции бета-адренорецепторов в миометрии при беременности способствует снижению тонуса матки. Поэтому при угрозе преждевременных родов назначают бета2-адреномиметики (гексопреналин, сальбутамол или тербуталин).
В той или иной степени гестагены могут взаимодействовать с рецепторами других стероидных гормонов (андрогенными, глюко- и минералокортикоидными и, в ряде случаев, даже эстрогенными) и физиологически активных веществ (например, ГАМК, глициновых рецепторов), формируя в каждом случае индивидуальный профиль фармакологической активности. Данные о сродстве гестагенов к рецепторам других стероидных гормонов представлены в таблице 1.
Само по себе сродство гормона к рецептору не позволяет судить о характере фармакологического эффекта, так как стероид может быть его агонистом или антагонистом. Кроме того, иногда стероид выступает в качестве частичного агониста или антагониста. Поэтому, имея данные только о сродстве того или иного гормона к определенному рецептору, нельзя говорить о характере его биологической активности in vivo. Об этом можно судить с помощью специальных тестов, результаты которых в обобщенном виде представлены в таблице 2.
Величина того или иного эффекта гестагена определяется не только характером взаимодействия гормона с соответствующим рецептором, но и его фармакокинетикой. Кроме того, поскольку гестагены применяют при ГЗТ и контрацепции совместно с эстрогенами, важно оценивать действие препарата в совокупности, учитывая, что гестагенный и эстрогенный компоненты влияют на активность друг друга. Для ГЗТ особое значение имеет наличие у гестагена частичного андрогенного эффекта, который может противодействовать положительному влиянию эстрогенов на обмен липидов. Особого внимания с этой точки зрения заслуживает диеногест – единственное производное 19-нортестостерона с клинически выраженными антиандрогенными свойствами
Показания к использованию гестагенов
После открытия прогестерона, начиная с 30-х гг. прошлого века, гестагены (прогестины) начали широкого применяться в медицинской практике, и за прошедшие годы показания к их применению значительно расширились (табл. 3.), учитывал новые данные о механизмах действия стероидных гормонов.
Компенсация недостаточности желтого тела
Первичное показание к использованию гестагенов – восполнение дефицита эндогенного прогестерона при недостаточности желтого тела, которая может иметь место как до, так и после середины жизни женщины (первая и вторая фазы).
Первая фаза включает период после менархе до 35-40 лет, когда наблюдается доминирование эстрогенов. При относительном превышении уровня эстрогенов по отношению к прогестерону наблюдаются нарушение менструального цикла, предменструальный синдром (включает чувство переполнения молочных желез и мастодинию), развитие миом и мастопатии. Во всех этих случаях гестагены назначают ежедневно в течение 10-14 дней во вторую половину цикла до тех пор, пока перечисленные симптомы не исчезнут. Если наблюдается аменорея, то прогестиновый тест – наилучший способ выяснения ее причины. Женщинам с синдромом поликистозных яичников назначают гестагены без андрогенной активности (препарат выбора – ципротерона ацетат). В случае недостаточности эндогенных гестагенов для имплантации яйцеклетки, для обеспечения нормальной беременности применение гестагенных препаратов является необходимым, но схемы их использования требуют уточнения с учетом синтеза и метаболизма прогестерона у каждой пациентки.
Во вторую фазу жизни, начинающуюся в 45-48 лет, недостаточность желтого тела обычно сопровождается гипоэстрогенемией. В связи с этим в течение 20-21 дня каждого цикла следует принимать дозу гестагена, достаточную для антигонадотропного эффекта, в сочетании с природным эстрогеном, так как этинилэстрадиол может оказывать нежелательное действие на сердечно-сосудистую систему.
Для ГЗТ чаще всего используют производные 17альфа-гидроксипрогестерона (прогестерона), 19-норпрогестерона и 19-нортестостерона.
Производные прогестерона по своим свойствам ближе к эндогенному гормону, но они, как правило, имеют невысокую биодоступность. В то же время производные 19-нортестостерона, подразделяющиеся на эстраны (норэтистерон, норэтинодрел) и гонаны (левоноргестрел, гестоден, норгестимат, дезогестрел), характеризуются высокой биодоступностью и рядом дополнительных свойств как полезных, так и нежелательных. Особый интерес представляют так называемые «гибридные» прогестины – норпрегнаны: промегестон (R 5020), номегестрола ацетат, тримегестон и производное андростана – дроспиренон. Эти прогестины объединяют свойства природного прогестерона и современных 19-норпрогестинов. Общей структурной особенностью гибридных прогестинов является отсутствие 17альфа-этинильной группы [38,40]. Первым таким соединением стал диеногест (17альфа-цианометил-17бета-гидрокси-4,9-эстрадиен-3-один; STS 5579) [39].
Использование гестагенов при проведении ГЗТ у женщин с интактной маткой необходимо для защиты эндометрия от пролиферативного действия эстрогенов. От характера используемого гестагена существенным образом зависит не только спектр получаемых фармакологических эффектов, но и приемлемость (переносимость) препарата [49].
В составе ГЗТ, проводимой у женщин с интактной маткой, гестаген в адекватной дозе (в обязательном порядке) назначается в течение 10 дней каждого цикла для предотвращения гиперплазии эндометрия, вызываемой эстрогенами, принимаемыми в течение 21 дня [46]. Если эстроген принимается в течение 28 дней, то продолжительность приема гестагена увеличивают до 14 дней. В период постменопаузы комбинацию эстрогена с гестагеном принимают без перерыва. Для этой цели, обычно, используют левоноргестрел (125 мкг), диеногест (2 мг), медроксипрогестерона ацетат (5 мг), ципротерона ацетат (1 мг), дидрогестерон (10-20 мг) или норэтистерона ацетат (1 мг). У пожилых пациенток с высокой степенью гиперплазии эндометрия для ее подавления требуются более высокие дозы гестагена. Всасывание прогестерона, даже в микронизированной форме после перорального введения, очень вариабельно, и биодоступность невелика. В то же время синтетические гестагены, особенно производные андростана и эстрана, как правило, быстро всасываются и имеют высокую биодоступность, их максимальная концентрация в сыворотке сохраняется в течение 2-5 часов.
Выбор гестагена, дозы и режима использования определяются его способностью эффективно защищать эндометрий, оказывать положительное влияние на обменные процессы, способствуя улучшению самочувствия женщины, и не противодействовать терапевтическим эффектам эстрогенов в плане профилактики и лечения остеопороза, предотвращения развития атеросклероза, болезни Альцгеймера и атрофических изменений слизистых оболочек и кожи.
В этом аспекте особый интерес вызывает новый гибридный гестаген диеногест, уникальность которого состоит в том, что в одной молекуле удалось объединить положительные свойства 19-норпрогестинов (высокая биодоступность при пероральном приеме, короткий период полужизни в сыворотке, отсутствие влияния на цитохром Р450 в микросомах печени, выраженная способность вызывать трансформацию эндометрия, надежное ингибирование овуляции и хороший контроль цикла) и производных прогестерона (умеренное антигонадотропное действие, антиандрогенная активность) [8,24,26,27,33]. Кроме того, только для диеногеста присущи такие свойства, как селективность к рецепторам прогестерона, отсутствие взаимодействия с глобулином, связывающим половые стероиды (ГСПС) и практическое отсутствие влияния на различные параметры метаболизма.
Способность различных гестагенов влиять на матку и яичники, отраженная в величине дозы, вызывающей трансформацию эндометрия (ТД), ингибирующей овуляцию (ДИО) и сдвигающей срок менструации (ДСМ), представлена в таблице 4.
Помимо того, что диеногест обладает очень сильным прогестагенным влиянием на эндометрий, он полностью лишен эстрогенных, антиэстрогенных и андрогенных свойств. Антигонадотропное влияние, а именно подавление секреции ФСГ и ЛГ выражено незначительно. У женщин с регулярным менструальным циклом необходимый антиовуляторный эффект достигается при использовании только 1 мг диеногеста в день, в основном, благодаря его периферическому воздействию – подавлению предовуляторного овариального пика 17b-эстрадиола. Это препятствует положительному по механизму обратной связи воздействию на гипофиз, в результате чего не возникают овуляторные пики ФСГ и ЛГ или они являются отсроченными 20.
По величине отношения дозы, необходимой для подавления овуляции (мг/сут), к дозе, вызывающей полноценную трансформацию эндометрия (мг/цикл), определенной в так называемом тесте Кауфмана, гестагены располагаются следующим образом: норэтинодрона ацетат, левоноргестрел, гестоден [1], дезогестрел и норгестимат [3], ципротерона ацетат и хлормадинона ацетат 6, диеногест [17]. Таким образом, для диеногеста характерно преобладание периферических эффектов, что определяет его благоприятное воздействие на эндометрий, близкое к природному прогестерону.
Гестагены очень эффективны для лечения симптомов эндометриоза и предотвращения его рецидивов [31,54]. Для этой цели обычно используют гестагены без андрогенной активности (медроксипрогестерона ацетат, дидрогестерон) в течение длительного срока.
Для оценки возможности использования диеногеста в лечении эндометриоза использовали модель хирургической аутотрансплантации эндометриоидных имплантатов с последующей овариэктомией. Диеногест оказался наиболее эффективным как для профилактики, так и для лечения экспериментально индуцированного эндометриоза у грызунов и кроликов, так как при его использовании наблюдалось улучшение вызванных имплантатами нарушений внутриклеточного метаболизма и показателей иммунитета [30]. Поэтому при проведении клинических испытаний диеногеста у больных с эндометриозом было принято во внимание, что механизм его действия может быть не только прогестагенным, но и специфическим антипролиферативным [36]. Полученные клинические результаты свидетельствуют о том, что диеногест может применяться с целью уменьшения выраженности эндометриоидных гетеротопий и симптомов, типичных для клинической картины этого заболевания.
Следует подчеркнуть, что большинство прогестинов, которые применяют для лечения эндометриоза, должны при этом заболевании использоваться в более высоких дозах, чем в составе комбинированных оральных контрацептивов (КОК) или препаратов для ГЗТ. Это относится к норэтистерона ацетату, дидрогестерону и медроксипрогестерона ацетату [40] (табл. 5).
В противоположность этому, диеногест является первым прогестином, который при эндометриозе может быть использован в низкой дозе (всего 2 мг/сут), что указывает на высокую тропность препарата к эндометрию. Повышение его дозы до 10 мг 2 раза в день не усиливало клиническую эффективность и не ухудшало переносимость. Побочные эффекты при приеме диеногеста наблюдались крайне редко. По данным стандартизированного опросника, он значительно улучшал общее самочувствие [21].
Еще одной сферой медицинского применения гестагенов является их использование в составе гормональных контрацептивов [7,52,44].
Все современные гормональные контрацептивы можно разделить на гестагенные и комбинированные гестаген-эстрогенные препараты.
Контрацептивы, содержащие только гестаген, в меньшей степени, чем комбинированные, подавляют овуляцию (овуляция происходит приблизительно у 40% женщин, применяющих гестагенную контрацепцию). Поэтому принято считать, что важное значение в противозачаточном действии чисто гестагенных препаратов имеет увеличение вязкости цервикальной слизи, затрудняющее попадание сперматозоидов в полость матки. Даже в тех редких случаях, когда сперма проникает в полость матки, подвижность сперматозоидов оказывается пониженной и вероятность оплодотворения яйцеклетки близка к нулю. Кроме того, гестагены уменьшают число и диаметр желез в эндометрии, а также толщину эндометрия, что снижает возможность имплантации.
Оральные гестагенные контрацептивы (например, левоноргестрел 0,03 мг) часто назначают кормящим женщинам, а также при наличии противопоказаний к использованию эстрогенов. Установлено, что при применении таких препаратов количество гормона, выделяемого с грудным молоком, минимально и практически не оказывает влияния на младенца. При грудном вскармливании, как правило, наблюдаются аменорея и подавление функции яичников, овуляция маловероятна и повышенная вязкость цервикальной слизи затрудняет проникновение спермы в полость матки. Все эти факторы потенцируют контрацептивный эффект гестагенов в период лактации.
В последние годы довольно большое распространение получили парентеральные гестагенные контрацептивные препараты: инъекционные, имплантационные и внутриматочные. Гестагенные парентеральные контрацептивы показаны женщинам, которые плохо переносят пероральные комбинированные гормональных средства или недостаточно внимательны, чтобы строго соблюдать режим ежедневного приема препарата. К преимуществам парентеральных контрацептивов следует отнести возможность использования гормонов в более низких дозах, чем при приеме внутрь, что обусловлено исключением их частичного метаболизма при первичном прохождении через печень. Принципиально новым достижением следует признать разработку внутриматочной системы, содержащей контейнер с гестагеном левоноргестрелом (52 мг), который, постепенно высвобождаясь, оказывает местное воздействие на матку. Система сочетает в себе преимущества внутриматочных спиралей и гормональных контрацептивов, имея при этом ряд преимуществ. По сравнению с пероральными контрацептивами при ее использовании требуется меньшая доза гормона, а по сравнению с внутриматочными медьсодержащими спиралями она не вызывает воспалительных реакций в эндометрии, значительно уменьшает интенсивность менструальных кровотечений и частоту дисменореи. Система приобретает все большую популярность, особенно у рожавших женщин и женщин позднего репродуктивного возраста, когда требуется снижение доз гормонов в используемых контрацептивных средствах. При этом важно, что левоноргестрел защищает женщин от остеопороза, в отличие от другого гестагена – медроксипрогесторона ацетата.
Вместе с тем, в настоящее время большинство женщин предпочитают применять комбинированные оральные контрацептивы, как наиболее надежные, удобные (хорошо контролирующие менструальный цикл) и доступные.
Если в качестве эстрогенного компонента практически всех современных комбинированных оральных контрацептивов используют этинилэстрадиол, то химическая структура гестагенного компонента различна. Именно от природы гестагена, в первую очередь, зависят как величина ингибирования овуляции и увеличение вязкости слизи шейки матки (собственно контрацепция), так и дополнительные эффекты – контроль менструального цикла, изменение обмена липидов, углеводов, белков, андрогенов и др., определяющие индивидуальные характеристики препарата и создающие возможность оптимального выбора.
Среди современных гестагенов наиболее сильным и избирательным по специфическому фармакологическому действию является гестоден; его создание позволило снизить дозу гестагенного компонента до самого низкого уровня 14. В дозе 75 мкг гестоден в сочетании с этинилэстардиолом (30 или 20 мкг) входит в состав нескольких монофазных препаратов. Содержится он и в некоторых трехфазных комбинированных контрацептивах.
Безопасность и высокая эффективность гестоденсодержащих препаратов была доказана в многочисленных доклинических и клинических испытаниях [10,17,35,41,45,47,53]. Фармакологическое обоснование возможности создания на основе гестодена сверхнизкодозированных комбинированных оральных контрацептивов состоит в том, что у добровольцев его ежедневная доза, необходимая для подавления овуляции (основной механизм контрацепции), является наименьшей (0,03 мг/день) по сравнению с другими гестагенами, используемыми в современных гормональных контрацептивах: дезогестрелом (0,06 мг/день), норгестиматом (0,2 мг/день), левоноргестрелом (0,05 мг/день) и норэтистерона ацетатом (0,5 мг/день). Гестоден активен сам по себе и обладает практически 100% биодоступностью, тогда как, например, дезогестрел проявляет свою активность только в виде метаболита 3-кето-дезогестерла и обладает примерно 60% биодоступностью. Данные о рецепторотропной активности гестодена, 3-кето-дезогестрела и прогестерона представлены в таблице 6.
Из таблицы следует, что гестоден и 3-кето-дезогестрел имеют более высокое сродство к прогестероновым рецепторам, чем сам прогестерон. Оба производных 19-нортестостерона проявляли заметное сродство к андрогенным рецепторам простаты и глюкокортикоидным рецепторам тимуса; прогестерон в этом отношении был менее активен. Гестоден и 3-кето-дезогестерл сильно отличались в отношении тропности к минералокортикоидным рецепторам; в этом случае гестоден имеет сходство с прогестероном. Ни одно из испытуемых соединений не взаимодействует с эстрогенными рецепторами. Если использовать только эти данные и на их основании строить гипотезы о преимуществе того или иного препарата, рассчитывая индексы андрогенности, то можно прийти к неправильным выводам, как это имеет место, например, в работе В.Н. Серова и С.В. Никитина [3]. Однако, как уже отмечалось выше, сам по себе факт связывания еще не говорит о том, будут ли рецепторы активированы или ингибированы – поэтому U. Fuhrmann и соавт. [16] провели дополнительное исследование с целью оценки способности гестагенов активировать рецепторы андрогенов, глюкокортикоидов и минералокортикоидов по степени индукции рецепторопосредуемой транскрипции. Было обнаружено, что если агонист андрогенных рецепторов R1881 стимулирует эти рецепторы в клетках CV-1 крысы, то прогестерон не влияет на их функциональную активность. При этом 3-кето-дезогестрел в концентрациях 10-6 и 10-5 М стимулировал андрогенные рецепторы сильнее, чем гестоден. При оценке андрогенной активности гестагенов в организме мыши in vivo не было найдено различий между гестоденом и дезогестрелом (пролекарство 3-кето-дезогестрела) по их способности стимулировать активность андрогензависимого фермента бета-глюкуронидазы в почках [9]. Несмотря на то, что дезогестрел и гестоден имеют небольшую адрогеноподобную активность, их комбинация с этинилэстрадиолом характеризуется in vivo выраженным антиандрогенным действием, благодаря индукции синтеза глобулина, связывающего половые стероиды и ингибированию выработки гонадотропинов, стимулирующих синтез андрогенов в яичниках. Приведенные факты свидетельствуют о том, что оценка андрогенных свойств гестагенов самих по себе, вообще, не может дать правильной информации об андрогенной активности комбинированного препарата, содержащего гестаген и эстроген.
Сравнивая преимущества и недостатки дезогестрел- и гестоденсодержащих комбинированных оральных контрацептивов, с точки зрения их эффективности в плане лечения гиперандрогиний, не следует забывать, что в рекомендациях по их применению нет таких показаний, как акне, гирсутизм, андрогенетическая алопеция или себорея, но они существуют для комбинированного гормонального препарата, содержащего, помимо этинилэстрадиола (35 мкг), ципротерона ацетат (2 мг) – уникальный гестаген, обладающий антиандрогенной активностью, обусловленной блокадой андрогенных рецепторов и ингибированием a-редуктазы, катализирующей превращение тестостерона в более активный дигидротестостерон. В сочетании с этинилэстрадиолом ципротерона ацетат, также как и другие комбинированные контрацептивы, повышает уровень глобулина, связывающего половые стероиды, и ингибирует выработку гонадотропинов гипофизом, что приводит к уменьшению как общей концентрации андрогенов, так и их свободной фракции. В многочисленных рандомизированных клинических сравнительных исследованиях было доказано, что по антиандрогенной активности эстрадиол 35 мкг/ципротерона ацетат 2 мг достоверно превосходит другие комбинированные оральные контрацептивы, в т.ч. дезогестрелсодержащие [15].
Сосредоточив внимание на дополнительных эффектах гестагенов, ученые предложили для целей контрацепции новый гестаген – диеногест, характеризующийся не только хорошей переносимостью, но и сочетанием достоинств природного прогестерона с метаболической устойчивостью синтетических 19-норгестагенов. Диеногест не накапливается в организме при ежедневном приеме и никак не влияет на основные виды обмена – белковый, липидный и углеводный.
Особое преимущество диеногеста в ряду гестагенов состоит в его антиандрогенной активности, поскольку другим 19-норгестагенам, напротив, присущи андрогенные свойства. В отличие от них диеногест не ингибирует активность цитохрома Р450 в микросомах печени крыс и не связывается со специфическими транспортными белками крови – глобулинами, переносящими половые стероиды и глюкокортикоиды.
Учитывая все вышеперечисленные обстоятельства, был разработан оральный комбинированный контрацептив, содержащий 2 мг диеногеста и 30 мкг этинилэстрадиола, который по своим свойствам приближается к представлениям о препарате для широкого применения. Благодаря высокой контрацептивной надежности, очень хорошей переносимости, метаболической нейтральности, контролю менструального цикла и положительному действию на кожу и волосы, он может применяться в течение всего репродуктивного периода.
Физиологические и фармакологические исследования, проведенные в последние десятилетия, позволили описать механизм действия прогестерона и синтетических гестагенов на матку, уточнить их участие в регуляции менструального цикла, пролиферации и дифференциации клеток эндометрия; процессах овуляции и имплантации; росте матки и поддержании беременности [23,28,34,37,48]. Прогресс в исследовании механизмов действия прогестерона и синтетических гестагенов на репродуктивную систему млекопитающих привел к разработке современных гестагенных препаратов, нашедших широкое применение для ГЗТ, гормональной контрацепции, лечения эндометриоза и гормонозависимых опухолей. Однако для правильного выбора гестагенсодержащих препаратов необходимо иметь более точную информацию о молекулярных механизмах их действия как в отдельности, так и в комбинации с эстрогенами. Эти данные необходимы для разработки адекватных критериев выбора того или иного гестагена для каждой женщины в соответствии с индивидуальными особенностями функционирования ее гестагенных рецепторов. Дальнейшие углубленные исследования всех этапов реализации биологической активности гестагенов в клетках разных типов (в норме и патологии) должны способствовать более селективному использованию гестагенных препаратов для ГЗТ, контрацепции, и, особенно, при лечении гормонозависимых опухолей.