Гестагенный эффект что это
Роль гестагенов в клинико-фармакологических эффектах гормональных контрацептивов
*Пятилетний импакт фактор РИНЦ за 2020 г.
Читайте в новом номере
Российский государственный медицинский факультет МЗ РФ
В настоящее время врачами-гинекологами общепризнаны достоинства метода гормональной контрацепции для планирования семьи и улучшения здоровья женщины, продолжаются исследования механизмов действия гормональных контрацептивов и внедрение новых препаратов, создаваемых как путем синтеза новых гормональных соединений, так и с помощью поиска новых комбинаций и дозировок уже известных гестагенов и эстрогенов. [11, 13].
Разработка первых гормональных контрацептивов началась в Германии, в 50-х годах на основании имевшихся в то время сведений о подавлении овуляции во время беременности и о том, что данный эффект обусловлен прогестероном. В 1952 году были получены синтетические гестагены и в конце пятидесятых годов начались клинические испытания этих препаратов в аспекте их способности ингибировать овуляцию и предотвращать беременность. Все современные гормональные контрацептивы можно разделить на чисто гестагенные и комбинированные гестаген-эстрогенные препараты. Комбинированные оральные контрацептивы (КОК) более надежны, лучше контролируют менструальный цикл по сравнению с гестагенными препаратами и поэтому применяются чаще.
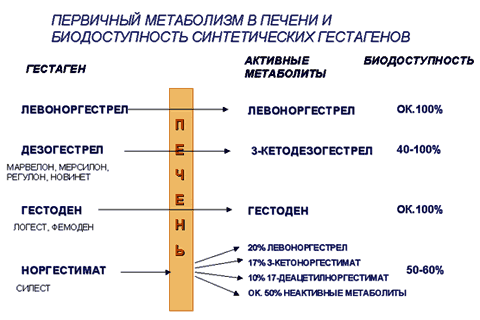
Рис.1 Первичный метаболизм в печени и биодоступность синтетических гестагенов
Существует большое количество исследований in vitro связывания гестагенов с различными стероидными рецепторами [15, 29]. В работе U. Fuhrmann, E. Slater [15] показано, что гестоден и 3-кетодезогестрел могут связываться с андрогенными рецепторами простаты и глюкокортикоидными рецепторам тимуса сильнее, чем прогестерон (табл. 3). Гестоден и 3-кето-дезогестрел отличаются в отношении тропности к минералокортикоидным рецепторам; в этом случае гестоден имеет сходство с прогестероном. Но, как уже отмечалось, сам по себе факт связывания еще не говорит о том, будут ли рецепторы активированы или ингибированы. О результате взаимодействия гормона с рецептором можно судить, оценивая индукцию транскрипции ДНК, зависящую от данного рецептора. Показано, что по способности инициировать транскрипцию в результате связывания с андрогенными рецепторами гестагены расположились в порядке убывания следующим образом: 3-кетодезогестрел > гестоден > прогестерон (заметим, что, именно эти данные лучше отражают андрогенную активность стероидов, в отличие от данных по связыванию с рецепторами). При оценке андрогенной активности гестагенов в целом организме (мыши) не найдено различий между гестоденом и дезогестрелом в их способности стимулировать активность андрогензависимого фермента [8]. Хотя сами по себе дезогестрел и гестоден имеют небольшую остаточную адрогенную активность, их комбинация с этинилэстрадиолом в составе КОК in vivo характеризуется выраженным антиандрогенным действием. Это связано с тем, что КОК подавляют выработку ЛГ, стимулирующего синтез андрогенов в яичниках, и этинилэстрадиол стимулирует синтез в печени транспортного белка крови, переносящего половые стероиды (ГСПС). Это приводит к уменьшению свободной фракции андрогенов в крови. По разным данным, КОК, содержащие 20-30 мкг этинилэстрадиола, вызывают увеличение содержания ГСПС в крови примерно в 1,5-3 раза. Значимых различий увеличения ГСПС при приеме КОК с разными гестагенами нет [20, 26].
Рассматривая другие свойства современных гестагенов, следует отметить, что гестоден и 3-кето-дезогестрел примерно одинаково активируют рецепторы глюкокортикоидов человека. Несмотря на заметное сродство 3-кето-дезогестрела и гестодена к глюкокортикоидным рецепторам, их глюкокортикоидная активность in vivо, определяемая по инволюции тимуса у крыс, была пренебрежимо мала (в 3000 раз слабее дексаметазона). Подобно прогестерону, гестоден ингибирует индукцию альдостероном транскрипции в клетках COS-1, содержащих минералокортикоидные рецепторы человека, а 3-кето-дезогестрел в этом отношении неактивен [15]. При этом сам гестоден не активирует минералокортикоидные рецепторы. В сродстве 3-кетодезогестрела и гестодена к гестагенным рецепторам человека, кроликов и грызунов существуют видовые различия. Таким образом, приведенные данные свидетельствуют о наибольшем сходстве фармакологических свойств гестодена из исследуемых синтетических гестагенов производных 19-нортестостерона с прогестероном. Наличие у гестодена антиминералокортикоидного действия может объяснить меньшую частоту возникновения таких побочных эффектов, как напряжение молочных желез, головные боли, по сравнению с дезогестрелсодержащими контрацептивами [18].
В клинике современный контрацептив должен обеспечивать высокую контрацептивную надежность, хороший контроль менструального цикла, быть хорошо переносимым и безопасным при длительном применении. Безопасность и высокая эффективность гестоденсодержащих препаратов была доказана в многочисленных доклинических и клинических испытаниях [6, 7, 9, 17, 25, 26, 28]. Важно подчеркнуть, что снижение дозы этинилэстрадиола до 20 мкг в комбинации с гестоденом не снижает контрацептивной надежности [11]. Благодаря 100% биодоступности гестоден имеет стабильную фармакокинетическую кривую, что обеспечивает хороший контроль менструального цикла даже в комбинации с низкой дозой эстрогена. В клинических исследованиях показана низкая частота «мажущих» и «прорывных» межменструальных кровянистых выделений при назначении препарата, содержащего 20 мкг этинилэстрадиола в комбинации с 75 мкг гестодена.
В клинических исследованиях показано, что гестоденсодержащие контрацептивы не оказывают клинически значимого влияния на метаболизм липидов, углеводов и систему гемостаза, имеют мало побочных эффектов и хорошо переносятся при длительном применении [10, 12, 13, 16, 26].
Гестагены — что это? Влияние на организм женщины и применение в медицине
Гестагены (от лат. gesto — носить, быть беременной + греч. genes — порождающий, производящий) это группа природных гормонов, а также их синтетических аналогов, которые обладают биологической активностью прогестерона. Лекарственные препараты, содержащие гестагены широко используются в медицине.
Они применяются при планировании и для поддержания беременности (таблетки для приема внутрь, препараты для вагинального введения). Гестагены входят в состав лекарственных препаратов для плановой контрацепции (таблетки, уколы, имплантаты) и экстренной контрацепции. Гестагены назначают в качестве заместительной гормональной терапии женщинам в период менопаузы.
Определение и функции гестагенов
Гестагены (от лат. gesto — носить, быть беременной + греч. genes — порождающий, производящий) это группа природных гормонов, а также их синтетических аналогов, которые обладают биологической активностью прогестерона.
Гестагены влияют на созревание и выход яйцеклетки, имплантацию оплодотворенной яйцеклетки, поддержание и сохранение беременности, развитие альвеолярного аппарата молочной железы, на центральную регуляцию секреции гонадотропинов и полового поведения. Естественные гестагены. оказывают разнонаправленное действие на организм, как местное, так и системное. Общее влияние гестагенов на организм:
Прогестерон и его влияние на организм
Самый важный гестаген в организме — это прогестерон. Прогестерон называют еще гормоном беременности. Этот естественный стероидный гормон вырабатывается желтым телом, плацентой и корой надпочечников. Его концентрация в крови зависит от фазы менструального цикла.
Во время менструации и в фолликулярной фазе его концентрация низкая. Прогестерон начинает вырабатываться во второй фазе цикла, затем происходит овуляция и формирование желтого тела. В лютеиновую фазу наблюдается максимальный уровень прогестерона. Если не произошло оплодотворение, к концу менструального цикла, в связи с обратным развитием желтого тела, его концентрация снижается. Это вызывает отторжение слизистой оболочки матки, происходит менструальное кровотечение.
При наступлении беременности, желтое тело активно функционирует и вырабатывает прогестерон. С четвертого месяца беременности на месте желтого тела образуется плацента. Теперь она отвечает за образование прогестерона в большом количестве, что поддерживает развитие беременности и формирование плода. Незадолго до родов высвобождение прогестерона снижается, уровень гормона падает, что облегчает наступление родов.
Биологическое действие прогестерона заключается в вызове циклических изменений в слизистой оболочке матки, подготовке к беременности.
Применение гестагенов в медицине
В медицинской практике используются основное влияние гестагенов на репродуктивную систему женщины:
Для наступления и развития беременности используют следующее действие гестагенов:
Способы введения препаратов
Препараты гестагенов применяются перорально (внутрь), инъекционно, трансдермально, интравагинально.
Наибольший эффект гестагенов достигается при их вагинальном применении. Вагинальное введение микронизированных гестагенов (например, прогестерона) имеет ряд преимуществ по сравнению с пероральным и инъекционным, благодаря высокому профилю безопасности и хорошей переносимости.
Эффективное действие препаратов при вагинальном введении развивается потому, что в матка и влагалище имеют уникальную систему кровообращения. Это позволяет получить высокую концентрацию препаратов в нужном месте, они не подвергаются системному метаболизму, риск развития общих побочных эффектов минимален.
Длительное вагинальное применение препаратов не влияет на функции печени, почек и липидный профиль, а также на уровень других гормонов, таких как ФСГ (фолликулостимулирующий гормон), ЛГ (лютеинизирующий гормон), кортизола.
Применение гестагенов для контрацепции
За контрацептивное действие из всех гестагенов отвечает прежде всего прогестерон. Только прогестерон можно использовать в качестве эффективного средства контрацепции. Контрацептивное действие прогестерона основано на блокаде выработки гипофизом лютеинизирующего гормона, изменении слизистой оболочки матки, на увеличении густоты цервикальной слизи и снижении ее проницаемости для сперматозоидов. Прогестерон уменьшает сокращение маточных труб. В яичниках гестагены удлиняют выделение эстрогенов и тормозят овуляцию.
Противозачаточные средства могут быть двухкомпонентными и монокомпонентными. В состав двухкомпонентных препаратов входят гестагены и эстрогены. Овуляцию блокирует только гестаген (прогестерон). Эстрогены вводят не для защиты от нежелательной беременности, а для усиления действия гестагенов и контроля менструального цикла.
Монокомпонентные препараты содержат только гестагены. К ним относятся:
Мини-пили
Мини-пили — это таблетки для приема внутрь, содержат только гестагены в одной и той же дозировке, принимаются постоянно, без перерыва. Основное действие препаратов — подавление овуляции, а также увеличение вязкости цервикальной слизи. Мини-пили являются альтернативой для женщин, которые не могут принимать препараты, содержащие эстрогены из-за их непереносимости или при наличии противопоказаний для приема эстрогенов.
К преимуществам данных лекарственных средств относят возможность их применения при кормлении грудью начиная с 6 недели после родов, применяются для контрацепции в позднем репродуктивном возрасте, разрешены курящим женщинам старше 35 лет.
Инъекционная контрацепция
Для инъекционной контрацепции к препаратам гестагенов относится Депо-Провера. Депо-Провера применяется в виде внутримышечной инъекций и вводится один раз в 12 недель. Преимущества препарата: удобство применения (один раз в три месяца), контрацептивное действие сохраняется на протяжении всего периода, высокая эффективность (по оценке специалистов до 99,6%). К недостаткам относят межменструальные кровотечения или выделения с содержанием крови особенно на начальном этапе применения. следует также задержка менструации.
Противозачаточный имплант
Противозачаточный имплант — это средство контрацепции, которое вшивается под кожу в виде пластикового стержня и содержит гормон.
Преимущества: высокая эффективность, действие на протяжении 3-5 лет, не содержит эстрогенов, поэтому может применяться в период лактации (после 6 недель после родов) и при наличии противопоказаний к эстрогенам, разрешен к применению у женщин старшего возраста, в том числе курящих, после удаления имплантата быстро восстанавливается фертильность.
Недостатки: высокая цена, устанавливает и удаляет только врач, возможны сбои цикла, особенно в начале применения. Единственный доступный имплантат — это система Норплант с левоноргестрелом. Выпускается в виде шести тонких палочек-капсул, выделяющих гормон на протяжении пяти лет. Имплантация проводится подкожно в район предплечья.
Гестагены как средство экстренной контрацепции
Гестагены можно использовать в качестве средства для экстренной контрацепции непосредственно после полового акта Препарат следует принимать после консультации гинеколога. Терапия обычно включает в себя прием двух таблеток. Первая принимается сразу после полового акта, вторая — через 12 часов. Эта форма контрацепции не применяется после 72 часов после незащищенного полового акта. Если произошла рвота, нужно принять еще одну таблетку.
Механизм действия препарата заключается в торможении продвижения сперматозоидов через половые пути женщины, достигается при помощи увеличения вязкости и уплотнения цервикальной слизи, сокращении мышц шейки матки, создаются препятствия имплантации эмбриона путем изменения эндометрия, подавляется овуляция, блокируется действие эстрогенов.
Препарат гестагенов для экстренной контрацепции называется Постинор. Одна таблетка содержит 750 мкг левоноргестрела, форма выпуска: 2 таблетки. Среди типичных побочных эффектов отмечается: задержка менструации, тошнота, рвота, отсутствие аппетита, головная боль, депрессия, головокружение. Препарат нельзя использовать в качестве постоянного метода контрацепции. Эффективность зависит времени между половым актом приемом таблеток (чем позже прием — тем меньше эффективность.
Применение гестагенов при патологических кровотечениях у женщин
Одним из показаний для применения гестагенов являются аномальные кровотечения из половых путей. Кровотечения у молодых женщин вызваны нарушением баланса между эстрогенами и прогестероном. Это вызывает чрезмерный рост слизистой матки и сосудов, при его отторжении.
Для остановки кровотечения можно применить гестагены в депо-форме (форма препарата с пролонгированным высвобождением), а также прогестерон внутримышечно в течение 3 дней. Если кровотечение длится более 10 дней, появляются сильные недомогания, боли внизу живота, необходимо присоединить терапию антибиотиками. Примерно через 36 часов аномальное кровотечение из половых путей останавливается. Адъювантная терапия проводится в течение 2-3 циклов.
Применение гестагенов в период менопаузы
Препараты, содержащие гестагены, используются в качестве заместительной гормональной терапии в период менопаузы у женщин. Этот период является физиологическим, переходным этапом, когда происходит снижение гормональной функции яичников, истощение фолликулярной системы, уменьшается выработка прогестерона, а затем эстрогенов. ЗГТ позволяет предотвратить, уменьшить и устранить нарушения функций органов и систем, которые развиваются при дефиците половых гормонов.
Применяется прогестерон и его производные в сочетании с эстрогенами. К гестагенным препаратам, которые используются для заместительной гормональной терапии, относятся: 17-гидроксипрогестерон и 19-норэтистерон. Условиями безопасности применения заместительной гормональной терапии является проведение гинекологического осмотра, мазок на цитологию, ультразвуковое исследование, оценка слизистой оболочки матки (эндометрия) и маммография.
Рекомендуется определение уровня холестерина в крови, коагулограмма, анализ на печеночные пробы. Заместительная гормональная терапия препаратами противопоказана при: кровотечениях из половых органов неустановленной этиологии, некоторых заболеваниях ЦНС, тромбофлебите, печеночной недостаточности, при перенесенном или текущем раке молочной железы, раке матки.
Общие противопоказания для применения гестагенов
Основные противопоказания для применения препаратов, содержащих гестагены следующие: тромбофлебит, тяжелые заболевания печени (печеночная недостаточность, цирроз, опухоли), злокачественные и гормонозависимые опухоли.
Роль гестагенов в заместительной гормональной терапии. Нужны ли гестагены при хирургической менопаузе?

В статье представлены данные литературы и точка зрения авторов по важной медико-социальной проблеме — болезням молочных желез, занимающим ведущее место в заболеваемости женщин. Эти болезни крайне многообразны, они не только нарушают трудоспособность женщи
The article reviews the literature and present the author’s opinion on important medical and social problem – diseases of mammary glands that are the major type of women illness. These diseases are manifold and do not only hamper work ability of women but affect their reproductive functions. The article provides the details of the variants of effective pathogenetic therapy of mastopathies and results of clinical trials. It also gives recommendations to application of unified gynaecological and mammalogy screening as the base of prophylaxis, diagnostics and treatment of mammary glands diseases.
Заместительная гормональная терапия (ЗГТ) является эффективным средством коррекции климактерических нарушений, которые традиционно ассоциируются с вазомоторными симптомами (приливы жара, потливость), нарушениями сна, изменением настроения, метаболическими нарушениями (менопаузальный метаболический синдром), нарушением сексуальной функции и урогенитальными атрофическими изменениями. Кроме того, своевременное назначение ЗГТ является эффективной мерой профилактики постменопаузального остеопороза. Согласно современным представлениям, термин ЗГТ используется для обозначения терапии, включающей эстрогены, гестагены, комбинированную эстроген-гестагенную терапию, андрогены и тиболон [1].
Несмотря на высокую эффективность, широкому применению ЗГТ у женщин в пери- и постменопаузе препятствует ряд стереотипов, мифов и противоречивых данных, связанных с безопасностью такой терапии. В частности, недостаточно изучены вопросы влияния различных типов ЗГТ на молочные железы и сердечно-сосудистую систему. Как правило, ЗГТ назначается сроком не более 5 лет [2]. Это связано с тем, что ряд исследований показал повышение риска развития рака молочной железы при использовании эстроген-гестагенной ЗГТ свыше 5 лет за счет негативного действия гестагенного компонента на молочные железы. Кроме того, у женщин с хирургической менопаузой рекомендуется применять монотерапию эстрогенами для снижения риска развития рака молочной железы, в то время как считается, что гестагены нужны только женщинам с сохраненной маткой для профилактики гиперпластических процессов в эндометрии [3].
В последние годы во многих странах отношение к назначению ЗГТ становится более либеральным, что нашло свое отражение в ряде руководств по постменопаузальной ЗГТ [1, 3, 4], в то время как в России по-прежнему остаются сильны старые стереотипы о том, что ЗГТ при длительном применении значительно повышает риск развития рака молочной железы, инфарктов, инсультов, а также о том, что ЗГТ нельзя назначать пожизненно. Краеугольным камнем и постоянным поводом для дебатов является роль гестагенного компонента в ЗГТ, которая, на наш взгляд, часто остается недооцененной. Гестагены являются синтезированными производными прогестерона — одного из ключевых гормонов, необходимого не только для реализации репродуктивной функции у женщин, но и для поддержания метаболизма.
Роль прогестерона у женщин
Как следует из его названия (лат. pro — для, gestation — беременность), прогестерон — ключевой гормон, необходимый для подготовки к беременности (секреторная трансформация эндометрия) и ее вынашивания (токолитическое действие).
Помимо влияния на матку, прогестерон оказывает действие и на молочные железы, вызывая рост альвеол, долек и приводя к развитию в них железистой трансформации. На протяжении нормального менструального цикла митотическая активность эпителия молочных желез невелика в фолликулярной фазе и достигает максимума в лютеиновой фазе менструального цикла, что связывают с митогенным действием прогестерона. Это действие, однако, непродолжительно, и постоянное присутствие гормона быстро прекращает пролиферацию эпителия [5]. В то же время пролиферация эндометрия максимальна в фолликулярной фазе (благодаря высокой концентрации эстрогенов), а в лютеиновой фазе под действием прогестерона она уменьшается. В зависимости от дозы и продолжительности воздействия прогестерон потенциально может видоизменять ответ как нормальных, так и раковых клеток молочной железы на разных уровнях: посредством стимуляции продукции 17-бета-гидроксистероиддегидрогеназы и эстронсульфотрансферазы, которые быстро окисляют эстрадиол в менее активный эстрон и затем, связывая последний, превращают его в неактивный эстрона сульфат; созревания и дифференцировки эпителия альвеол, который подвергается дальнейшему клеточному делению; down-регуляции эстрогенных рецепторов в эпителии молочных желез, что проявляется снижением пролиферации клеток, стимулированной эстрогенами; модуляции апоптоза клеток модулирования митогенных протоонкогенов.
Таким образом, наряду со снижением экспрессии рецепторов эстрогенов, прогестерон уменьшает локальный уровень активных эстрогенов, ограничивая тем самым стимуляцию пролиферации тканей молочной железы.
Однако было бы ошибочно полагать, что прогестерон оказывает влияние только на ткани и органы репродуктивной системы.
Влияние прогестерона на жировой и углеводный обмен
Прогестерон оказывает важное влияние на показатели углеводного, липидного и белкового обмена. Этот гормон вызывает гиперинсулинемию, возможно, путем прямого действия на бета-клетки поджелудочной железы, а также увеличивает запасы гликогена в печени. При этом он противодействует эффектам инсулина в метаболизме глюкозы в мышечной ткани, вызывая инсулинорезистентность. Прогестерон способствует повышению липопротеидов низкой плотности (ЛПНП) и снижению липопротеидов высокой плотности (ЛПВП). Прогестерон стимулирует отложение жира в организме и оказывает катаболические эффекты на белковый обмен. Все эти биологические эффекты прогестерона определяют физиологические изменения, наблюдаемые во время нормальной беременности [6].
Так, инсулинорезистентность является физиологичным состоянием для беременной женщины и необходима для защиты матери от гипогликемии, так как плод получает глюкозу из материнской крови. ЛПНП являются источником для построения клеточных мембран, соответственно, их повышение необходимо для роста и развития плода. Увеличение жировой массы во время беременности под действием постоянно возрастающей секреции прогестерона является своеобразным энергетическим депо. В то же время инсулинорезистентность, повышение ЛПНП, снижение ЛПВП, увеличение жировой массы (особенно висцерального жира) являются основными факторами риска сердечно-сосудистых заболеваний [1].
Исходя из этого, препараты прогестерона при превышении физиологических концентраций у небеременных женщин могут оказывать негативное влияние на жировой, углеводный и липидный обмен, и чем выше активность препарата (что имеет место у синтетических гестагенов), тем значительнее будут выражены эти негативные побочные эффекты.
Влияние прогестерона на центральную нервную систему
Известно, что наряду с хорошо изученным репродуктивными и эндокринными эффектами, прогестерон играет важную роль в регуляции пластических процессов в головном и спинном мозге, периферической нервной системе. Установлено, что он синтезируется в нейронах и глиальных клетках центральной и периферической нервной системы в приблизительно равных концентрациях у мужчин и женщин [7]. Центральные механизмы действия прогестерона в центральной нервной системе (ЦНС) полностью не изучены.
Прогестерон и синтетические гестагены способны стимулировать синтез и высвобождение нейромедиаторов и нейропептидов в ответ на определенные физиологические и патологические раздражители. Эти эффекты реализуются путем активации рецептора прогестерона или набора внутриклеточных путей его действия. Отличные друг от друга эффекты различных гестагенов на ЦНС определяются количеством нейроактивных метаболитов прогестерона, таких как 3- и 5-альфа-аллопрегнанолон. Аллопрегнанолон влияет на возбудимость нейронов и глии путем прямой активации рецепторов гамма-аминомасляной кислоты (ГАМК)-A, оказывает седативное, анксиолитическое, обезболивающее и противосудорожное действие [8]. Эстрогены повышают в ЦНС и сывороточные уровни аллопрегнанолона, и назначение некоторых синтетических прогестинов может приводить к дальнейшему увеличению уровней аллопрегнанолона в случае, если химическая структура молекулы прогестина приближена к натуральному прогестерону. Натуральный прогестерон и синтетические гестагены могут оказывать различные биологические эффекты в ЦНС [9]. В одном исследовании было показано, что введение энантиомера (зеркального изомера) прогестерона уменьшало отек мозга, гибель нейронов, воспалительные цитокины и реактивный глиоз [10].
Влияние прогестерона на сердечно-сосудистую систему
В исследовании с использованием видеомикроскопической записи кровотока, морфологии кровеносных сосудов, а также деятельности различных клеток крови животных, назначение прогестерона не привело к сосудистой токсичности [11]. Кроме того, в других исследованиях прогестерон и дидрогестерон не противодействовали вазодилатации, вызываемой эстрогенами [12–14]. Тем не менее, были некоторые опасения, связанные с применением высоких доз прогестерона [15, 16]. Некоторые авторы считают, что применение прогестерона может усугублять сердечно-сосудистые воспалительные реакции [17]. В других же исследованиях было продемонстрировано благотворное влияние прогестерона в экспериментально вызванной ишемии головного мозга, где вазоконстрикция является ключевым патологическим процессом [18].
В отличие от натурального прогестерона, применение синтетических прогестинов, таких как медроксипрогестерона ацетат (МПА), показало их сосудистую токсичность [11]. Было показано, что синтетические прогестины вызывали разрушение эндотелия в периферических сосудах и сосудах головного мозга, накопление моноцитов в стенке сосуда, а также активацию тромбоцитов [11]. Подобные эффекты, демонстрирующие негативные последствия МПА на сосудистую систему, были описаны и в других исследованиях [19, 20]. В то же время прогестерон и дидрогестерон увеличивали синтез оксида азота эндотелиальными клетками человека, что не было описано при применении синтетических гестагенов [13, 14].
Влияние прогестерона на нижние мочевые пути
Менопаузальный цистит относится к средневременным последствиям менопаузы. Частота данной патологии по различным данным составляет 30–40% от общего количества урологических больных женщин и наблюдается преимущественно у пациенток от 45 лет и выше, с тенденцией к увеличению в поздний постменопаузальный период, когда угасание гормональной функции достигает своего апогея. В развитии заболевания ведущая роль, в частности, принадлежит дисфункции яичников, сопровождающейся недостатком половых гормонов. Бактериальная обсемененность мочевого пузыря является только предпосылкой к воспалению, реализация же его происходит при нарушении структуры и функции мочевого пузыря. Контроль за эпителиальной проницаемостью в мочевом пузыре традиционно считают результатом уникального строения эпителия, который представляет ионную помпу благодаря наличию специальных соединений между клетками. В то же время известно, что изнутри уротелий покрыт тонким защитным слоем протеогликанов или глико-замзиногликанов (ГАГ), с помощью которого может создаваться и поддерживаться барьер между стенкой мочевого пузыря и мочой, так называемый барьер «кровь–моча». Поверхностные протеогликаны или муцин выполняют в мочевом пузыре различные защитные функции, включая антиадгезивную, и регулируют трансэпителиальное движение растворов. Переходные клетки наружной поверхности ГАГ-слоя способны предотвращать адгезию бактерий, кристаллов, протеинов и ионов. В защитной системе слизистой оболочки мочевого пузыря важная роль отводится гликопротеину, который покрывает слизистую мочевого пузыря, тем самым защищая подлежащие ткани мочевого пузыря от воздействия мочи как агрессивного химического фактора, и выполняет антисептическую функцию. Гликокаликс вырабатывается переходным эпителием. Обволакивая микроорганизмы, попавшие в мочевой пузырь, он элиминирует их. Образование мукополисахаридного слоя (муцина) у женщин является в основном гормонально зависимым процессом, где эстрогены влияют на его синтез, а прогестерон — на выделение его эпителиальными клетками [21].
Влияние прогестерона на костную ткань
Хорошо известно, что костная ткань является мишенью для половых гормонов. Наиболее хорошо изучены эффекты эстрогенов на костную ткань. Кроме того, было показано, что, помимо эстрогенов, андрогены также оказывают действие на костный метаболизм [22, 23]. В 1990 г. были получены экспериментальные, эпидемиологические и клинические данные, подтверждающие важную роль прогестерона в метаболизме костной ткани [24]. Автор предложил, что прогестерон может играть определенную роль в балансе резорбции кости и образовании костной ткани, при том что основное действие эстрогенов — подавление резорбции, а основной эффект прогестерона — формирование костной ткани. Прогестерон может стимулировать образование костной ткани непосредственно путем регуляции экспрессии генов-мишеней, а также косвенным путем, противодействуя влиянию глюкокортикоидов, которые, как известно, подавляют образование костной ткани [24–26].
С момента публикации J. C. Prior [24], публикации, относящиеся к эффектам прогестерона и прогестинов на метаболизм костной ткани, остаются относительно редкими, и их значение в физиологии костного ремоделирования еще недостаточно изучено. Это объясняется несколькими фактами: 1) в ЗГТ используются различные виды прогестинов с разными фармакологическими свойствами и не всегда ясно, могут ли эффекты ЗГТ быть отнесены к действию на прогестероновые рецепторы или этот эффект реализуется через с другие стероидные рецепторы; 2) положительный эффект прогестерона и прогестинов может быть замаскирован одновременным использованием эстрогенов, витамина D и кальция [27, 28]; 3) прогестагены могут действовать в синергии с эстрогенами и не имеют никакого влияния на прогестероновые рецепторы (ПР). В одном клиническом исследовании сочетание низкой дозы этинилэстрадиола с норэтистерона ацетатом оказывало больший остеопротективный эффект, чем монотерапия эстрогенами [29].
Что касается действия непосредственно прогестерона, внутриклеточные ПР присутствуют в культурах остеобластов и остеокластов человека [30–32]. Существует также доказательство того, что прогестерон может воздействовать на костные клетки совместно с эстрадиолом и тем самым усиливать свои эффекты. Таким образом, в культуре остеобластов человека эстрадиол, как было показано, увеличивает удельную связь прогестерона с его ядерными рецепторами [33].
Заключение
На наш взгляд, роль гестагенного компонента в ЗГТ по-прежнему остается недооцененной. Как правило, применение гестагенов в составе ЗГТ обосновывается только защитой эндометрия от пролиферативных эффектов эстрадиола и считается, что назначение гестаген-содержащих препаратов нежелательно женщинам с хирургической менопаузой ввиду возможного повышения риска рака молочной железы. В то же время в исследованиях, показавших, что гестагены могут способствовать увеличению риска развития рака молочной железы при длительном применении, использовались синтетические препараты, такие как МПА и норэтистерона ацетат, действительно повышающие этот риск. В противоположность этому применение натурального прогестерона и максимально приближенного к нему дидрогестерона достоверно не увеличивало риск развития рака молочной железы [34, 35]. Кроме того, в пользу применения гестагенов в составе ЗГТ говорит тот факт, что совместное применение эстрогенов и гестагенов, в отличие от монотерапии эстрогенами, снижает риск возникновения рака печени, рака желчного пузыря и колоректального рака приблизительно на 40% [36, 37].
Мы считаем, что в ЗГТ должны применяться только препараты, максимально приближенные к тем гормонам, которые вырабатываются в организме женщины, а все значимые побочные эффекты (как метаболические, так и онкологические риски) обусловлены только синтетическими составляющими гестагенного компонента ЗГТ.
Литература
ФГБОУ ВПО РУДН, Москва