Гипергликемия неуточненная что это за диагноз
Гипергликемия
Общие сведения
Углеводный обмен во многом определяет общее состояние метаболизма. Углеводы принимают участие практически во всех видах обмена веществ: белков (гликопротеины), нуклеиновых кислот (рибоза/дезоксирибоза), липидов (гликолипидов), нуклеотидов (АТФ, АМФ, АДФ), нуклеозидов (аденозин), ионов. Простые и сложные углеводы являются одним из основных источников энергии, обеспечивающих жизнедеятельность организма, и относятся к обязательному компоненту рациона питания. Расстройства углеводного обмена объединяют в несколько типовых форм (групп) патологии: гипо- и гипергликемия, агликогенозы, гликогенозы, гексоз‑ и пентоземии.
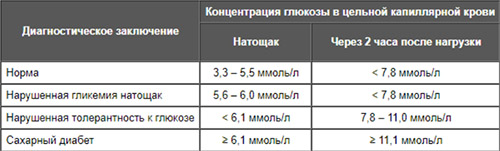
Гипергликемия представляет собой клинический симптом, для которого характерно повышение глюкозы в крови (в плазме крови) более 6,5 ммоль/л натощак и более 8,9 ммоль/л в любое время суток). Код гипергликемии по МКБ-10: R73.9 — Гипергликемия неуточненная. По показателю содержания глюкозы (GLU) различают слабо выраженное состояние 6,7-11,1. Характеризуется значительным и стойким увеличением ГПК до уровня 10,5-11,0 ммоль/л и сочетается с расстройством жизнедеятельности организма. Такого рода гипергликемия определяется как гипергликемический синдром. Наиболее тяжелым проявлением является гипергликемический криз (ГПК> 16,5).
Предметом статьи является ранние нарушения углеводного обмена, которые некоторые авторы определяют как «предиабет». К ранним нарушениям углеводного обмена принято относить состояния нарушенной толерантности к глюкозе (НТГ) и нарушенную гликемию натощак (НГН) или сочетание этих состояний (НТГ+НГН). Принято считать, что предиабет сопровождается высоким риском развития СД2-типа, но в ряде случаев предиабет в СД2Т не конвертируется и оценивается рядом авторов как самостоятельный фактор риска развития сердечно-сосудистых заболеваний. По сути, это пограничные нарушения углеводного обмена, предшествующие развитию сахарного диабета, т.е. гипергликемия при значениях глюкозы, недостаточных для диагноза СД.
Установлено, что при НГН инсулинорезистентность печени и гиперпродукция глюкозы печенью более выражена чем при изолированной НТГ, подтверждением чего является более высокая выработка печенью глюкозы и показатель индекса инсулинорезистентности. Для НТГ характерна периферическая инсулинорезистентность, подтверждением чего являются более низкие показатели индекса чувствительности к инсулину. В случаях комбинации этих состояний (НТГ+НГН) нарушена первая фаза секреции инсулина.
Согласно литературным данным общемировая распространенность НТГ у лиц в возрасте от 30 до 70 лет составляет около 6,7% и продолжает нарастать, а в РФ предиабет имеют около 19% активного населения, то есть эти лица находятся в группе риска развития диабета. Предиабет, как и СД2, ассоциируется с возрастом обследуемых и увеличением массы тела. Гендерные различия в распространенности ранних нарушений углеводного обмена не выявлены.
По экспертным данным риск развития СД2-го типа у лиц с НТГ в 6 раз выше, чем у лиц с нормальной толерантностью к глюкозе, а в случаях сочетания НТГ/НГН риск выше в двенадцать раз. Относительный риск общей смертности у лиц с НТГ в 1,48 раза выше, чем в норме, при этом риск сердечно-сосудистых осложнений повышается в 1,66 раза. При наличии НГН риск развития СД2 в 4,7 раза выше, чем у лиц с нормальной толерантностью к глюкозе. Также НГН ассоциируется с относительно высоким риском развития сердечно-сосудистых осложнений.
Таким образом активное вмешательство необходимо проводить уже на предиабетическом уровне гликемии (этапе НГН и НТГ), тем самым предотвращая развитие СД2-типа, который сопровождается различными осложнениями в виде нарушений зрения, атеросклероза сосудов сердца, нижних конечностей и мозга, нефропатии, поражения нервной системы.
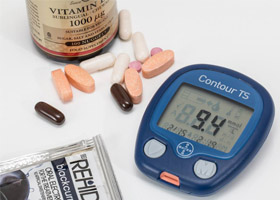
С этой целью всем лицам необходим регулярно проводимый скрининг, позволяющий максимально рано выявить НТГ, НГН, а также СД2-типа и соответственно начать своевременное лечение, а значит, предотвращая тем самым риск развития тяжелых осложнений и потенциальную инвалидизацию пациента в будущем. С этой целью должен регулярно проводиться тест «Постпрандиальная глюкоза», особенно лицам с высоким риском СД, который определяет уровень сахара в крови после приема пищи (через 2 часа). Этот тест позволяет выявить состояние предиабета на ранней стадии, когда еще показатели тощаковой гликемии находятся в норме. Частота самоконтроля уровня глюкозы регулируется в зависимости от потребностей, конкретных обстоятельств и целей пациента. Появление индивидуальных глюкометров различного типа для измерения уровня гликемии позволяет сделать самоконтроль относительно простым и доступным большинству заинтересованных лиц.
Показатели теста постпрандиальной глюкозы кроме диагностики ранних стадий сахарного диабета используются также для оценки риска осложнений со стороны сердечно-сосудистой системы (атеросклероз, ИБС) при СД2.
Патогенез
Патогенез предиабета обусловлен качественным/количественными дефицитом инсулина в основе которого лежит снижение активности инсулина в адипоцитах, мышечной ткани и гепатоцитах, обусловленное дефицитом выработки инсулина β-клетками поджелудочной железы и инсулинорезистентность (снижение чувствительности рецепторов к инсулину). Эти нарушения пострецепторного действия инсулина совместно с нарастающим снижением продуцирования инсулина способствуют повышению глюкозы до соответствующих значений НГН (6,1– 6,9 ммоль/л) и/или НТГ (7,8–11,0 ммоль/л после ПГТТ с глюкозой). У пациентов с умеренной гипергликемией в основе лежит в снижении чувствительности к инсулину периферических тканей, преимущественно мышечной ткани. А при гипергликемии натощак негативно действующим дополнительным фактором может быть увеличение продукции глюкозы печенью.
Классификация
Причины
Причины повышения глюкозы в крови варьируют в широких пределах, основными из которых являются:
К факторам риска развития нарушений углеводного обмена относятся:
Симптомы
Особенностью предиабета является отсутствие четкой специфической клинической симптоматики, характерной для сахарного диабета, что обусловлено в первую очередь сохраненным обеспечением энергией тканей и органов и незначительной глюкозурией. В редких случаях симптомы гипергликемии на этапе НГН и НТГ проявляются в виде неспецифических жалоб пациента на повышенную утомляемость, снижение трудоспособности, ухудшение заживления раневых дефектов.
К косвенным признакам гипергликемии на ранней стадии относят:
При осмотре у большинства пациентов с преддиабетом отмечается увеличение окружности талии до показателей >94 см у лиц мужского пола и >80 см у женщин. При этом, жировая масса распределена преимущественно на туловище при ее относительном уменьшении в области бедер/ягодиц.
Анализы и диагностика
С целью диагностики предиабетного состояния проводится ряд тестов:
Лечение
У большинства пациентов с предиабетом в последующие годы развивается СД 2-го типа, в связи с этим необходимо серьёзно отнестись к этому состоянию. Немедикаментозные методы лечения предусматривают:
В большинстве случаев этих мероприятий достаточно для контроля уровня сахара, и они значительно снижают риск развития диабета. Согласно рекомендациям, нужно стараться достичь показаний гликированного гемоглобина менее 7%. Если диета и физические нагрузки не дают желаемого результата, тогда пациентам рекомендуется медикаментозное лечение. При преддиабете чаще всего назначается Метформин, применение которого является профилактикой сахарного диабета. Основное действие препарата направлено на уменьшение продукции глюкозы печенью и повышение чувствительности мышц и печени к инсулину. В результате ткани активно утилизируют глюкозу, а это улучшает секрецию инсулина поджелудочной железы. Данный препарат не приводит к гипогликемии и не стимулирует секрецию инсулина. Метформин снижает HbA1c на 1,5%. Кроме этого, благоприятно влияет на обмен липидов: снижает содержание холестерина, триглицеридов и липопротеинов низкой плотности. При приеме препарата вес остается стабильным или умеренно снижается.
Наиболее часто при предиабете применяется метформин обычного высвобождения, который принимают 2 раза в день для улучшения секреции инсулина. Препарат Глюкофаж начинают принимать с 500 мг один раз в сутки вечером, а потом к концу первого месяца увеличивают до 850 мг 2 раза в день. При непереносимости этой формы метформина назначают пролонгированный препарат 750 мг по 2 таблетки вечером. Максимально эффективной дозой является 1000 мг 2 раза в день, но чаще всего 850 мг дважды в день. Чем выше доза, тем больше вероятность побочных эффектов со стороны желудочно-кишечного тракта. Эти побочные эффекты ограничивают повышение дозы препарата.
При неэффективности препарата или увеличении уровня гиперкликемии, что свидетельствует о наличии сахарного диабета, лечение проводится различными препаратами, которые подбираются индивидуально. Выбранный гипогликемический препарат должен поддерживать целевой уровень гликемии длительное время. Это могут быть Хлорпропамид, глибенкламид (Манинил, Глиданил, Эуглюкон, Даонил), репаглинид (Диаглинид, НовоНорм), Натеглинид. Прогрессирующий характер заболевания требует комбинированного лечения для достижения гликемии. Также не исключается назначение инсулина.
Показания к назначению инсулина:
У больных всегда имеется опасность декомпенсации углеводного обмена, что проявляется гипо- или гипергликемическими коматозными состояниями.
Если известно, что у больного диабет, но трудно установить причину коматозного состояния, рекомендуется эмпирическое струйное введение глюкозы 40% от 20 до 60 мл. Если у больного состояние гипогликемии, это улучшит его состояние и позволит дифференцировать эти два коматозных состояния. При гипергликемической коме это количество глюкозы почти не скажется на состоянии больного. Быстро некупированная гипогликемия смертельна для пациента. Базисными препаратами для больных в коме, если невозможно определить уровень сахара, являются внутривенно вводимые Витамин В1 100 мг, глюкоза 40% 60 мл и блокатор опиоидных рецепторов Налоксон 0,4-2 мг.
Следует отметить, что гипергликемические коматозные состояния бывают чаще и обусловлены выраженным дефицитом инсулина. Кетоацидотическая кома является осложнением СД 1 типа. Состояние характеризуется повышением сахара более 14 ммоль/л, кетонемией и ацидозом (рН меньше 7,35). Диабетический кетоацидоз может развиваться в течение нескольких часов или нескольких дней, в виде постепенного ухудшения состояния и нарастания декомпенсации. Причина резкого дефицита инсулина:
Первая помощь при гипергликемии прежде всего заключается во введении инсулина малыми дозами, что позволяет постепенного снизить уровень гликемии. В состоянии кетоацидотической комы используют инсулины короткого действия. Если за 2-4 часа не удается снизить гипергликемию, доза инсулина увеличивается.
Диабетический кетоацидоз корригируется также введением жидкости и электролитов, поэтому первая помощь обязательно включает:
Что такое
гипергликемия?
Для людей с впервые диагностированным диабетом, которым незнакомы предупреждающие признаки и симптомы гипергликемии, это состояние может быть пугающим. Гипергликемия может возникнуть, когда уровень сахара в крови слишком высок — натощак или после еды. Поскольку причины гипергликемии довольно разнообразны, обычно каждый больной диабетом рано или поздно переживает приступ. Если диабет у Вас диагностирован недавно, не нужно волноваться — редкие легкие приступы не ведут к существенным отдаленным проблемам со здоровьем, это ожидаемое явление при диабете и часть Вашего обучения. Просто помните о рекомендациях, приведенных в этой статье, и соблюдайте ежедневный режим.
Причины гипергликемии
На уровень сахара в крови влияют многие факторы. Основные причины повышения сахара в крови:
Симптомы и признаки гипергликемии
Как и при гипогликемии, организм сообщает Вам, когда уровни сахара в крови повышаются. Хотя гипергликемия достаточно просто купируется, постоянно высокие уровни сахара в крови могут вызвать серьезные отдаленные осложнения со стороны различных органов.
Основные симптомы гипергликемии:
Купирование гипергликемии
Что же делать, если у вас или кого-то из Ваших близких возникла гипергликемия? Помните о том, что Ваша основная цель — снизить уровень сахара в крови до нормальных значений, в пределах 4-7 ммоль/л (72-126 мг/дл)
Гипергликемия может привести к тяжелым последствиям, если уровень сахара в крови часто выходит за пределы рекомендуемого диапазона. Все больные диабетом самостоятельно отвечают за контроль, отслеживание и регулирование уровня глюкозы в крови, поэтому важно выполнять следующие действия:
Как предупредить гипергликемию
Гипергликемия — состояние, требующее постоянной профилактики. Осведомленность о том, какими могут быть первые признаки повышенного сахара, даст Вам возможность быстро отреагировать и минимизировать вероятность приступа гипергликемии. Есть несколько способов, как держать сахар в норме, например:
С увеличением стажа жизни с диабетом Вы начнете разбираться в том, что подходит для Вашего образа жизни, а что нет. Найдя правильный баланс между введением инсулина, планированием приемов пищи и физической нагрузкой, Вы сможете эффективно осуществлять контроль уровня сахара в крови. Конечно, сначала это может быть сложно, но не переживайте, Вы привыкните и подберете режим, который будет лучше всего работать в Вашем случае.
Осложнения гипергликемии
Если гипергликемия возникает очень редко, Вам не о чем беспокоиться. У многих больных диабетом, как 1, так и 2 типом, это синдром проходит без дальнейших последствий. Если же необходимая помощь не оказана, а высокий уровень сахара в крови сохраняется в течение длительного периода времени, Вы можете столкнуться с краткосрочными и отдаленными осложнениями.
Наиболее распространенное краткосрочное осложнение — это диабетический кетоацидоз (ДКА), который возникает, когда организм вырабатывает большое количество кетоновых тел. Это может приводить к очень серьезным последствиям, в частности, к коме и смерти.
При правильном лечении, контроле и здоровом образе жизни больные диабетом в течение многих лет не страдают никакими осложнениями. Однако если Вы не будете следить за своим организмом или будете болеть диабетом несколько десятков лет, могут возникнуть различные отдаленные осложнения: заболевания сердца, повреждение нервов, проблемы с глазами и стопами и даже ампутации.
Если Вы желаете обсудить с Medtronic какие-либо интересующие вас вопросы касательно гипергликемии, будем рады вам помочь.
1 Diabetes. (n.p.). Diabetes and Hyperglycemia. Retrieved 15 April, 2016, from http://www.diabetes.co.uk/Diabetes-and-Hyperglycaemia.html
©2017 Medtronic International Trading Sarl. Все права защищены. Контент сайта не может быть использован без разрешения компании Medtronic. MiniMed, Bolus Wizard, SMART GUARD, Enlite и Carelink являются зарегистрированными торговыми марками Medtronic, Inc.
Лечение ранних нарушений углеводного обмена
Cпециальной резолюцией Организации Объединенных Наций (ООН) от 20 декабря 2006 года стремительный рост заболеваемости диабетом объявлен чрезвычайной угрозой для всего мирового сообщества, а Всемирный день борьбы против диабета, отмечае
Cпециальной резолюцией Организации Объединенных Наций (ООН) от 20 декабря 2006 года стремительный рост заболеваемости диабетом объявлен чрезвычайной угрозой для всего мирового сообщества, а Всемирный день борьбы против диабета, отмечаемый ежегодно 14 ноября, стал официальным днем ООН. По мнению экспертов ВОЗ, на борьбу с диабетом в различных странах расходуется от 2,5% до 15% годового бюджета систем здравоохранения, а косвенные затраты на эти цели в пять раз выше.
Именно поэтому в настоящее время все большее количество исследований посвящено ранним нарушениям углеводного обмена (РНУО), к которым относят: нарушенную толерантность к глюкозе (НТГ) и нарушенную гликемию натощак (НГН), а также их сочетание (НТГ+НГН) [1]. Ряд авторов объединяют данные нарушения общим термином «предиабет», что подчеркивает их неблагоприятную прогностическую направленность [2, 3].
По данным обзора McMaster, относительный риск развития сахарного диабета 2-го типа (СД 2-го типа) у человека с НТГ в шесть раз выше, чем у человека с нормальной толерантностью к глюкозе (и в двенадцать раз выше при сочетании НТГ и НГН). У лиц с НТГ относительный риск общей смертности в 1,48 раза выше, чем в норме, причем относительный риск фатальных сердечно-сосудистых событий повышается в 1,66 раза [4]. По данным этого же автора, риск развития СД 2-го типа при наличии НГН в 4,7 раза выше, чем при нормальной толерантности к глюкозе. НГН ассоциируется с повышенным риском развития сердечно-сосудистых событий и смертности от всех причин [5]. Таким образом, повышение риска сердечно-сосудистых осложнений наблюдается уже на предиабетическом уровне гликемии [6, 7, 8, 9, 10], соответственно и активное вмешательство должно проводиться уже на этапе НГН и НТГ, предотвращая развитие СД 2-го типа.
Скрининг (от англ. screening— «просеивание») позволяет максимально рано выявить НТГ, НГН и СД 2-го типа, что способствует своевременному началу лечения, а значит, и предотвращению развития серьезных осложнений и инвалидизации больного в будущем [11, 12].
Основой лечения ранних нарушений углеводного обмена является модификация образа жизни (гипокалорийная диета и повышение физической активности). Это подтверждается результатами ряда крупных международных исследований, таких как DPS, USDPP, Da Qing, XENDOS, STORM, STOP-NIDDM и др. [13, 14, 15, 16, 17, 18]. Так, в исследовании DPP в группе интенсивной модификации образа жизни риск развития снизился на 58% по сравнению с группой контроля [20]. Однако, к сожалению, многие пациенты с предиабетом не готовы к радикальному изменению пищевых предпочтений и регулярной физической активности. Поэтому необходим регулярный мониторинг гликемии для оценки состояния углеводного обмена. При этом оральный глюкозо-толерантный тест (ОГТТ) следует проводить каждые 6 месяцев. Если на фоне диеты и регулярных физических нагрузок при повторном проведении ОГТТ через 6 месяцев сохраняются НТГ и/или НГН, следует задуматься об усилении терапии.
Для коррекции гипергликемии на стадии предиабета, помимо модификации образа жизни [13, 15, 20], в литературных источниках имеются указания на успешное применение медикаментозных сахароснижающих препаратов, в частности бигуанидов (метформина) [16, 20] и ингибиторов альфа-глюкозидаз (акарбоза) [21, 22, 23], хотя в настоящее время данные препараты не прошли лицензирование по использованию для лечения НТГ и НГН.
В настоящее время не выработано четко сформулированных показаний к выбору той или другой группы пероральных сахароснижающих препаратов у больных с РНУО, поэтому изучение патофизиологических механизмов у данной категории больных представляется весьма актуальным [24]. Использование внутривенного теста толерантности к глюкозе (ВТТГ) у лиц с РНУО позволяет оценить изменение продукции глюкозы печенью и скорости утилизации глюкозы из крови на фоне назначения различных сахароснижающих препаратов. С этой целью применяется математический анализ с определением показателя скорости элиминации глюкозы из крови (k-индекс) и показателя продукции глюкозы печенью (Н-индекс) [24, 25, 26, 27].
Целью исследования было оценить влияние терапии метформином и акарбозой в сочетании с модификацией образа жизни на развитие СД 2-го типа у больных с РНУО с применением нового метода оценки параметров кинетики глюкозы в ходе ВТТГ.
Материал и методы
ВТТГ проводился исходно и через 6 месяцев следующим образом: внутривенно болюсно вводился раствор 50% глюкозы (из расчета 0,6 г глюкозы на кг массы тела) с последующим забором крови для определения уровня глюкозы. Схема забора крови: –20, —10, 0 (точка введения глюкозы), 2, 3, 4, 5, 6, 8, 10, 14, 19, 22, 24, 27, 30, 40, 50, 70, 90, 120, 150, 180 минута. В каждой точке глюкоза определялась в условиях биохимической лаборатории МОНИКИ. В последующем производился математический анализ результатов (с помощью специально разработанной компьютерной программы, доступной в сети Интернет [29]) с определением показателя скорости элиминации глюкозы из крови (k-индекс) и показателя продукции глюкозы печенью (Н-индекс).
Уровни инсулина, С-пептида, гликированного гемоглобина (HbA1c), аминотрансфераз (АЛТ, АСТ) оценивались при включении в исследование и через 6 месяцев участия в программе. Определение биохимических показателей (глюкоза, АЛТ, АСТ) проводилось в условиях биохимической лаборатории МОНИКИ (биохимический анализатор Hitachi 912, Hoffmann-La Roche Ltd/Roche Diagnostics GmbH, Швейцария-Германия), определение HbA1c производилось на автоматическом анализаторе гликированного гемоглобина Диастат (Био-Рад Лабораториз, США). Инсулин и С-пептид определялись РИА-методом с помощью тест-систем Immunotech RIA (Чехия).
Инсулинорезистентность оценивалась с помощью индекса HOMA-2 [30], который рассчитывался с помощью компьютерной программы HOMA2 Calculator, доступной в сети Интернет [31].
Статистическая обработка результатов исследования проводилась с помощью компьютерной программы SPSS 11.0. Все результаты представлены в виде средних значений (М)± стандартное отклонение (SD), а также целых значений (n) и процента (%). Для сравнения числовых данных (после проверки данных на нормальное распределение с помощью критерия Колмогорова–Смирнова) использовался метод дисперсионного анализа ANOVA для нескольких групп. Анализ количественных данных, изменяющихся в динамике, осуществлялся с помощью критерия Стьюдента для связанных совокупностей. Различия считали статистически значимыми при p 0,05), по частоте нормализации углеводного обмена между группами лечения метформином и акарбозой статистически достоверной разницы не было, а в сравнении с группой контроля разница статистически достоверна (р
А. В. Древаль, доктор медицинских наук, профессор И. В. Мисникова, кандидат медицинских наук И. А. Барсуков МОНИКИ им. М. Ф. Владимирского, Москва
Неотложные состояния при сахарном диабете
Неотложные состояния при сахарном диабете (СД) различаются по этиологии и патогенезу.
Выделяют следующие клинико-метаболические варианты острых осложнений в диабетологии:
— диабетический кетоацидоз и кетоацидотическая кома,
— гиперосмолярная кома и гиперосмолярное гипергликемическое состояние,
— молочнокислый ацидоз (лактат-ацидоз),
— гипогликемия и гипогликемическая кома.
ДИАБЕТИЧЕСКИЙ КЕТОАЦИДОЗ И КЕТОАЦИДОТИЧЕСКАЯ КОМА
Диабетический кетоацидоз (ДКА) – это критическое, ургентное состояние при СД, которое развивается вследствие абсолютного дефицита инсулина или выраженной относительной инсулиновой недостаточности, при несвоевременной диагностике и лечении, приводящее к развитию кетоацидотической комы с тяжелыми гормонально-метаболическими нарушениями органов и систем. ДКА, как правило, развивается при декомпенсации СД 1 типа, но вместе с тем редко может развиваться и при СД 2 типа. Это имеет подтверждение в исследованиях отечественных и зарубежных авторов (В. В. Потемкин, 2008, А. М. Мкртумян, 2008).
Причиной ДКА является абсолютный дефицит инсулина. Той или иной выраженности ДКА определяется у большинства пациентов на момент манифестации СД-1 (10—20 % всех случаев ДКА).
У пациента с установленным диагнозом СД-1 ДКА может развиться при прекращении введения инсулина, зачастую самим пациентом (13 % случаев ДКА), на фоне сопутствующих заболеваний, в первую очередь, инфекционных, при отсутствии увеличения дозы инсулина (30-40 %).
До 20 % случаев развития ДКА у молодых пациентов с СД-1 связаны с психологическими проблемами и/или нарушениями пищевого поведения (боязнь прибавки веса, боязнь гипогликемии, подростковые проблемы). Достаточно частой причиной ДКА в ряде стран является отмена инсулина самим пациентом из-за дороговизны препаратов для некоторых слоев населения (табл. 7. 11).
Вследствие нарастания кетонемии появляется тошнота, рвота, анорексия. Дефицит инсулина и повышенная секреция контринсулярных гормонов способствует распаду белков (катаболизм – протеолиз) в печени и образованию из них глюкозы в реакциях глюконеогенеза, а также аммиака, мочевины, что приводит к азотемии. Гипергликемия, гиперкетонемия, гиперазотемия приводят к нарушениям водно-электролитного обмена, повышению осмотического диуреза, выведению натрия, калия, фосфора, хлора. При полиурии вначале преобладает выделение натрия, поскольку он содержится во внеклеточной жидкости, а затем позднее присоединяется выход калия из клеток и повышенное его выделение с мочой. Развивается выраженное обезвоживание организма, уменьшается объём циркулирующей крови.
Таким образом, при кетоацидотической коме происходят глубокие метаболические нарушения, декомпенсация углеводного, липидного, белкового, электролитного обмена.
Токсическое воздействие кетоновых тел на клетки центральной нервной системы, угнетение ферментных систем, снижение утилизации глюкозы клетками мозга, кислородное голодание ведёт к нарушению сознания, развитию кетоацидотической комы.
Развитие ДКА в зависимости от вызвавшей его причины может занимать от нескольких недель до суток. В большинстве случаев ДКА предшествуют симптомы декомпенсации диабета, но иногда они могут не успеть развиться. Клинические симптомы ДКА включают полиурию, полидипсию, похудение, разлитые боли в животе («диабетический псевдоперитонит»), дегидратацию, выраженную слабость, запах ацетона изо рта (или фруктовый запах), постепенное помутнение сознания. Истинная кома при ДКА в последнее время в силу ранней диагностики развивается относительно редко. При физикальном обследовании выявляются признаки обезвоживания, тургора кожи и плотности глазных яблок, тахикардия, гипотония. В далеко зашедших случаях развивается дыхание Куссмауля. Более чем у 25% пациентов с ДКА развивается рвота, которая по цвету может напоминать кофейную гущу.
Базируется на данных клинической картины, указаниях на наличие у пациента СД-1, а также данных лабораторного исследования. Для ДКА характерна гипергликемия (в ряде случаев незначительная), кетонурия, метаболический ацидоз, гиперосмолярность.
Лабораторная диагностика острых осложнений сахарного диабета
Эффективная осмо-лярность, мОсм/кг
При обследовании пациентов с острой декомпенсацией СД необходимо определение уровня гликемии, креатинина и мочевины, электролитов, на основании чего производится расчет эффективной осмолярности. Кроме того, необходима оценка кислотно-основного состояния. Эффективная осмолярность (ЭО) рассчитывается по следующей формуле:
2 X [Na+ (мЭкв/л) + глюкоза (ммоль/л) ].
У большинства пациентов с ДКА определяется лейкоцитоз, выраженность которого пропорциональна уровню кетоновых тел в крови. Уровень натрия, как правило, снижен вследствие осмотического оттока жидкости из интрацеллюлярных пространств в экстрацел-люлярные в ответ на гипергликемию. Реже уровень натрия может быть снижен ложноположительно как следствие выраженной гипертриглицеридемии. Уровень калия сыворотки исходно может быть повышен вследствие его перемещения из экстрацеллюлярных пространств.
Базируется на данных клинической картины, указаниях на наличие у пациента СД-1, а также данных лабораторного исследования. Для ДКА характерна гипергликемия (в ряде случаев незначительная), кетонурия, метаболический ацидоз, гиперосмолярность
Лабораторная диагностика острых осложнений сахарного диабета
Эффективная осмо-лярность, мОсм/кг
У большинства пациентов с ДКА определяется лейкоцитоз, выраженность которого пропорциональна уровню кетоновых тел в крови. Уровень натрия, как правило, снижен вследствие осмотического оттока жидкости из интрацеллюлярных пространств в экстрацел-люлярные в ответ на гипергликемию. Реже уровень натрия может быть снижен ложноположительно как следствие выраженной гипертриглицеридемии. Уровень калия сыворотки исходно может быть повышен вследствие его перемещения из экстрацеллюлярных пространств.
Другие причины потери сознания у пациентов с СД. Дифференциальная диагностика с гиперосмолярной комой, как правило, не вызывает затруднений (развивается у пожилых пациентов с СД-2) и не имеет большого клинического значения, т. к. принципы лечения обоих состояний сходны. При невозможности оперативно выяснить причину потери сознания пациента с СД ему показано введение глюкозы, т. к. гипогликемические состояния встречаются значительно чаще, а быстрая положительная динамика на фоне введения глюкозы сама по себе позволяет выяснить причину потери сознаний.
Лечение
Диабетический кетоацидоз, прекоматозное состояние и кома требуют немедленной госпитализации больного для проведения экстренной медицинской помощи. Необходимо срочное определение гликемии, глюкозурии, кетонемии и кетонурии, кислотно-щелочного равновесия, содержания натрия и калия, креатинина, мочевины, клинического анализа крови и мочи, ЭКГ, неврологическое обследование. На догоспитальном этапе или в приемном отделении после определения гликемии, глюкозурии, ацетонурии начинают внутривенно капельно инфузию 0, 9 % раствора хлорида натрия, при выраженной дегидратации до 1 л/час, инсулин короткого действия 20 ЕД в/м. Дальнейшее лечение осуществляют в реанимационном отделении или в отделении интенсивной терапии. Лечение ДКА легкой степени при сохраненном сознании и отсутствии тяжелой сопутствующей патологии можно проводить в эндокринологическом или терапевтическом отделении. В отделении реанимации и интенсивной терапии необходимо проводить мониторинг лабораторных показателей в целях предупреждения осложнений терапии – гипогликемии, гипокалиемии и гипонатриемии. Предлагаются следующие схемы лабораторного мониторинга:
Исследование глюкозы крови 1 раз в час, до снижения гликемии ниже 14 ммоль/л, затем 1 раз в 3 часа
Контроль ацетона мочи и кетоновых тел – 2 раза в первые 2 суток, затем 1 раз в сутки
Фосфор – только у пациентов при недостаточности питания и хроническом алкоголизме
Остаточный азот, мочевина, креатинин сыворотки – исходно и через 3 дня
Гематокрит, газоанализ и рН – 1-2 раза в сутки до нормализации кислотно-основного состояния Терапия ДКА направлена на коррекцию основных патофизиологических нарушений. Основные компоненты лечебных мероприятий при кетоацидотической коме включают: устранение инсулиновой недостаточности, восстановление электролитного баланса и кислотно-основного равновесия, лечение сопутствующих заболеваний, которые могут быть причиной ДКА.
В настоящее время доказана целесообразность режима малых доз инсулина при лечении кетоацидотической комы, так как при введении больших доз инсулина имеется опасность развития гипогликемии, гипокалиемии, отёка мозга. Введение малых, физиологических доз инсулина проводится одновременно с регидратацией. При ДКА проводится внутривенная (в/в) инсулинотерапия в виде длительных инфузий. Для достижения оптимальных концентраций инсулина в крови необходима непрерывная инфузия малых доз инсулина – 0, 1 ЕД/кг/час, 4-10 ЕД инсулина в час (в среднем 6 ЕД/час). Это позволяет снизить липолиз, кетогенез и продукцию глюкозы печенью, таким образом воздействовать на главные звенья патогенеза ДКА. Начальная доза ИКД составляет 0, 15 ЕД/кг массы тела (в среднем 10-12 ЕД) и вводится в/в болюсно. Необходимую дозу инсулина набирают в инсулиновый шприц, добирают 0, 9 % NaCl до 1 мл вводят очень медленно (2-3 мин). Затем переходят на в/в введение ИКД по 0, 1 ЕД/кг/час (5-8 ЕД/час) с помощью инфузомата (первый вариант). Инфузионнную смесь готовят следующим образом: 50 ЕД ИКД+2 мл 20% раствора альбумина или 1 мл крови пациента для предотвращения сорбции инсулина в системе, и доводят общий объем до 50 мл 0, 9% NaCl. При отсутствии инфузомата используется второй вариант инсулинотерапии. С этой целью инфузионный раствор готовят из расчета 100 ЕД ИКД на каждые 100 мл 0, 9% раствора NaCl, концентрации ИКД будет составлять 1 ЕД/мл. Для предотвращения сорбции инсулина необходимо добавить 4 мл 20% альбумина на 100 мл раствора. Недостатком данного метода является трудность в титровании малых доз инсулина 12 по числу капель или мл смеси, а также возможность перегрузки жидкостью. Если инфузомата нет, более удобен в использовании 3 вариант. ИКД вводят в/в болюсно 1 раз в час шприцем в “резинку” инфузионной системы. Пример: в инсулиновый шприц набирают 6 ЕД ИКД, набирают в шприц 2 мл и добирают до 2 мл 0, 9% раствора NaCl и вводят медленно в течение 2-3 минут. Длительность фармакодинамического эффекта ИКД при этом составляет до 60 минут. Преимуществом этого способа введения является отсутствие сорбции инсулина, не нужно добавлять в раствор альбумин или кровь, а также более точен учет и коррекция введенной дозы ИКД. Внутримышечная (в/м) инсулинотерапия проводится при невозможности в/в доступа, в отсутствии нарушений гемодинамики и при легкой форме ДКА. Доза ИКД примерно 0, 4 ЕД/кг, из них половина вводится в/в, половина – в/м, затем введение ИКД осуществляется по 5-10 ЕД/час. Недостатками введения ИКД в/м является снижение его всасывания при нарушении микроциркуляции (коллапс, прекома, кома) и дискомфорт для больного (24 в/м инъекции в сутки). При этом, если через 2 часа после начала в/м введения ИКД гликемия не снижается, необходимо переходить на в/в введение. Скорость снижения гликемии при лечении ДКА должна быть не более 4 ммоль/час. Более резкое снижение гликемии создает опасность обратного осмотического градиента между внутри- и внеклеточным пространством, осмотического дисбаланса и отека мозга. В первые сутки не следует снижать гликемию ниже 13 ммоль/л. При отсутствии снижения гликемии в первые 2-3 часа следует провести коррекцию дозы инсулина – удвоить следующую дозу ИКД до 0, 2 ЕД/кг и проверить адекватность гидратации. Если снижение гликемии составило около 4 ммоль/л в час или достигнуто снижение гликемии до 14-15 ммоль/л, необходимо уменьшить следующую дозу ИКД вдвое (0, 05 ЕД/кг), примерно 2-4 ЕД/час. При снижении гликемии ниже 4 ммоль/час рекомендуется пропустить следующую дозу ИКД и продолжить ежечасно определять гликемию. После улучшения 13 состояния, стабилизации гемодинамики, уровень гликемии не более 11-12 ммоль/л и рН>7, 3 переходят на п/к введение ИКД каждые 4-6 часов с коррекцией дозы в зависимости от гликемии в сочетании с инсулином продленного действия 1-2 раза в сутки с начальной дозы 10-12 ЕД.
Адекватная регидратация восполняет не только водный и электролитный дефицит, но и приводит к снижению гликемии, улучшает периферическую гемодинамику и почечный кровоток. При исходно нормальном уровне натрия (менее 145 мэкв/л) для регидратации применяется изотонический (0, 9%) раствор хлорида натрия, при гипернатриемии (>150 мэкв/л) используют гипотонический раствор NaCl. Скорость регидратации составляет 1 литр в 1-й час (с учетом жидкости, введенной на догоспитальном этапе), затем по 0, 5 л во 2-й и 3-й час, по 0, 25-0, 5 л в последующие часы. Скорость регидратации корректируется в зависимости от показателей центрального венозного давления и клинической картины. Объем вводимой за час жидкости не должен превышать часовой диурез более чем на 500-1000 мл. Общее количество жидкости, введенной в первые 12 часов терапии, не должно превышать 10% массы тела.
При достижении уровня глюкозы крови 13-14 ммоль/л, переходят на введение 5-10% раствора глюкозы.
Восстановление электролитных нарушений
Важным разделом терапии кетоацитодической комы является коррекция электролитных нарушений. Развитие дефицита калия в организме, снижение его внутриклеточного содержания при кетоацитодической коме обусловлено повышенной экскрецией калия с потом, вследствие осмотического диуреза. Инсулиновая терапия, регидратация, снижение гликемии, уменьшение ацидоза способствуют поступлению калия в клетку вместе с глюкозой, в обмен на ионы водорода. Явления гипокалиемии проявляются обычно через 3-4 часа после начала инсулинотерапии и введения жидкости, при тенденции к нормолизации рН. Развитие гипокалиемии может приводить к тяжелым осложнениям со стороны сердечно-сосудистой системы – тахикардия, снижение АД, нарушения ритма; дыхательной системы, а также атонии желудка, кишечника, мочевого пузыря. Если уровень К+ плазмы неизвестен, в/в инфузию калия начинают не позднее, чем через 2 часа после начала инсулинотерапии, под контролем ЭКГ и диуреза. В/в инфузию калия начинают одновременно с введением инсулина по следующей схеме: