Гипертрофия трубных валиков у ребенка что это
Новый подход к лечению острого ринита у детей с тубарной дисфункцией
В подавляющем большинстве случаев острые вирусные инфекции, сопровождающиеся ринитом, являются пусковым механизмом для развития дисфункции слуховой трубы. Ключевым моментом в развитии данных функциональных нарушений является отек слизистой носа и носоглотки, а также скопление секрета, что ведет к нарушению вентиляционной функции слуховой трубы (в норме при носовом дыхании воздух через слуховую трубу попадает в среднее ухо, уравновешивая давление по обе стороны барабанной перепонки) и снижению интратимпанального давления. Данные изменения приводят к снижению активности цилиарного транспорта в слуховой трубе и среднем ухе, повышая риск инфицирования среднего уха и развития острого среднего отита [2].
Среди существующего ряда клинических проявлений тубарной дисфункции самым легким является евстахеит (тубоотит). Данное состояние при отоскопии проявляется втяжением барабанной перепонки без признаков ее воспаления (мирингита). При евстахеите ребенок может предъявлять жалобы на заложенность уха или неприятные тянущие ощущения в нем. Однако в большинстве случаев дети дошкольного возраста жалоб не предъявляют [3].
В ряде случаев евстахеит переходит в острый средний катаральный отит, обязательным клиническим проявлением которого является ушная боль. Острый средний катаральный отит чаще отмечается у детей дошкольного возраста. По данным отечественных авторов, в первые три года жизни хотя бы один эпизод острого среднего катарального отита переносят 90% детей [4]. При этом в последние годы увеличилось число ятрогенных острых средних катаральных отитов, возникающих как следствие назначения пациенту методов струйной ирригации полости носа без учета анамнеза со стороны отиатрической патологии [5].
При длительно сохраняющейся тубарной дисфункции у детей возможно развитие экссудативного среднего отита. Еще А. Politzer в 1862 г. описал болезнь уха, которая по характерным клиническим симптомам напоминала это заболевание. G. Bezold в 1906 г. разработал научные основы клиники заболевания, которые послужили толчком для последующих исследований. Существует множество синонимов названия этого заболевания, в зависимости от точки зрения автора на преобладающее значение того или иного фактора в развитии болезни: «хроническая тубарная дисфункция», «туботимпанит», «отосальпингит», «секреторный отит», «клейкое ухо», «острый негнойный средний отит» и т. д. [6]. По последним данным, распространенность экссудативного среднего отита в детской популяции составляет 6–8% [7–8]. Большую проблему педиатрической оториноларингологии представляет недостаточно высокая клиническая эффективность как консервативных, так и хирургических методов лечения экссудативного среднего отита [9].
Одним из основных направлений в лечении тубарной дисфункции принято считать противовоспалительную терапию, при этом наиболее популярным методом лечения тубоотитов в России является применение назальных сосудосуживающих препаратов [2]. Преимущества вазоконстрикторов заключаются в простоте применения и быстром наступлении эффекта. Однако существует множество побочных эффектов, связанных с применением назальных сосудосуживающих препаратов у детей. В отличие от взрослых, у детей осложнением применения назальных сосудосуживающих препаратов чаще является не развитие медикаментозного ринита, а острое отравление α-адреномиметиками. По последним данным, в структуре госпитализируемых в педиатрические токсикологические отделения детей не менее 20–30% составляют случаи отравления нафазолином [10]. Помимо воздействия на сосудистую систему полости носа вазоконстрикторы отрицательно действуют и на функцию мерцательного эпителия. Экспериментальные исследования показали, что большинство деконгестантов замедляет частоту биения ресничек [11]. Наибольшей цилиотоксичностью обладают препараты нафазолина, оксиметазолина и препараты тетризолина на масляной основе [12]. Однако последние исследования показали, что львиная доля цилиотоксического эффекта назальных сосудосуживающих препаратов обеспечивается консервантами-антисептиками (бензалкония хлорид, моногидрат лимонной кислоты, цитрат натрия), входящими в состав большинства деконгестантов [13–14]. Возникновение жжения, явления раздражения и сухости слизистой полости носа при применении назальных сосудосуживающих препаратов также определяются действием консервантов‑анти-септиков. Последними исследованиями было установлено, что разные консерванты-антисептики в составе сосудосуживающих препаратов имеют различную степень цилиотоксичности: угнетение частоты биения ресничек мерцательного эпителия полости носа в меньшей степени проявляется при применении носовых капель, содержащих бензалкония хлорид, чем при наличии в качестве кон-серванта-антисептика комплекса моногидрата лимонной кислоты и натрия цитрата [14].
Возможной альтернативой назальным сосудосуживающим препаратам в лечении воспалительных заболеваний полости носа являются комплексные гомеопатические препараты, среди них – Коризалия («Лаборатория Буарон», Франция). Благодаря своему составу Коризалия устраняет не только воспалительные изменения полости носа (действие Belladonna, Gelsemium), но и нормализует количество (действие Alium cepa, Sabadilla, Belladonna) и реологию секрета (действие Kalium bichromicum, Pulsatilla) в полости носа и носоглотке, быстро и эффективно устраняя симптомы ринита и аденоидита. При этом ранее накопленный клинический опыт применения препарата Коризалия в педиатрической практике говорит об отсутствии противопоказаний и побочных эффектов, связанных с его использованием [15–16].
В проведенном исследовании повышения клинической эффективности терапии детей с острым ринитом и тубарной дисфункцией приняли участие 150 детей в возрасте от 3 до 15 лет с клиническими признаками острого ринита и тубарной дисфункции. Исследуемые дети были распределены на три группы. В 1‑й группе 50 пациентам ежедневно проводили промывание полости носа препаратом Аквалор® Софт (не менее 3 раз в сутки), а также давали препарат Коризалия по схеме (1‑й день – 1 таблетка рассасывать под язык каждый час; 2–5‑й дни – 1 таблетка каждые 2 часа); во 2‑й группе 50 пациентам в качестве терапии было назначено интраназальное применение физиологического раствора и дозированного спрея 0,05%-ного (до 6 лет) и 0,1%-ного раствора ксилометазолина на семидневный курс лечения; в 3‑й группе 50 пациентов получали монотерапию препаратом Коризалия в течение 5–7 дней.
Критериями исключения из исследования были приняты: клинически подтвержденные первичные и вторичные иммунодефициты; онкологические заболевания; гипертрофия аденоидных вегетаций III степени; клинически значимые изменения архитектоники полости носа (искривления носовой перегородки, гипертрофия носовых раковин); хронические формы ринитов и риносинуситов; гнойные формы средних отитов; самовольное или самостоятельное применение лекарственных препаратов, которые не включены в схему лечения по протоколу исследования.
Оценку эффективности лечения проводили на основании как субъективных, так и объективных критериев. Субъективная оценка эффективности лечения (степень затруднения носового дыхания, количество выделений из носа) давалась родителями пациентов по десятибалльной ВАШ, в которой отсутствие симптома соответствовало 0 баллов, максимальная его выраженность равнялась 10 баллам. Также учитывались жалобы пациентов (или со слов их родителей) на заложенность уха или снижение слуха. На стадии «визит 0» (1‑й день) учитывали особенности строения носоглотки (степень гипертрофии аденоидных вегетаций, состояние устья слуховой трубы). На стадии «визит 3» (21‑й день) родители пациентов давали свою оценку результату лечения (положительный или отрицательный). Объективную оценку получали на основании результатов эндоскопического исследования полости носа и носоглотки: определяли степень отечности слизистой полости носа (по десятибалльной ВАШ).
Риноэндоскопическое исследование осуществлялось жесткими эндоскопами диаметром 2,7 мм с 0° торцевым сечением по стандартной методике. Оценку функции слуховой трубы проводили по данным акустической тимпанометрии по стандартной методике на импедансометре Interacustics AТ235 h. Типы тимпанограмм определялись в соответствии с классификацией Jerger (1970): тип А – отсутствие патологии среднего уха и нормально функционирующая слуховая труба, давление в барабанной полости равно атмосферному (поэтому максимальная податливость регистрируется при создании в наружном слуховом проходе такого же давления, принимаемого за «0»); тип В – полость среднего уха заполнена экссудатом (поэтому изменение давления в наружном слуховом проходе не приводит к существенному изменению податливости – тимпанограмма выглядит как ровная или слегка выпуклая линия без видимого пика); тип С – нарушение вентиляции полости среднего уха и возникновение в нем отрицательного давления ниже –100 мм вод. ст. (рис. 1–2).
Контрольные осмотры проводились на 5‑й, 10‑й и 21‑й день после начала лечения.
Статистическую обработку результатов осуществляли с помощью программы Statistica v.6.0. Для сравнения результатов использовали критерий Вилкоксона. Разницу считали статистически достоверной при р 0,05). Однако на 21‑й день наблюдения разница между показателями в 1‑й и 2‑й группах вновь была статистически достоверна: в 1‑й группе – 1,0 ± 0,4 балла, во 2‑й – 2,2 ± 0,8 (p 0,05) (рис. 4).
По данным риноэндоскопической картины отек слизистой оболочки полости носа пациентов был выражен в баллах ВАШ. До начала лечения данный показатель составил в 1‑й группе исследования 9,2 ± 0,6 балла, во 2‑й группе – 9,4 ± 0,6 и в 3‑й группе – 9,5 ± 0,6 балла. На 5‑й день исследования данные показатели составили: в 1‑й группе – 5,5 ± 1,6 балла, во 2‑й группе – 4,8 ± 1,2 и в 3‑й группе – 5,8 ± 1,2 балла (р > 0,05). Не было получено достоверной разницы между показателями ВАШ у пациентов групп исследования и на 10‑й день после начала лечения: 1‑я группа – 3,8 ± 1,4 балла, 2‑я группа – 3,6 ± 1,5 и 3‑я группа – 4,2 ± 1,8 балла (р > 0,05). При контрольном осмотре на 21‑й день была отмечена отрицательная динамика у пациентов во 2‑й группе исследования, где показатель ВАШ составил 4,4 ± 1,6 балла, тогда как у пациентов в 1‑й и 3‑й группах исследования значительной отрицательной динамики выявлено не было, и показатель ВАШ в 1‑й группе составил 3,2 ± 1,2 балла, в 3‑й группе – 4,0 ± 1,6 балла. При этом было получено статистически достоверное различие между показателями ВАШ в 1‑й и 2‑й группах исследования (р
Гипертрофия аденоидов
Гипертрофия аденоидов (аденоидные вегетации/разрастания, гипертрофия носоглоточной/глоточной миндалины) – это стойкое увеличение носоглоточной миндалины. Может встречаться как изолированно, так и в сочетании с гипертрофией небных миндалин.
Носоглоточная миндалина (аденоиды) – скопление лимфоэпителиальной ткани в верхней части носоглотки. Результат ее увеличения называется гипертрофией аденоидов, а при воспалении процесс называют аденоидитом. В сочетании с небными, трубными и язычной миндалинами составляют кольцо Пирогова-Вальдейера, расположенного на входе в верхние дыхательные пути и пищеварительный тракт и выполняющего роль местного иммунного барьера.
Гипертрофия аденоидов чаще всего наблюдается в возрасте от 2 до 6 лет, но может встречаться и в более позднем возрасте.
Существует несколько классификаций аденоидов по степени увеличения. Наиболее популярно разделение, основанное на субъективной оценке врачом размера миндалины при осмотре:
Однако недостаточно только оценки размера миндалины, важным критерием является тщательный сбор анамнеза.
Гипертрофия аденоидов I-II степени в возрасте от 2 до 6 лет зачастую является физиологическим процессом, который связан с тем, что ребенок начинает активно контактировать с окружающим миром и миндалина подвергается постоянной антигенной стимуляции.
Выраженная (или патологическая) гипертрофия, которая приводит к описанным ниже симптомам, может возникнуть из-за инфекционной или неинфекционной причины. Среди инфекционных выделяют следующие:
Среди неинфекционных причин выделяют гастроэзофагеальный рефлюкс, аллергию, длительное воздействие сигаретного дыма.
Симптоматика при гипертрофии возникает из-за увеличения размеров миндалины и/или наличия в ней хронических воспалительных изменений (хронический аденоидит). Хотя эти процессы зачастую связаны (длительное воспаление приводит к гипертрофии), нужно учитывать, что так происходит не всегда. Например, при аденоидных вегетациях I степени могут присутствовать выраженные признаки хронического воспаления, а при вегетациях III степени может вообще не быть клинических проявлений. При физиологической гипертрофии процесс проходит без каких-либо симптомов либо с незначительными проявлениями.
При выраженной гипертрофии у ребенка затруднено носовое дыхание, в связи с чем он дышит через рот, храпит во время сна, иногда с остановками дыхания (синдром обструктивногоапноэ во сне). Нарушение вентиляции полости носа приводит к слизистым выделениям, частым риносинуситам. Характерно чихание, неприятный запах изо рта. Крупные аденоиды давят на мягкое небо, у детей нарушается фонация и артикуляция, дети гнусавят. Если аденоиды блокируют слуховые трубы, это может проявляться рецидивирующими острыми отитами, снижением слуха, связанным со скоплением в среднем ухе жидкости (экссудативный средний отит). Со временем из-за кислородного голодания ребенок становится вялым и апатичным, раздражительным. Происходит ухудшение памяти, снижение внимания, трудности в обучении. Сон с открытым ртом в течение длительного времени приводит к нарушению развития лицевого скелета. Твердое небо становится высоким и узким, нижняя челюсть узкой и удлиненной, нарушается прикус, что в будущем может потребовать ортодонтического лечения. Опытный оториноларинголог сразу распознает типичный «аденоидный» вид ребенка.
Различают острое и хроническое воспаление слизистой оболочки носоглоточной миндалины:
Золотым стандартом диагностики в общемировой практике и стандартом нашей больницы является проведение эндоскопического осмотра полости носа. Данное исследование мы проводим тонким гибким фиброскопом под местной анестезией.
Проведение рентгенографии в боковой проекции является распространенным способом оценки гипертрофии, однако может вводить в заблуждение. Например, на рентгенограмме может быть видна картина аденоидов III степени из-за увеличения трубных миндалин (они находятся по бокам от носоглоточной), из-за отека слизистой оболочки или скопления густой слизи. Данный метод применяется только в случае невозможности проведения эндоскопии носоглотки.
Важно проводить дифференциальную диагностику с заболеваниями, которые могут иметь похожие клинические проявления (юношеская ангиофиброма, атрезия хоан, полипоз, увеличение задних концов нижних носовых раковин, гипертрофия трубных миндалин).
Физиологическая гипертрофия без каких-либо проявлений или с минимальной симптоматикой лечения не требует, однако необходим эндоскопический осмотр для проведения дифференциальной диагностики.
Лечение может быть консервативным. Оно включает устранение факторов, которые могут вызывать гипертрофию: аллергия, гастроэзофагеальный рефлюкс, пассивное курение. Соответственно, в ряде случаев необходим мультидисциплинарный подход оториноларинголога, аллерголога, гастроэнтеролога и педиатра. Положительный эффект может оказать смена климата на более благоприятный, например, морской. Топические кортикостероиды у детей с трех лет используются в качестве дополнительного лечения, при этом в ряде исследований отмечался некоторый положительный эффект, но целом данные об эффективности этих препаратов неоднозначны. При остром и обострении хронического аденоидита в случае бактериальной инфекции проводится лечение антибиотиками. Также в лечении используют орошение носоглотки солевым раствором. Применение различных масел, муколитиков, местных антибактериальных препаратов, растворов серебра, фитопрепаратов, физиотерапия на сегодняшний день не имеют качественной доказательной базы.
В некоторых случаях без оперативного лечения не обойтись. Операция нужна далеко не каждому ребенку и для нее нужны конкретные показания. При их определении врачи Ильинской Больницы следуют принципам доказательной медицины, опираясь на общемировой опыт. Среди показаний – неэффективность консервативного лечения, рецидивирующие инфекции, острые отиты и синуситы, «аденоидное» лицо. Родители должны понимать, что длительный отказ от операции при наличии показаний, попытка «переждать» или «перерасти» гипертрофию аденоидов может привести к осложнениям, лечение которых в дальнейшем потребует большого количества времени и может отрицательно повлиять на развитие ребенка. Согласно рекомендациям Американской Академии Оториноларингологии и Хирургии Головы и Шеи, аденотомию следует проводить в следующих случаях:
При наличии патологии небных миндалин зачастую операцию по их резекции/удалению проводят одновременно (аденотонзиллотомия/аденотонзиллэктомия), а при экссудативном среднем отите одновременно проводят шунтирование.
Аденотомия со временем претерпела значительные изменения. Ранее эту операцию проводили под местной анестезией с помощью специального ножа (аденотом) под контролем небольшого зеркала, а иногда и вслепую. Во время операции ребенок испытывал стресс, а хирург мог не в полном объеме выполнить операцию. В наше время подобный подход практически не используется, однако в некоторых клиниках сохранился.
Нормализация тубарной функции при аллергическом рините

В процессе течения аллергического воспаления повышается экспрессия адгезивных молекул, которые осуществляют прилипание эозинофилов к сосудистому эндотелию. Доказано, что адгезивные молекулы являются одновременно рецепторами для вирусов, в том числе и для риновирусов. Этим объясняется тот факт, что больные с АР и бронхиальной астмой более подвержены развитию вирусных инфекций. При этом частые респираторно-вирусные заболевания у пациентов с атопией снижают местный иммунитет, особенно в области верхних дыхательных путей, способствуя формированию очагов хронического воспаления (аденоидита, синусита, ринита, тонзиллита) вследствие присоединения вторичной инфекции [1]. Нередко аллергический ринит сопровождается «заложенностью ушей», некоторым снижением слуха, «потрескиваниями» в ушах и иными симптомами, свидетельствующими о дисфункции слуховых труб.
Слуховая труба (tuba auditiva) — евстахиева труба, барабанно-глоточная труба — канал, соединяющий носоглотку с барабанной полостью. Впервые подробно описана в 1564 г. итальянским врачом и анатомом Евстахием (В.?Eustachio).
Слуховая труба (рис. 1) — парное образование длиной 30–40 мм; диаметр ее просвета равен 1–2 мм. Ось слуховой трубы наклонена книзу и кнутри и образует угол около 45° с сагиттальной и около 30° с горизонтальной плоскостью. Барабанное отверстие слуховой трубы проецируется в нижнепереднем сегменте барабанной перепонки. Слуховая труба имеет костную (около 1/3 длины) и хрящевую части. Костная часть слуховой трубы открывается на передней (сонной) стенке барабанной полости барабанным отверстием. Она представляет собой нижнюю часть мышечно-трубного канала височной кости — полуканал слуховой трубы, расположенный в месте соединения каменистой и чешуйчатой частей височной кости. Медиально от нее находится сонный канал с проходящей в нем внутренней сонной артерией.
Хрящевая часть слуховой трубы лежит на наружном основании черепа в борозде у заднего края большого крыла клиновидной кости и подходит медиальным концом к основанию медиальной пластинки крыловидного отростка клиновидной кости. Хрящевая часть слуховой трубы заканчивается глоточным отверстием, расположенным на боковой стенке носоглотки. В области отверстия медиальная пластинка образует утолщение в виде валика. Место перехода костной части в хрящевую называется перешейком слуховой трубы, просвет ее в области перешейка сужен.
От стенок слуховой трубы берут начало три мышцы мягкого неба: напрягающая небную занавеску, поднимающая небную занавеску и трубно-глоточная. Сокращение этих мышц, вызывающее смещение хрящевых и перепончатой пластинок стенки слуховой трубы, регулирует величину ее просвета и способствует проникновению воздуха в барабанную полость.
Артерии слуховой трубы являются ветвями восходящей глоточной, средней менингеальной артерий и артерии крыловидного канала. Вены сопровождают артерии и впадают в венозное крыловидное сплетение. Лимфатические сосуды направляются в латеральные заглоточные и глубокие шейные лимфатические узлы. Иннервация слуховой трубы осуществляется ветвями барабанного сплетения и крылонебного узла.
Слизистая оболочка стенки слуховой трубы представляет собой продолжение слизистой оболочки барабанной полости с одной стороны и носоглотки — с другой. Слуховая труба покрыта многорядным мерцательным эпителием, содержащим бокаловидные слизистые клетки. Движение ресничек эпителия направлено в сторону носоглотки. На поверхности эпителия открываются протоки слизистых желез. Вблизи глоточного отверстия слуховой трубы в слизистой оболочке носоглотки сосредоточена лимфоидная ткань — трубная миндалина.
Слуховая труба выполняет вентиляционную, дренажную и защитную функции. Вентиляционная функция (барофункция) обеспечивает звукопроведение и заключается в поддержании равенства давления с обеих сторон барабанной перепонки. При повышении атмосферного давления воздух из носоглотки через слуховую трубу проникает в барабанную полость, а при понижении — в обратном направлении — из среднего уха в носоглотку. При нарушении барофункции слуховой трубы наблюдаются снижение слуха за счет нарушения звукопроведения и понижение устойчивости барабанной перепонки по отношению к баротравме. Дренажная функция слуховой трубы заключается в удалении из барабанной полости транссудата или экссудата. Защитная функция слуховой трубы связана с бактерицидными свойствами ее слизи, выделяемой слизистыми железами и содержащей Ig А.
Следует отметить некоторые анатомические особенности слуховой трубы у новорожденных: барабанное отверстие слуховой трубы проецируется в верхнем сегменте барабанной перепонки, слуховая труба короткая и широкая, имеет форму цилиндра, что способствуют более легкому (по сравнению со взрослыми) проникновению возбудителей инфекции в надбарабанное углубление барабанной полости.
Нарушение дренажной и защитной функций слуховой трубы может явиться причиной развития острого среднего отита. Нарушение проходимости слуховой трубы является противопоказанием к работам, требующим хорошего слуха, связанным с перепадами атмосферного давления. Основной признак нарушения функции слуховой трубы — втянутость барабанной перепонки, что определяется более низким давлением в барабанной полости по сравнению с атмосферным.
Существует ряд несложных субъективных тестов для определения эффективности работы (проходимости) слуховой трубы.
Проба «пустого глотка». Если проходимость слуховых труб у пациента нормальная, то при глотании он ощущает «щелчки» или «потрескивания» в ушах.
Проба Тойнби (глотание при прижатых к перегородке крыльях носа). При хорошей проходимости слуховых труб также ощущаются «щелчки» или «потрескивания» в ушах.
Проба Вальсальвы — пациент делает глубокий вдох, закрывает рот и нос и пытается выдохнуть. Если слуховые трубы проходимы, возникают такие же ощущения, как в предыдущих пробах. Не следует проводить данный тест у лиц пожилого и старческого возраста и пациентов, склонных к повышению артериального давления.
Продувание по Политцеру. Для проведения данной пробы необходим баллон (резиновая груша емкостью 300–500 мл) с трубкой со съемным наконечником-оливой. Наконечник вводят аккуратно в нос. Пациент произносит по слогам такие слова, как: пароход, ку-ку, также-также. В этот момент доктор сдавливает грушу, и воздух попадает в носоглотку и слуховые трубы. В редких случаях продувание слуховых труб этим методом может вызывать у пациента головокружение, ощущение тяжести во лбу, боль в ухе в момент продувания. С осторожностью следует использовать этот метод при рубцовых изменениях барабанной перепонки, т. к. это может привести к ее разрыву.
Объективным методом исследования работы слуховых труб является тимпанометрия, оценка результатов которой не представляет особых затруднений (рис. 2).
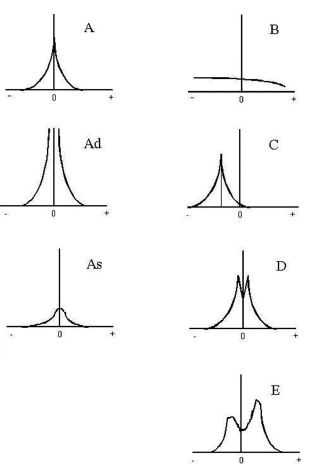
Тимпанограмма типа А — при отсутствии патологии среднего уха и нормально функционирующей слуховой трубе давление в барабанной полости равно атмосферному, поэтому максимальная податливость барабанной перепонки регистрируется при создании в наружном слуховом проходе такого же давления, которое принимается за 0.
Тимпанограмма типа В — при наличии выпота в среднем ухе или адгезивных явлениях в барабанной полости изменение давления в наружном слуховом проходе не приводит к существенному изменению податливости. Поэтому тимпанограмма выглядит как ровная или слегка выпуклая линия без видимого пика.
Тимпанограмма типа С — при нарушении проходимости слуховой трубы, вызванном евстахиитом, патологией носоглотки и т. п., в среднем ухе создается отрицательное давление. Максимальная податливость барабанной перепонки может быть достигнута при создании в наружном слуховом проходе давления, равного давлению в барабанной полости, поэтому тимпанограмма сохраняет нормальную конфигурацию, но и пик ее оказывается смещенным в сторону отрицательного давления.
Тимпанограмма типа D — наблюдается при наличии отдельных рубцов или атрофических изменений барабанной перепонки, приводящих к увеличению ее податливости, проявляющейся, в зависимости от частоты зондирующего тона импедансометра, в повышении амплитуды пика кривой или дополнительных «всплесках» в области максимальной податливости.
Тимпанограммы типа Ad, Е — при разрыве цепи слуховых косточек, вызванном травмой, воспалительным процессом или асептическим некрозом, происходит резкое увеличение податливости звукопроводящей системы. Конфигурация регистрируемой при этом тимпанограммы различна в зависимости от частоты зондирующего тона. При низкой частоте — амплитуда пика обычно превышает рабочий диапазон прибора, при этом появляющаяся «разомкнутая» тимпанограмма обозначается как тип Ad. При высокой частоте зондирующего тона кривая характеризуется появлением дополнительного пика (реже — нескольких дополнительных пиков) и обозначается как тип Е.
Тимпанограммы типа As наблюдаются при отосклерозе, когда барабанная перепонка сохраняет свою эластичность, но фиксация стремени приводит к некоторому снижению податливости звукопроводящей системы, что, как правило, сопровождается некоторым снижением амплитуды тимпанометрической кривой и закруглением ее пика [2].
В течение 2008–2009 гг. под нашим наблюдением находилось 32 пациента с тубарной дисфункцией на фоне аллергического ринита в возрасте от 19 до 42 лет, из них 18 мужчин и 14 женщин. Всем пациентам дважды (до и по окончании курса лечения) кроме клинического анализа крови и ЛОР-осмотра проводилось бактериологическое и цитологическое исследование отделяемого из полости носа, тимпанометрия и аудиометрия, мукоцилиарный транспорт. Все пациенты обследованы аллергологом. У всех пациентов диагноз «аллергический ринит» подтвержден данными лабораторных исследований. Пациенты были разделены на две группы. Распределение больных по полу, возрасту и выраженности клинических проявлений в обеих группах было сравнимо. Пациенты первой группы (17 человек) в течение 6 дней получали местно (путем орошения слизистой оболочки полости носа) глюкокортикостероиды и лечебную гимнастику (ЛГ) для слуховых труб, направленную на улучшение работы мышц, напрягающих небную занавеску, поднимающих небную занавеску и трубно-глоточных. Пациенты второй группы кроме ЛГ получали Виброцил® гель в каждую половину полости носа 3 раза в день. Пациентам рекомендовалось вводить препарат поочередно в правую и левую половины носа, на 1–2 минуты наклоняя голову назад и в сторону той половины носа, в которую введен Виброцил® для лучшего доступа лекарственного средства к устью слуховой трубы. Выбор Виброцила® в форме геля объясняется его более равномерным распределением по поверхности слизистой оболочки и дополнительным увлажняющим эффектом (большинство пациентов (29 человек) отмечали сухость слизистой оболочки носа вне обострения аллергического ринита). Виброцил® — комбинированный препарат для симптоматического местного лечения ринита, содержащий фенилэфрин — альфа-адреномиметик (при местном применении оказывает селективное умеренное сосудосуживающее действие за счет стимуляции альфа1-адренорецепторов, расположенных в сосудах) и диметинден — противоаллергический ЛС-блокатор H1-гистаминовых рецепторов (не оказывает действия на активность мерцательного эпителия слизистой оболочки полости носа).
По окончании лечения было отмечено, что у пациентов второй группы раньше отмечалось уменьшение заложенности ушей и субъективное улучшение слуха (на 2–3 дня), восстановление носового дыхания (без возникновения ощущения сухости носа) — на 2–4 дня. Аудиологические показатели у пациентов второй группы при повторном осмотре (на 6 день лечения) были достоверно лучше, чем в первой группе.
Нежелательных явлений у пациентов обеих групп зарегистрировано не было.
Таким образом, Виброцил ® является эффективным средством при лечении тубарной дисфункции на фоне аллергического ринита, поскольку обладает как сосудосуживающим, так и противоаллергическим свойствами.
Литература
Ключевые слова: тубарная дисфункция, евстахиит, тимпанограмма, ритимпанометрия, аллергический ринит.