Гипофизарная надпочечниковая система что это
Эндокринный бос
Квалификация современных врачей зачастую настолько низка, что они просто не могут поставить диагноз и определить, в каком случае необходимо вмешательство эндокринолога.
О причинах и следствиях этой опасной для жизни пенсионера неразберихи нам рассказала Анна Андреева, заведующая отделением московской ГКБ имени В.В. Вересаева.
Как известно, эндокринология изучает различные обменные процессы, и чаще всего мы говорим о таких заболеваниях, как сахарный диабет или патологии щитовидной железы. Хотя нередко специалисты выявляют другие проблемы, связанные с нарушениями гормональной функции того или иного эндокринного органа. В частности, речь идет о нейроэндокринологии – так называемых заболеваниях гипотоламо-гипофизарной системы.
Гипоталамо-гипофизарная система является «директором» для большого количества органов обмена веществ. Туда входит щитовидная железа, надпочечники, органы репродуктивной системы.
Заболевания гипофиза, вызванные дефицитом или, наоборот, избытком гормонов, напрямую влияют на функциональный актив и состояние периферических систем организма. При этом такие заболевания могут протекать как сопутствующие или существовать отдельно, поэтому догадаться о нейроэндокринном патологическом процессе может не каждый врач.
РАСТЯЖКИ КАК ОБМЕННАЯ ПРОБЛЕМА
Одно из наиболее частых заболеваний – так называемый эндогенный гиперкортицизм, или синдром Иценко-Кушинга. Это редкая, многосимптомная эндокринная болезнь гипоталамо-гипофизарной-надпочечниковой системы, проявляющаяся избыточной продукцией гормона кортизола, который вырабатывает кора надпочечников.
Нередко пациенты с неконтролируемым сахарным диабетом, артериальной гипертензией, ожирением и другими проблемами обращаются к кардиологам, терапевтам и эндокринологам, им подбираются и меняются препараты, однако терапия оказывается неэффективной. Состояние пациентов ухудшается.
Это должно насторожить врача, вызвать вопрос, почему лечение не помогает. Не является ли причиной какой-то другой патологический процесс?
Есть и другие, более специфические проявления нейроэндокринных процессов у таких больных: это хрупкость и ломкость костей (остеопороз), низкорослость, резкий набор веса, изменения кожи и появление растяжек от розового до багрово-синюшного цвета. Чаще всего такие растяжки (стрии) появляются на бедрах, животе, в подмышечной области, в области грудных (молочных) желез.
Классический пример формирования таких растяжек – беременность. Однако в данном случае подобные процессы происходят вне беременности из-за потенциирования катаболического действия кортизола на белковый обмен, нарушения структуры дермы, дезорганизации и снижения количества эластиновых волокон, нарушения коллагенизации, в результате чего кожа истончается. Наличие гематом, изменение цвета стрий является следствием повышенной ломкости капилляров, повышенной проницаемости сосудов.
При обследовании такого «подозрительного» пациента можно также увидеть электролитные изменения крови, такие как гипокалиемия – низкий уровень калия в крови, что может способствовать развитию мышечной слабости.
УСТАЛОСТЬ – ТОЖЕ БОЛЕЗНЬ
Хотя кому из нас незнакомо состояние усталости? Зачастую не только мы сами, но и врачи интерпретируют это как проявление банального переутомления, вирусной инфекции, депрессии. Но если пациент говорит о том, что не может подняться по лестнице, встать со стула без помощи, а недавно делал это, – врач должен задуматься.
Причина этих явлений – гиперсекреция кортизола, очень сильного гормона, который влияет на углеводный и липидный обмен, на перераспределение жировой клетчатки и состояние кожи, на сосудистую проницаемость и электролитные изменения.
Классический пациент с эндогенным гиперкортицизмом имеет избыточную массу тела, ожирение, артериальную гипертензию, страдает сахарным диабетом, остеопорозом, имеет в анамнезе низкотравматичные переломы.
В последние годы все чаще врачи сталкиваются с так называемым скрытым или «субклиническим» гиперкортицизмом, когда подобная симптоматика проявляет себя не яркой клинической картиной, а только одним или двумя симптомами.
В результате обследования в этом случае чаще всего выявляют объемное образование в надпочечниках (кортикостерома). Однако обычно надпочечники являются лишь посредниками этого процесса, а причина изменений кроется в работе гипоталамо-гипофизарной системы.
При подозрении на так называемый центральный гиперкортицизм можно найти образование (аденому) в гипофизе (кортикотропинома). Значительно реже подобные опухоли распространены в других тканях и органах – например, в легких, в тимусе, в желудочно-кишечном тракте.
Обнаружить их ввиду крошечных размеров крайне затруднительно. Пациенту назначают мультиспиральную компьютерную томографию всех заинтересованных органов. При подтверждении заболевания в любом случае требуется хирургическое вмешательство. Сегодня это малоинвазивные методики, после которых пациент быстро восстанавливается и хорошо себя чувствует.
Глюкокортикоиды: мифы и правда
Одни их боятся, другие не представляют себе жизни без них. Все это о глюкокортикостероидах. Глюкокортикостероиды (ГКС) — это стероидные гормоны, которые вырабатываются в коре надпочечников.
Контролирует выработку и уровень этих гормонов система, в которую входят структуры головного мозга: гипоталамус, гипофиз и сами надпочечники. Главным является гипоталамус, он чувствителен к количеству гидрокортизона в плазме крови и стрессу. Если уровень гидрокортизона в крови низкий или случился стресс (напряжение, повреждение, вторжение инфекции) гипоталамус вырабатывает специальное вещество, которое активирует гипофиз. Гипофиз, в свою очередь, выделяет в кровь адренокортикотропный гормон. Он уже действует на надпочечники и стимулирует их на продукцию глюкокортикостероидных гормонов. Когда уровень этих веществ в крови поднимается до нужной концентрации, гипоталамус прекращает стимулировать эту цепочку. Также работу гипофиза и надпочечников могут стимулировать провоспалительные цитокины. Наличие большого количества ГКС угнетает их производство. Так в упрощенном виде происходит взаимодействие и регуляция синтеза глюкокортикостероидов в организме. Надпочечники активно вырабатывают гормоны утром с 6-8 часов, а вечером и ночью их активность минимальна.
На клеточном уровне глюкокортикостероиды попадают в клетку и повышают скорость производства белков с противовоспалительным действием. Эффект проявляется не сразу, а через несколько часов, так как на синтез этих веществ требуется время.
Действие в организме
Противовоспалительное
Гормоны коры надпочечников оказывают противовоспалительное действие, так как влияют на многие звенья этого процесса. Они угнетают синтез веществ способствующих развитию реакции воспаления и наоборот стимулируют образование противовоспалительных элементов. Уменьшают капиллярную проницаемость, что снижает образование отека. Снижают образование рубцовой ткани в зоне воспаления. Уменьшают выраженность немедленных аллергических реакций.
Действие ГКС настолько широкое, что может использоваться при любом типе воспаления. Например, при аллергиях, травмах, инфекциях. Да, это не уберет причину проблемы, но может сдержать симптомы, иногда разрушительные для организма.
Подавление иммунитета
Четко определить черту, когда противовоспалительное действие перейдет в подавление иммунитета нельзя. Вмешательство в иммунные механизмы приводит к разрегулированности иммунитета. Какие-то процессы угнетаются, другие и вовсе блокируются. Это оказывается полезным при аутоиммунных заболеваниях, трансплантации органов и тканей.
Обмен веществ
Глюкокортикостероиды могут ускорять и замедлять образование ферментов, играющих роль в обмене веществ.
Углеводный обмен. Способствуют откладыванию гликогена в печени. Ткани становятся менее чувствительны к глюкозе отчего повышается уровень сахара в крови. Тормозится действие инсулина.
Белковый обмен. Усиливают распад белка и снижают его продукцию. Это преобладает в коже, костях, мышцах. Проявиться это может похудением, мышечной слабостью, истончением кожи, стриями, кровоизлияниями. Снижение синтеза белка становится одной из причин замедления регенеративных процессов. У детей замедляется рост.
Водно-солевой обмен. В почках задержка ионов натрия вызывает постепенное увеличение объема циркулирующей крови и повышение артериального давления. Возникает дефицит калия.
В почках задержка ионов натрия вызывает постепенное увеличение объема циркулирующей крови и повышение артериального давления.
Кальций. ГКС снижают всасывание кальция из желудочно-кишечного тракта и повышают его выведение почками, что может вызвать гипокальциемию и гиперкальциурию. При длительном назначении ГКС нарушение обмена кальция вместе с распадом белкового компонента в костной ткани приводит к развитию остеопороза.
Кровь
Применение ГКС снижает в крови количество эозинофилов, моноцитов и лимфоцитов. Содержание эритроцитов, ретикулоцитов, нейтрофилов и тромбоцитов возрастает. Так действует даже однократное введение с достижением эффекта через 4-6 часов. Восстановление исходного состояния происходит через 24 ч. При продолжительном приеме изменения в крови могут оставаться до 1-4 недель.
Угнетение гипоталамо-гипофизарно-надпочечниковой системы
Так как прием ГКС угнетает производство собственных гормонов, может развиться недостаточность функции коры надпочечников. А проявится она при резкой отмене препарата. Риск возникает уже после 2 недель приема.
Противострессовое действие
Говоря про стрессовое воздействие, имеется в виду повреждение организма (травма, инфекция), которое может нарушить его баланс. ГКС повышают устойчивость организма к стрессу. В условиях тяжелого стресса уровень кортизола может увеличиться более чем в 10 раз. Это нужно, чтобы избыточная воспалительная реакция не привела к фатальным последствиям и была под контролем. Сами цитокины, которые вырабатываются при воспалении стимулируют выработку гормонов надпочечниками, которые ограничивают степень воспаления. Так множество связанных путей регуляции помогают организму поддерживать баланс и выживать в сложных условиях.
Действие на другие гормоны
Глюкокортикостероиды могут оказывать влияние на организм, усиливая действие других гормонов. Так воздействие малых доз ГКС способствует расщеплению жира, оказывает тонизирующее действие на сердечно-сосудистую систему. В результате происходит нормализация сосудистого тонуса, повышается сократимость миокарда и уменьшается проницаемость капилляров. Наоборот, нехватка естественных ГКС характеризуется низким сердечным выбросом, расширением артериол и слабой реакцией на адреналин.
Виды препаратов
На группы эту группу гормонов можно разделить по скорости выведения из организма:
Гормоны также отличаются по выраженности глюкокортикоидных и минералкортикоидных свойств и по силе воздействия на систему регуляции гипоталамус-гипофиз-надпочечники.
Применение
Глюкокортикостероиды применяются врачами только если это необходимо.
Эти лекарства используются в анестезиологической и реаниматологической практике. Внутривенное введение ГКС во время анестезии поддерживает показатели гемодинамики. При тяжелых нарушениях кровообращения препараты способствуют увеличению тканевой перфузии и венозного оттока, нормализацию периферического сопротивления и сердечного выброса, стабилизацию клеточных и лизосомальных мембран.
При тяжелых аллергических реакциях внутривенное введение адекватных доз ГКС оказывает терапевтический эффект, однако начало действия ГКС при этом отсрочено. Так, основные эффекты гидрокортизона развиваются только спустя 2-8 ч после его введения.
Глюкокортикостероиды оказывают выраженный эффект при надпочечниковой недостаточности, развившейся до и во время оперативных вмешательств. Для проведения заместительной терапии используют гидрокортизон, кортизон и преднизолон.
Введение длительно действующих ГКС практикуется для профилактики синдрома дыхательных расстройств у недоношенных детей, что снижает риск осложнений и смерти на 40-50%.
Формы препаратов
Выпускаются различные формы гормональных препаратов. Это сделано не только для удобства применения, но и позволяет получить нужный эффект. Таблетированные формы используются для лечения системных заболеваний, аллергий.
Мази ( Синафлан ), гели используются в дерматологии для лечения кожных заболеваний, аллергий.
Нежелательные эффекты
Нежелательные эффекты связаны с длительностью лечения и дозой. Чаще при длительном использовании более 2 недель и высоких дозах. При этом высокие дозы гормонов в течение 1-5 дней обычно не вызывают развития нежелательных явлений. Проведение заместительной терапии считается безопасным, так как используют очень низкие дозы ГКС.
Нежелательные эффекты:
1. На начальных этапах приема:
2. При сочетании приема ГКС и других препаратов, болезней:
3. Возможные при применении на длительный срок с большими дозами:
4. Поздние и развивающиеся постепенно (связанные с накоплением):
Резкое прекращение краткосрочной (в течение 7-10 дней) терапии ГКС не сопровождается развитием острой надпочечниковой недостаточности, хотя некоторое подавление синтеза кортизола все же происходит. Более длительная терапия ГКС (дольше 10-14 дней) требует постепенной отмены препаратов.
Прием синтетических препаратов с длительным сроком действия вызывают нежелательные эффекты. Резкое прекращение приема гормонов может привести к острой надпочечниковой недостаточности. Восстановление работы надпочечников может занять от нескольких месяцев до полутора лет.
Противопоказания
Глюкокортикостероиды не следует применять без рекомендации врача.
Абсолютных противопоказаний нет, если польза больше, чем риск. Особенно в условиях неотложных ситуаций и краткосрочного применения. При длительном лечении относительными противопоказаниями могут быть:
Без глюкокортикостероидов сегодня в медицине не обойтись. Так как действие их очень разнообразно, врач должен подобрать препарат, подходящий именно в вашем случае.
Гипоталамо-гипофизарная дисфункция
Основой репродуктивной системы женщины является взаимосвязанная цепочка нейроэндокринных органов – гипоталамус – гипофиз – яичник, правильное функционирование которой обеспечивает созревание полноценной яйцеклетки, изменение структуры эндометрия, необходимое для нормальной имплантации эмбриона, правильное функционирование эпителия маточных труб для продвижения оплодотворенной яйцеклетки в матку, имплантацию и сохранение ранней беременности.
Наивысшим органом регуляции гипоталамо-гипофизарно-яичниковой системы является центральная нервная система, путем целого комплекса прямых и обратных взаимодействий обеспечивающая стабильную работу системы репродукции.
Гипоталамус (структура головного мозга) является центром регуляции менструального цикла. С помощью рилизинг-гормонов гипоталамус управляет работой нижележащей железы – гипофиза. Гипофиз, в свою очередь, регулирует работу всех желез внутренней секреции – вырабатывает фолликулостимулирующий гормон (ФСГ), лютеинизирующий гормон (ЛГ), тиреотропный гормон (ТТГ). Под влиянием гормонов гипофиза (ФСГ, ЛГ и пролактина) осуществляются циклические изменения в яичниках: созревание яйцеклетки и овуляция. При большинстве гипоталамо-гипофизарных заболеваний у женщин развивается менструальная дисфункция вплоть до прекращения менструации.
Гипоталамо-гипофизарная недостаточность
Гипоталамо-гипофизарная недостаточность характеризуется снижением уровня гормонов гипоталамуса, приводящим к гипоменструальному и гиперменструальному (реже) синдрому – скудные или обильные со сгустками менструации.
У пациенток с гипоталамо-гипофизарной недостаточностью матка уменьшена в размерах, шейка матки имеет коническую форму, трубы удлиненные, тонкие, извитые, атоничные, влагалище узкое. Такое патологическое состояние называют половым инфантилизмом (недоразвитием). Такие анатомические особенности половых органов играют определенную роль в происхождении бесплодия, но приоритетное значение имеет отсутствие овуляции вследствие снижения уровня фолликулостимулирующего гормона и, как итог, низкого показателя эстрогенов крови.
Лечение эндокринного бесплодия проводится в зависимости от характера и локализации пораженного органа. При гипоталамо-гипофизарной дисфункции в сочетании с половым инфантилизмом только своевременное назначение гормонотерапии приводит к положительным репродуктивным прогнозам. Гормональная терапия обязательно должна проводиться под контролем гинеколога-эндокринолога с обязательной оценкой уровня эстрадиола крови.
Гипоталамо-гипофизарная дисфункция
Причинами дисфункции гипоталамо-гипофизарной системы могут быть физический или психо-эмоциональный стресс, инфекционные заболевания (менингит, энцефалит), заболевания носоглотки (тонзиллит, гайморит), черепно-мозговые травмы, нарушение сна, голодание. В результате нарушается количество и цикличность синтеза половых гормонов. Клинические проявления гипоталамо-гипофизарной дисфункции с расстройствами менструального цикла: недостаточность лютеиновой фазы, ановуляторные циклы (отсутствие овуляции) или аменорея (отсутствие менструации). Отмечается повышенная секреция эстрогенов и высокий уровень пролактина и гонадотропина в крови (гормонов, синтезирующихся в гипоталамусе).
Недостаточное количество ФСГ приводит к отсутствию роста фолликулов, ановуляции и, как следствие, к ановуляторному бесплодию. При ановуляторном бесплодии всегда страдает рост и созревание эндометрия, то есть присоединяется маточный фактор бесплодия. К этой же группе можно отнести женщин с повышенным уровнем выработки яичниками андрогенов (гормонов, отвечающих за мужские половые признаки). Постоянно высокий уровень андрогенов приводит к хроническому подавлению овуляции и может вызвать гирсутизм (повышенное оволосение в нетипичных для женщин местах), угревую сыпь (акне), бесплодие, отсутствие менструаций в течение более чем 6 месяцев. У женщин с гипоталамо-гипофизарной дисфункцией лечение зависит от уровня гормонов в крови.
Гормональное обследование является приоритетным и необходимым условием успешного лечения гипоталамо-гипофизарной дисфункции. При наличии высокого уровня пролактина в крови в сочетании с ановуляцией перед назначением гормональной терапии проводится курс лечения, направленного на снижение выработки пролактина. Если после снижения уровня пролактина восстановления самостоятельной овуляции не произошло, решается вопрос о применении стимуляции функции яичников. На фоне гормональной терапии гиперпролактинемии также проводят стимуляцию овуляции определенными препаратами, что зачастую дает возможность зачать ребенка.
Недостаточность лютеиновой фазы менструального цикла
Одной из причин гипоталамо-гипофизарной дисфункции является недостаточность лютеиновой фазы (НЛФ) менструального цикла. Эта патология возникает при выработке желтым телом недостаточного количества прогестерона, что приводит к неполноценному созреванию структуры эндометрия, необходимому для нормальной имплантации эмбриона, нарушению функционирования эпителия маточных труб для продвижения оплодотворенной яйцеклетки в матку, нарушению процессов имплантации из-за тонкой структуры и морфологического несоответствия эндометрия. Это может привести к эндокринному бесплодию, появлению мажущих кровянистых выделений за 4-5 дней до начала очередной менструации или же к самопроизвольной потере на ранних сроках беременности (6-8 недель).
Гормональным проявлением недостаточности лютеиновой фазы является снижение продукции прогестерона желтым телом, сопровождающееся нормальной или повышенной секрецией эстрадиола. На клеточном уровне недостаточность лютеиновой фазы проявляется усилением клеточных делений (эндометрий, молочная железа, миометрий). Клинически недостаточность лютеиновой фазы проявляется предменструальным синдромом, нарушениями менструального цикла, бесплодием, доброкачественными заболеваниями молочных желез (фиброзно-кистозная мастопатия, фиброаденома молочной железы), патологией эндометрия (полип эндометрия, гиперплазия эндометрия), патологией миометрия (миома матки).
Причинами бесплодия при недостаточности лютеиновой фазы являются недостаточная морфологическая зрелость эндометрия, затрудняющая нормальную имплантацию яйцеклетки, и низкий уровень прогестерона, недостаточный для поддержки беременности малого срока. Недостаточность прогестерона встречается в 25-30 % случаев эндокринного бесплодия. Лечение бесплодия у пациенток с недостаточностью лютеиновой фазы проводится путем назначения препаратов прогестерона во вторую фазу менструального цикла.
Диагностика гипоталамо-гипофизарной дисфункции
Для диагностики нарушений в гипоталамо-гипофизарной-яичниковой системе необходим весь спектр клинико-лабораторных, биохимических и гормональных исследований крови, рентгенологический снимок черепа (области турецкого седла, где находится гипофиз, с целью исключения пролактиномы). Информативным является измерение базальной температуры с построением графика. В период овуляции отмечается увеличение ректальной температуры в среднем на 1°С. При недостаточности лютеиновой фазы отмечается укорочение второй фазы цикла, разница температуры в обе фазы цикла составляет менее 0.6°С. Проводится ультразвуковое исследование роста фолликулов и толщины эндометрия в определенные дни менструального цикла. Проводится биопсия эндометрия за 2–3 дня до начала менструации, позволяющая определить морфологическое созревание эндометрия.
Информативным методом исследования гипофиза является компьютерная томография. Компьютерная томография области турецкого седла позволяет выявить изменения плотности гипофиза, дифференцировать микро- и макроаденомы, «пустое» седло и кисты от нормальной ткани гипофиза.
Для диагностики новообразований гипоталамо-гипофизарной области применяется магнитно-резонансная томография. Магнитно-резонансная томография позволяет различить стебель гипофиза, малейшие изменения структуры гипофиза, отдельные кисты, кистозную опухоль, кровоизлияния, кистозное перерождение гипофиза. Преимущество магнитно-резонансной томографии – в отсутствии рентгеновского облучения, что дает возможность многократно проводить обследование пациентки в динамике.
Роль минералокортикоидов в лечении больных с хронической надпочечниковой недостаточностью
Хроническая надпочечниковая недостаточность (ХНН) — клинический синдром, обусловленный недостаточным содержанием гормонов коры надпочечников, в результате нарушения функционирования одного или нескольких звеньев гипоталамо-гипофизарно-надпочечниковой сис
Хроническая надпочечниковая недостаточность (ХНН) — клинический синдром, обусловленный недостаточным содержанием гормонов коры надпочечников, в результате нарушения функционирования одного или нескольких звеньев гипоталамо-гипофизарно-надпочечниковой системы.
Классификация надпочечниковой недостаточности
Первичная надпочечниковая недостаточность
Центральная (гипоталамо-гипофизарная) надпочечниковая недостаточность
Вторичная надпочечниковая недостаточность
Третичная надпочечниковая недостаточность (повреждения гипоталамуса различного генеза)
Классическое описание первичной хронической надпочечниковой недостаточности было сделано Томасом Аддисоном в 1855 г., тогда как проведение эффективной заместительной терапии заболевания оказалось возможным только в 30-х гг. ХХ в. Первая попытка лечения больных экстрактом надпочечников, который назначался внутрь, была предпринята R. Stockman в 1867 г. и оказалась неудачной. В 1936 г. E. C. Kendall et al. впервые получили из экстракта коры надпочечников кортикостерон и дегидрокортикостерон в кристаллической форме, а в 1937 г. M. von Steiger и T. Reichstein выделили дезоксикортикостерона ацетат (ДОКСА) и синтезировали его из сигмастерола. С 1939 г. ДОКСА в виде внутримышечных инъекций начали с успехом использовать в лечении первичной хронической надпочечниковой недостаточности. В середине 70-х гг. ДОКСА применялся в виде подкожных подсадок кристаллов по 100 мг, что избавляло пациента от необходимости делать инъекции. Однако это затрудняло подбор дозировки из-за индивидуальной скорости всасывания препарата и невозможности регулирования его действия при нестабильном АД, а сама манипуляция подсадки требовала специальной квалификации персонала. В 1953 г. Freed и Sabo синтезировали пероральный минералокортикоид 9α-фторкортизол (кортинефф), который с тех пор широко используется во всем мире и в конце 70-х гг. пришел на смену препарату ДОКСА, применявшемуся до этого в России [2].
Современная заместительная терапия первичной хронической надпочечниковой недостаточности заключается в обязательном комбинированном назначении препаратов глюко- и минералокортикоидов. Типичной ошибкой является лечение первичной хронической надпочечниковой недостаточности с помощью монотерапии глюкокортикоидами. Часто в этой ситуации, несмотря на увеличение дозы препарата, состояние больных не нормализуется, а дозировки продолжают увеличивать, что в ряде случаев приводит к развитию экзогенного синдрома Кушинга [1, 3].
По данным Нидерландского исследования (P. M. J. Zelissen, 1994), назначение монотерапии глюкокортикоидами можно считать обоснованным не более чем в 6,6% случаев, при этом следует учитывать, что практически все обследованные пациенты получали таблетированный гидрокортизон или кортизон-ацетат, который обладает большей минералокортикоидной активностью, чем синтетические глюкокортикоиды.
При вторичной надпочечниковой недостаточности дефицит минералокортикоидов не наблюдается, и в назначении минералокортикоидов (кортинефф) необходимости, как правило, нет, за исключением тех случаев, когда у пациента имеется выраженная артериальная гипотензия [5].
Заместительная терапия первичной хронической надпочечниковой недостаточности минералокортикоидами подразумевает использование только одного препарата — 9α-фторкортизола (9α-FF, кортинефф). Естественный минералокортикоид альдостерон не назначается для заместительной терапии по той же причине, что и ДОКСА, — из-за полной метаболизации при первом прохождении через печень; кроме того, препарат чистого альдостерона стоит достаточно дорого.
Основные преимущества 9α-FF заключаются в его эффективности при пероральном применении, а также в минералокортикоидной активности. После приема внутрь препарат быстро и полностью всасывается из желудочно-кишечного тракта. Своего пика плазменная концентрация 9α-FF достигает через 1,5 ч после приема. Период полувыведения составляет 18—36 ч, что позволяет имитировать практически не имеющую циркадного ритма секрецию альдостерона, благодаря ежедневному однократному приему 0,05—0,2 мг препарата. Метаболизируется 9α-FF в печени, выделяется с мочой в виде неактивных метаболитов. Интересен тот факт, что, как и сам альдостерон, кортизол и 9α-FF имеют одинаковую аффинность к рецепторам альдостерона в почках. Однако если альдостерон и 9α-FF достигают рецептора, то кортизол, попав в клетку, в результате действия 11-b-гидроксистероиддегидрогеназы превращается в неактивный кортизон. Именно поэтому минералокортикоидная активность 9α-FF в 200—400 раз выше, чем у кортизола, хотя эти соединения отличаются друг от друга всего на один атом фтора, который делает 9α-FF неуязвимым для указанного фермента. Глюкокортикоидными эффектами 9α-FF на практике можно пренебречь, поскольку ощутимо они проявляются, если доза препарата превышает 0,5 мг/сут. Глюкокортикоидный эффект 1мг 9α-FF (10 таблеток кортинеффа) эквивалентен 20 мг гидрокортизона.
Фармакологическое действие кортинеффа заключается в воздействии на дистальную часть почечных канальцев, усилении обратного всасывания ионов натрия и воды, а также увеличении выделения ионов калия и водорода. Кортинефф влияет также на выделение воды и электролитов толстым кишечником, потовыми и слюнными железами. Увеличение объема внеклеточной жидкости и задержка натрия в организме приводят к повышению АД. При длительном применении кортинеффа повышение АД связано с увеличением периферического сопротивления, а не только с его влиянием на водно-электролитный обмен [3].
Кортинефф в дозах, превышающих терапевтические, может угнетать функцию коры надпочечников, у молодых пациентов — функцию вилочковой железы, тормозить секрецию АКТГ гипофизом, а также ускорять процесс отложения гликогена в печени, а при недостаточном количестве белка в пище приводить к отрицательному азотистому балансу. По данным литературы, частым симптомом передозировки 9α-FF являются отеки, которые, как правило, не сопровождаются значительным подъемом АД у пациентов с первичной ХНН. Отечность на фоне терапии носит преходящий характер, развиваясь при первом назначении или увеличении дозы препарата.
Кортинефф назначается один раз в сутки в дозе 0,05—0,1 мг (максимально 0,2 мг), ежедневно утром, после еды, его необходимо запивать большим количеством жидкости. В ряде случаев дозу 9α-FF приходится увеличивать летом, особенно в условиях жаркого климата, что связано с повышением потерь натрия и воды, выводящихся из организма с потом.
Если имел место пропуск приема препарата, следует принять его как можно быстрее. Если же приближается время следующего приема, пропущенную дозу нужно отменить. При необходимости доза препарата уменьшается постепенно. Во время терапии кортинеффом не следует проводить вакцинацию. Препарат может маскировать проявление симптомов инфекционно-воспалительных заболеваний. На фоне применения кортинеффа в высоких дозах обязательно определение концентрации электролитов в плазме крови (Na, K) [4].
На сегодняшний день разработаны следующие критерии адекватности минералокортикоидного компонента заместительной терапии первичной ХНН [1, 3]:
Как показало исследование M. Jadoul et al. (1991), артериальное давление при первичной ХНН коррелирует с АРП (см. рисунок) и, таким образом, с дозой 9α-FF. Следовательно, первым шагом в лечении артериальной гипертензии у больных первичной ХНН является ограничение потребления пищевой соли в сочетании с уменьшением дозы 9α-FF. Назначение диуретиков и спиронолактона вместе с кортинеффом не оправдано, поскольку эти препараты действуют как антагонисты [5].
| Воздействие ренин-ангиотензин-альдостерон системы на артериальное давление |
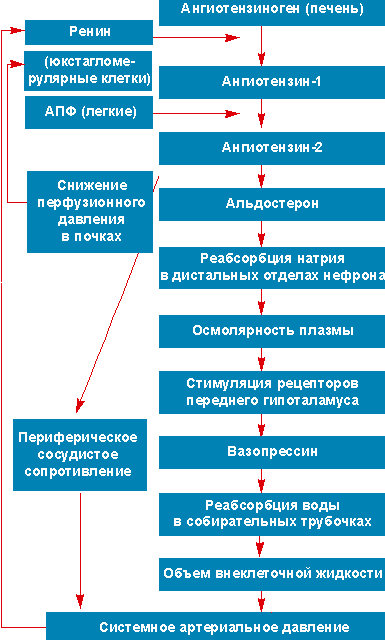 |
Нами был составлен регистр больных с ХНН г. Москвы. Из 300 человек минералокортикоиды были назначены 180 (60%). Большая часть пациентов, принимающих кортинефф, имеют первичную ХНН аутоиммунной природы или развившуюся вследствие оперативного вмешательства. Относительно низкий процент использования минералокортикоидов свидетельствует о недостаточной информированности врачей различных лечебных учреждений г. Москвы о современных подходах к заместительной терапии первичной ХНН. Доза кортинеффа составляла от 0,1 до 0,2 мг и принималась однократно утром. Побочных эффектов (подъемы АД и задержка жидкости) не наблюдалось.
Следует отметить некоторые особенности заместительной терапии кортинеффом во время беременности. При беременности происходит постепенное и значительное увеличение уровня прогестерона, который является антагонистом минералокортикоидов. Поэтому необходимая доза 9α-FF в этот период может значительно возрастать. Подбор дозы должен осуществляться по уровню калия плазмы и артериальному давлению. Уровень АРП неинформативен, поскольку во время беременности он и в норме значительно повышен. Описаны случаи, когда, основываясь на перечисленных критериях, дозу 9α-FF приходилось увеличивать до 0,3 и даже до 0,6 мг в день (S. Diederich et al., 1994).
Дети, рожденные от матерей, получавших 9α-FF, требуют тщательного медицинского наблюдения из-за опасности развития у них недостаточности функции надпочечников. При назначении препарата женщине в период кормления грудью следует решить вопрос о переводе ребенка на искусственное вскармливание [2, 5].
Надпочечниковая недостаточность представляет собой одну из самых серьезных по своим проявлениям и осложнениям эндокринопатий. Больных с хронической надпочечниковой недостаточностью необходимо обследовать два раза в год. Следует подчеркнуть, что для оценки эффективности заместительной терапии решающую роль имеют клинические данные. Не следует добиваться оптимальных лабораторных показателей за счет назначения высоких доз глюко- и минералокортикоидов, что может привести к передозировке и клиническим симптомам гиперкортицизма. В условиях заместительной терапии прогноз заболевания будет зависеть от ее адекватности, что делает обязательным обучение пациентов приемам самоконтроля и наблюдение за ними в специализированном лечебном учреждении.
По вопросам литературы обращайтесь в редакцию
Г. А. Мельниченко, доктор медицинских наук, профессор
Г. Ф. Александрова, кандидат медицинских наук
М. Б. Анциферов, доктор медицинских наук, профессор
Т. С. Елисеева, С. Ф. Машков
ГУ ЭНЦ, Диабетологический центр РАМН, Москва