Гипогаммаглобулинемия у взрослых что это
Гипогаммаглобулинемия у взрослых что это
ГБУЗ «Московский клинический научно-практический центр» Департамента здравоохранения Москвы
Московский клинический научно-практический центр
ГБУЗ «Центральный научно-исследовательский институт гастроэнтерологии» Департамента здравоохранения Москвы
Московский клинический научно-практический центр Департамента здравоохранения Москвы, Центральный НИИ гастроэнтерологии, Москва
Журнал: Терапевтический архив. 2014;86(12): 19-21
ГБУЗ «Московский клинический научно-практический центр» Департамента здравоохранения Москвы
ГБУЗ «Московский клинический научно-практический центр» Департамента здравоохранения Москвы
Московский клинический научно-практический центр
ГБУЗ «Центральный научно-исследовательский институт гастроэнтерологии» Департамента здравоохранения Москвы
Московский клинический научно-практический центр Департамента здравоохранения Москвы, Центральный НИИ гастроэнтерологии, Москва
Гипогаммаглобулинемическая спру (ГГГС) относится к орфанным (редким) заболеваниям и представляет собой особую форму общей вариабельной гипогаммаглобулинемии (ОВГГГ), при которой сочетаются симптомы ОВГГГ и целиакии.
Клиническая картина ГГГС характеризуется хронической диареей, тяжелым синдромом нарушенного всасывания (СНВ) и хроническими очагами инфекции (бронхит, пневмония, пиелонефрит и др.). Постоянным признаком ГГГС, как и ОВГГ, является нарушение иммунитета. Снижается содержание в сыворотке крови γ-глобулинов, иммуноглобулинов (ИГ) классов А и G, в меньшей степени М, секреторных ИГ А и М. Характерны также качественные и количественные изменения В-лимфоцитов: нарушается их способность вырабатывать антитела [1].
Характерной особенностью ГГГС являются атрофия слизистой оболочки (СО) желудка и ворсинок СО тонкой кишки и углубление крипт. Тотальная или субтотальная атрофия СО тонкой кишки напоминает морфологические изменения, свойственные целиакии. Однако в отличие от последней при ГГГС собственная пластинка СО желудка и тонкой кишки обильно инфильтрирована лимфоцитами, образующими скопления в виде лимфатических фолликулов. Количество плазматических клеток резко снижено, иногда они полностью отсутствуют. В криптах часто находят лямблии [2].
Патогенез диареи и СНВ при ГГГС сложный. Хроническая диарея обусловлена бактериальной и паразитарной контаминацией тонкой кишки вследствие дефицита секреторного ИГ А, атрофией энтероцитов и уменьшением абсорбционной поверхности из-за атрофии СО тонкой кишки. В результате в патогенезе диареи при ГГГС имеют значение гиперсекреторные и гиперосмолярные механизмы.
СНВ развивается по причине атрофических изменений СО тонкой кишки, уменьшения ее всасывательной поверхности и снижения энзиматической активности мембранных ферментов. Другой существенной причиной СНВ является избыточный рост микрофлоры в тонкой кишке. Развитие мальабсорбции при ГГГС существенно усугубляет клиническую картину ОВГГ.
Лечение больных ГГГС должно быть направлено на устранение токсического влияния глютена, повышение иммунологической реактивности организма, коррекцию метаболических нарушений, лечение хронической диареи, устранение избыточного бактериального роста в тонкой кишке и лямблиоза, а также сопутствующих очагов инфекции. Одним из основным методов терапии является АГД.
С целью повышения иммунологической реактивности организма больным назначают заместительную терапию препаратами ИГ или ГГ пожизненно.
С целью восстановления эубиоза кишечника, подавления роста микроорганизмов в тонкой кишке проводят терапию последовательными курсами антибактериальных препаратов, пробиотиков и пребиотиков: назначают бисептол, интетрикс и эрсефурил в обычной дозировке в течение 5-7 дней. Такие антибиотики, как цефазолин, кефзол, гентамицин, линкомицин и т.д. применяют внутримышечно для лечения сопутствующих хронических инфекций. При лямблиозе назначают фазижин (тинидазол) по 0,5 г утром натощак в течение 7 дней, затем метронидазол по 0,5 г 4 раза в день 10 дней.
После курсов антибактериальной терапии показано лечение пробиотиками (бифидумбактерин, линекс, бифиформ и др.) и пребиотиками (хилак форте по 60 капель 3 раза в день в течение 1-1,5 мес).
В периоды обострения диареи назначают адсорбенты, вяжущие препараты, обладающие способностью нейтрализовать органические кислоты. К ним относятся белая глина, глюконат кальция, дерматол, танальбин или смекта. Для улучшения процессов пищеварения применяют мезим форте, панкреатин, панзинорм или креон по 1-2 драже 3 раза в день во время еды.
При отсутствии эффекта от перечисленной комплексной терапии назначают короткие курсы кортикостероидов: преднизолон по 20 мг в день или метипред по 16 мг в день в течение 2-3 нед с постепенной отменой препарата.
Приводим одно из клинических наблюдений.
Больная О., 59 лет, поступила в отделение патологии тонкой кишки Центрального научно-исследовательского института гастроэнтерологии (ЦНИИГ) 09.01.01 с жалобами на жидкий, водянистый, обильный стул до 5 раз в сутки (объемом до 500-700 г), боли в животе, рвоту после еды, онемение рук, судороги мышц ног, отеки голеней и стоп.
Больной назначены АГД и симптоматическое лечение. В результате чего ее состояние улучшилось: прибавила в весе 10 кг, частота стула уменьшилась до 3-4 раз в сутки, но сохранялись онемение конечностей и эпизоды лихорадки. Клиническая ремиссия продолжалась около двух лет. В сентябре 2000 г. у больной обострились поносы, стала худеть, появились отеки голеней. Направлена в ЦНИИГ.
Рентгенологическое исследование: складки желудка сглажены, видны увеличенные желудочные ямки, невидимые в норме; все отделы тонкой кишки, включая двенадцатиперстную кишку, гипотоничные, рельеф сохранен.
По сравнению с предыдущим исследованием появились ворсинки, уменьшилась инфильтрация интраэпителиальными лимфоцитами. Количество плазматических клеток остается значительно уменьшенным. Таким образом, подтвержден диагноз ГГГС с СНВ III степени тяжести.
Проведено лечение АГД, ферментными препаратами, последовательными курсами амоксициллина, трихопола, интетрикса, бактисубтила, адсорбентами, витаминами, внутривенными капельными вливаниями физиологического раствора, глюконата кальция (10%), панангина, плазмы.
Состояние улучшилось, частота стула снизилась до 4 раз в день, уменьшились боли в животе, но сохранялись чувство онемения рук и затруднение при ходьбе.
Представленная история болезни демонстрирует редкий случай ГГГС. Течение ее характеризовалось рецидивами воспалительных заболеваний легких, почек, придаточных пазух носа, сочетавшихся с хронической диареей и СНВ III степени тяжести.
Ключевыми критериями диагностики служили выраженное снижение в сыворотке крови концентрации ГГ, ИГ G и А в сыворотке крови, атрофия ворсин с резким уменьшением плазматических клеток в собственной пластинке СО тонкой кишки.
Под влиянием АГД произошло частичное восстановление структуры СО тонкой кишки, что подтверждает связь целиакии с глютеном. В то же время качественных изменений в составе инфильтрата собственной пластинки СО не наступило, что указывает на стабильный характер первичного иммунодефицита.
Заключение
Агаммаглобулинемия – это наследственно обусловленное заболевание, при котором развивается тяжелый первичный иммунодефицит (дефект иммунной защиты организма) с выраженным снижением уровня гамма-глобулинов в крови. Проявляется болезнь обычно в первые месяцы и годы жизни ребенка, когда начинают развиваться повторные бактериальные инфекции: отит, синусит, пневмонии, пиодермии, менингит, сепсис. При обследовании в периферической крови и костном мозге практически отсутствуют сывороточные иммуноглобулины и B-клетки. Лечение агаммаглобулинемии заключается в пожизненной заместительной терапии.
МКБ-10
Общие сведения
Агаммаглобулинемия (наследственная гипогаммаглобулинемия, болезнь Брутона) – врожденный дефект гуморального иммунитета, обусловленный мутациями в геноме клеток, что приводит к недостаточности синтеза B-лимфоцитов. В результате нарушается образование иммуноглобулинов всех классов, и их содержание в крови резко снижается вплоть до полного отсутствия, развивается первичный иммунодефицит. Низкая реактивность иммунной системы приводит к развитию тяжелых повторных гнойно-воспалительных заболеваний ЛОР-органов, бронхов и легких, желудочно-кишечного тракта и мозговых оболочек. Болезнь Брутона встречается исключительно у мальчиков и наблюдается примерно у 1-5 человек из миллиона новорожденных, независимо от расы и этнической группы.
Причины
X-сцепленная форма наследственной агаммаглобулинемии возникает вследствие повреждения одного из генов X-хромосомы (расположен на Xq21.3-22.2). Этот ген ответственен за синтез фермента тирозинкиназы, участвующего в процессе образования и дифференцировки B-клеток. В результате мутаций этого гена и блокировки синтеза брутоновской тирозинкиназы нарушается формирование гуморального иммунитета. При агаммаглобулинемии молодые формы (пре-B-клетки) присутствуют в костном мозге, а их дальнейшая дифференцировка и поступление в кровеносное русло нарушена.
Классификация
Выделяют три формы наследственной агаммаглобулинемии:
Симптомы агаммаглобулинемии
Сниженная реактивность гуморального иммунитета при агаммаглобулинемиях приводит к развитию повторных гнойно-воспалительных заболеваний уже на первом году жизни ребенка (как правило, после прекращения грудного вскармливания – в 6-8 месяцев). При этом защитные антитела от матери в организм ребенка уже не поступают, а свои иммуноглобулины – не вырабатываются. К 3-4 летнему возрасту воспалительные процессы переходят в хроническую форму со склонностью к генерализации. Гнойная инфекция при агаммаглобулинемии может поражать различные органы и системы.
Со стороны ЛОР-органов нередки гнойные гаймориты, этмоидиты, отиты, причем гнойный отит чаще развивается на первом году жизни ребенка, а синуситы – в 3-5 лет. Из заболеваний бронхолегочной системы наблюдаются повторные бронхиты, пневмонии, абсцессы легкого. Часто встречается поражение желудочно-кишечного тракта с упорной диареей (поносами), вызванной хроническим инфекционным энтероколитом (основные возбудители – кампилобактерии, лямблии, ротавирус). На кожных покровах обнаруживается импетиго, микробная экзема, рецидивирующий фурункулез, абсцессы и флегмоны.
Нередким бывает поражение глаз (гнойные конъюнктивиты), полости рта (язвенные стоматиты, гингивиты), костно-мышечной системы (остеомиелиты, гнойные артриты). В целом клиническая картина агаммаглобулинемии характеризуется сочетанием общих симптомов, наблюдаемых при гнойной инфекции (высокая температура тела, озноб, боли в мышцах и головная боль, общая слабость, нарушение сна и аппетита и т. д.) и признаков поражения конкретного органа (кашель, одышка, затруднение носового дыхания, гнойное отделяемое, диарея и т. п.).
Осложнения
Любое инфекционное и соматическое заболевание у больного иммунодефицитом протекает тяжело, длительно и сопровождается осложнениями. Тяжелое течение агаммоглобулинемии может осложняться развитием менингита, вирусного энцефаломиелита, поствакцинального паралитического полиомиелита, сепсиса. На фоне заболевания повышена вероятность развития аутоиммунных и онкологических заболеваний. Гибель пациентов часто наступает от инфекционно-токсического шока.
Диагностика
При клиническом осмотре пациента врачом аллергологом-иммунологом выявляются признаки гнойно-воспалительного поражения того или иного органа (ткани) и симптомы, подтверждающие сниженную реактивность иммунной системы: гипоплазия миндалин, уменьшение периферических лимфатических узлов. Выражены и признаки отставания в физическом развитии ребенка.
Лабораторное исследование крови выявляет выраженное снижение уровня иммуноглобулинов в иммунограмме (IgA и IgM
Дифференциальная диагностика наследственной агаммаглобулинемии проводится с другими первичными и вторичными иммунодефицитными состояниями (генетическими нарушениями, ВИЧ и цитомегаловирусной инфекцией, врожденной краснухой и токсоплазмозом, злокачественными новообразованиями и системными нарушениями, иммунодефицитом вследствие интоксикации лекарственными препаратами и др.).
Лечение агаммаглобулинемии
Необходима пожизненная заместительная терапия антителосодержащими препаратами. Обычно используется введение внутривенного иммуноглобулина, а при его отсутствии – нативной плазмы от здоровых постоянных доноров. При впервые установленном диагнозе агаммаглобулинемии заместительное лечение проводится в режиме насыщения до достижения уровня иммуноглобулина IgG выше 400 мг/дл, после чего при отсутствии активного гнойно-воспалительного процесса в органах и тканях можно переходить к поддерживающей терапии с введением профилактических доз препаратов, содержащих иммуноглобулины.
Любой эпизод бактериальной гнойной инфекции, независимо от локализации воспалительного процесса, требует проведения адекватной антибактериальной терапии, которая выполняется одновременно с заместительным лечением. Чаще при агаммаглобулинемии используются антибактериальные средства из группы цефалоспоринов, аминогликозидов, макролидов, а также антибиотики пенициллинового ряда. Продолжительность лечения при этом в несколько раз превышает стандартную при данном заболевании.
Симптоматическое лечение проводится с учетом конкретного поражения того или иного органа (промывание околоносовых пазух носа антисептиками, выполнение вибрационного массажа грудной клетки и постурального дренажа при бронхитах и пневмониях и т. д.).
Прогноз
Если агаммаглобулинемия обнаружена в раннем возрасте до наступления тяжелых осложнений, и адекватная состоянию пациента заместительная терапия начата своевременно, возможно сохранение нормального образа жизни в течение многих лет. Однако в большинстве случаев диагностика наследственных нарушений гуморального иммунитета осуществляется слишком поздно, когда уже развились необратимые хронические гнойно-воспалительные заболевания органов и систем организма. В этом случае прогноз при агаммаглобулинемии неблагоприятный.
Избыточный бактериальный рост в тонкой кишке у больного общей вариабельной гипогаммаглобулинемией
*Пятилетний импакт фактор РИНЦ за 2020 г.
Отраслевыми стандартами Минздрава дисбактериоз кишечника определен как дифференцироваться вплазматические клетки ипродуцировать основные классы иммуноглобулинов M, AиG. Заболевание возникает влюбом возрасте: удетей после 2 лет, увзрослых— после 16, чаще— втретьем десятилетии жизни. ОВГГГ относится кредким болезням— частота еевобщей популяции составляет 4:106 для мужчин и15:106 для женщин. Клинически этот вид нарушения гуморального иммунитета проявляется повторными бактериальными инфекциями, повышенной частотой аутоиммунных заболеваний излокачественных опухолей [1]. Вполе зрения гастроэнтеролога больные ОВГГГ попадают всвязи срецидивирующей диареей инарушением всасывания втонкой кишке. Хроническая диарея обусловлена обсеменением тонкой кишки разнообразной кишечной микробиотой, включая вирусы, паразиты ипростейшие. Часто обнаруживаются лямблии. Причиной мальабсорбции являются воспалительные изменения слизистой оболочки тонкой кишки (СОТК), вызываемые микрофлорой [2].
Общая вариабельная гипогаммаглобулинемия (ОВГГГ)— наследственно передаваемая неспособность дифференцироваться вплазматические клетки ипродуцировать основные классы иммуноглобулинов M, AиG. Заболевание возникает влюбом возрасте: удетей после 2 лет, увзрослых— после 16, чаще— втретьем десятилетии жизни. ОВГГГ относится кредким болезням— частота еевобщей популяции составляет 4:106 для мужчин и15:106 для женщин. Клинически этот вид нарушения гуморального иммунитета проявляется повторными бактериальными инфекциями, повышенной частотой аутоиммунных заболеваний излокачественных опухолей [1]. Вполе зрения гастроэнтеролога больные ОВГГГ попадают всвязи срецидивирующей диареей инарушением всасывания втонкой кишке. Хроническая диарея обусловлена обсеменением тонкой кишки разнообразной кишечной микробиотой, включая вирусы, паразиты ипростейшие. Часто обнаруживаются лямблии. Причиной мальабсорбции являются воспалительные изменения слизистой оболочки тонкой кишки (СОТК), вызываемые микрофлорой [2].
Ключевые методы диагностики ОВГГГ — исследование иммуноглобулинов в сыворотке крови и оценка макро- и микроскопической картины СОТК. У всех больных в той или иной мере снижена концентрация IgG, IgA и IgM. При рентгенологическом и эндоскопическом исследовании выявляется необычный бугристый рельеф внутренней поверхности тонкой кишки. Он создается скоплениями лимфоцитов в собственной пластинке СОТК, именуемых диффузной узловой лимфоидной гиперплазией (ДУЛГ). Патогномоничным признаком служит характерный клеточный инфильтрат, представленный лимфоцитами с уменьшением или полным отсутствием зрелых лимфоцитов (плазмоцитов) [3]. Для лечения больных ОВГГГ применяют иммуноглобулины (400–600 мг/кг каждые 3–4 нед.), антибактериальные препараты, например, (сульфаметоксазол + триметоприм) по 3–5 мг/кг/сут, а также иммуномодуляторы (полиоксидоний, аминодиоксотетрагидрофталазиндион натрия и др.). Прогноз зависит от степени тяжести инфекций, возникновения аутоиммунных заболеваний и успешности профилактики инфекций [4].
В качестве примера приводим наше наблюдение, демонстрирующее успешную диагностику ОВГГГ с умеренной депрессией гуморального иммунитета, протекающей с преобладанием в клинической картине синдрома избыточного бактериального роста (СИБР) в тонкой кишке, с хорошим ответом на антибактериальную терапию.
Больной Б., 33 года, поступил в отделение патологии кишечника МКНЦ с жалобами на обильный жидкий стул 3 р./сут, боли вокруг пупка, стихающие после стула, иногда тошноту и рвоту съеденной пищей, похудение на 11 кг за 3 мес.
В детстве перенес сальмонеллез и гепатит А. В школьном возрасте часто болел бронхитом, пневмонией и пансинуситом. В ноябре 2013 г. появились подъемы температуры до 38°С, диарея и боли вокруг пупка. При обследовании в поликлинике обращено внимание на множественные участки гиперплазии слизистой оболочки двенадцатиперстной кишки (ДПК) до 0,2 см диаметром. С предположительным диагнозом «болезнь Крона» направлен в МКНЦ.
При поступлении состояние больного удовлетворительное. Правильного телосложения. Рост — 174 см, вес — 89 кг. Кожа и видимые слизистые нормальной окраски. Периферические лимфатические узлы не увеличены. система — без особенностей. Грудная клетка правильной формы. При перкуссии границы легких в пределах нормы, легочный звук ясный. При аускультации дыхание везикулярное с рассеянными сухими хрипами. Пульс — 88 уд./мин. АД — 135/80 мм рт. ст. Границы сердца в норме, тоны ясные, ритм правильный. Язык влажный, не обложен. Живот правильной формы, участвует в акте дыхания, при пальпации мягкий, безболезненный. Печень, селезенка и почки не пальпируются. Мочеиспускание свободное, безболезненное. Симптом поколачивания с обеих сторон отрицательный. Щитовидная железа не увеличена.
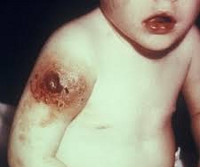
При глубокой антеградной энтероскопии обращал на себя внимание необычный рельеф слизистой оболочки ДПК и тощей кишки, напоминавший картину «булыжной мостовой» за счет многочисленных полушаровидных образований от 0,2 до 0,5 см диаметром (рис. 1), что давало основания для дифференциальной диагностики ДУЛГ с болезнью Крона и полипозом тонкой кишки.
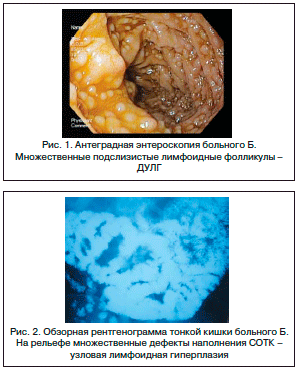
При рентгенологическом исследовании тонкой кишки (после приема 400 мл бариевой взвеси) на всем ее протяжении определялись множественные полиповидные дефекты наполнения до 3–4 мм в диаметре, с четкими контурами. Заключение: рентгенологическая картина ДУЛГ тонкой кишки (рис. 2).
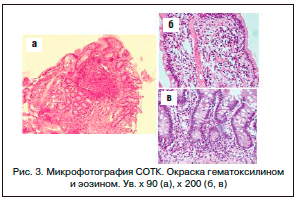
Диагностические трудности помогло разрешить морфологическое исследование биоптатов СОТК (рис. 3). Высота кишечных ворсин снижена, некоторые из них деформированы. Ворсины выстланы клетками высокого цилиндрического эпителия с небольшим количеством бокаловидных клеток. Число межэпителиальных лимфоцитов увеличено. Крипты неглубокие. Соотношение ворсина/крипт = 2/1. В эпителии дна крипт встречаются панетовские клетки. Собственная пластинка отечна и сильно инфильтрирована лимфоцитами с существенной примесью нейтрофилов и эозинофилов. Плазматические клетки в инфильтрате отсутствуют. В собственной пластинке располагаются крупные лимфатические фолликулы со светлыми центрами размножения и гиперплазированные сосуды капиллярного типа, просветы которых часто дилатированы. Заключение: гистологическая картина очагового субатрофического еюнита, вероятно, обусловленная патологией иммунной системы.
Больному выполнено иммунологическое исследование крови: IgG — 487 (норма — 751–1560 мг/дл), IgA — 6,67 (норма — 82–453 мг/дл), IgM — 17,7 (норма — 46–304 мг/дл). Общее количество иммуноглобулинов — 511 мг/дл (5,11 ). Антитела к тканевой трансглютаминазе (АтТГ) не определяются. Дыхательный водородный тест: концентрация Н2 в выдыхаемом воздухе — 237‰ (норма — 15–20‰).
Установлен диагноз: ОВГГГ, энтеропатия, ассоциированная с СИБР в тонкой кишке.
После выписки оставлен под наблюдение врача отделения патологии кишечника МКНЦ с рекомендацией продолжить повторные курсы антибактериальной терапии и лечение иммуномодуляторами в иммунологическом центре.
Позднее установление диагноза у больного (в возрасте 33 лет) обусловлено недостаточным информированием врачей, эндоскопистов, о данной патологии иммунной системы. Поэтому не были учтены многочисленные хронические инфекции, которым больной подвергался с самого раннего детства, не выполнялась биопсия СОТК при наличии ДУЛГ с целью исключения (или подтверждения) ОВГГГ.
Дальнейшая тактика ведения больного должна включать повторные курсы антибактериальной терапии с целью подавления СИБР в тонкой кишке, ежемесячные курсы лечения иммуноглобулином и иммунорегуляторами под наблюдением гастроэнтеролога и специалистов иммунологического центра.
Гипогаммаглобулинемия, болезнь Брутона, аутосомная рецессивная агаммаглобулинемия швейцарского типа
Гипогаммаглобулинемия — это заболевание, возникающее в результате дефицита В-клеток (В-лимфоцитов) в сочетании с уменьшением размера антител — иммуноглобулинов.
Эти антитела не только определяют чужеродные антигены, но и генерируют генетический ответ, который приводит к уничтожению этих антигенов.
Уменьшение количества антител в организме связано с периодическими инфекциями, вызываемыми конкретными формами бактерий. В случае ответа B-лимфоцитов на нарушение качества клеточного иммунитета автоматически регулируется количество бактериальных, грибковых и вирусных инфекций.
Наиболее частые разновидности нарушений, связанных с В-клетками — это непосредственно гипогаммаглобулинемия, а также агаммаглобулинемия (сцепленная с Х-хромосомой, или агаммаглобулинемия Брутона), а также аутосомная рецессивная агаммаглобулинемия швейцарского типа.
Причины, симптомы и методы лечения гипогаммаглобулинемии
В организме существует два вида лимфоцитов. Т-лимфоциты отвечают за уничтожение болезнетворных организмов, В-лимфоциты производят антитела, «налипающие» на атакующие организм патогены, таким образом, Т-лимфоциты и другие защитные клетки накапливаются и атакуют чужеродные организмы.
Антитела – это ключевые белки, ответственные за обнаружение болезнетворных патогенов, понижение их уровня увеличивает восприимчивость к инфекциям. Критическое снижение количества антител вызывает гипогаммаглобулинемию.
Причины
Гипогаммаглобулинемия может быть первичной (то есть, врожденной) или вторичной (приобретенной), вызванной заболеваниями. Первичная форма заболевания может проявиться как при рождении, так и позднее — в более старшем возрасте, несмотря на то, что дефектный ген в организме присутствует с рождения. Большинство случаев гипогаммаглобулинемии развивается после 6-месячного возраста. Случаи заболевания, проявляющиеся на 3-м или 4-м десятилетии жизни, принято считать первичным иммунодефицитом. Их развитие, полагают медики, является результатом еще не установленных генных дефектов.
Симптомы
Большинство пациентов с гипогаммаглобулинемией страдают от рецидивирующих инфекций. Острота проявления симптомов зависит от семейной истории болезни, возраста начала болезни, имеющихся в организме инфекций, состава крови, состояния ЖКТ и опорного аппарата, а также от того, имеются ли у пациента аутоиммунные заболевания или болезни сосудов.
Симптомы гипогаммаглобулинемии:
Лечение
Лечение гипогаммаглобулинемии направлено на устранение основной причины недомогания, заболевание или инфекцию. Пациентам с нарушением функции Т-клеток, тяжелыми расстройствами В-клеток не назначают живые вакцины. Высокие дозы ВВИГ (внутривенного иммуноглобулина) или интератекального иммуноглобулина могут быть полезны пациентам с энтеровирусным менингоэнцефалитом. Показано применение полиэтиленгликоля при дефиците аденозиндезаминазы. Для лечения гранулематозных заболеваний применяют фактор некроза опухолей (ФНО). Успешным методом лечения является и генная терапия, наиболее эффективна она у детей с агаммаглобулинемией Брутона. У взрослых и детей старшего возраста эффективность такого метода лечения ниже.
Аутосомная рецессивная агаммаглобулинемия швейцарского типа
Тяжелый комбинированный иммунодефицит (SCID, ТКИД), или аутосомная рецессивная агаммаглобулинемия швейцарского типа, является наиболее серьезным расстройством из группы человеческих иммунодефицитов. В медицинских источниках и литературе данное заболевание известно также под названием алимфоцитоз. Это заболевание врожденного характера.
Развитие ТКИД сопровождается нарушениям работы гуморальной части иммунной системы человека. Клетки, которые должны производить иммунный ответ, не функционируют. Дети с данным заболеванием подвержены повторяющимся тяжелым инфекциям, задержке роста и ранней смерти.
ТКИД встречается у одного из пятисот тысяч новорожденных. Понятие «тяжелый комбинированный иммунодефицит» объединяет несколько заболеваний, в частности:
Гуморальная система состоит из В-клеток, которые являются единственными клетками в организме, производящими антитела. При ТКИД ни клеточная, ни гуморальная часть иммунной системы не функционирует так, как необходимо.
Причины и симптомы
SCID является наследственным заболеванием. Существует два типа неправильного развития иммунной системы плода. При первом типе генетического нарушения В- и Т-клетки являются дефектными. При втором типе только Т-клетки являются аномальными, но их недостаток влияет на функционирование лимфоцитов.
В течение первых нескольких месяцев жизни ребенок с ТКИД защищен антителами, попавшими в его организм из крови матери. Однако уже в возрасте трех месяцев ребенок с подобным нарушением начинает страдать от грибковой инфекции полости рта (молочницы), хронической диареи, отита и легочных инфекций, в том числе пневмоцистной пневмонии. Ребенок теряет вес, становится очень слабым, и, в конце концов, умирает от условно-патогенной инфекции.
Лечение аутосомной рецессивной агаммаглобулинемии
Тяжелый комбинированный иммунодефицит/агаммаглобулинемию можно лечить с помощью антибиотиков и иммунной сыворотки. Однако такие методы лечения не могут защитить больных, а лишь защищают от инфекций. Постоянная защита невозможна из-за привыкания к антибиотикам и уничтожения полезной микрофлоры ЖКТ. В настоящее время один из немногих эффективных методов лечения этого заболевания — это пересадка костного мозга.
Сцепленная с X-хромосомой агаммаглобулинемия Брутона с дефицитом гормона роста
Что такое агаммаглобулинемия Брутона?
Агаммаглобулинемия Брутона — это заболевание, относящееся к иммунодефицитам, впервые описанное в 1952 году. Огден Брутон обратил внимание на отсутствие иммуноглобулинов у мальчика с пневмонией и другими бактериальными инфекциями. Фактически именно этот тип иммунодефицита является первым официально описанным иммунодефицитом в истории медицины. Брутон был первым специалистом, обеспечившим больному специфическую иммунотерапию — с этой целью он вводил больному иммуноглобулины внутримышечно.
Состояние больного после лечения улучшилось, однако в дальнейшем, уже на четвертом десятилетии жизни, предрасположенность к болезни легких дала о себе знать.
В настоящее время данное заболевание формально называют болезнью Брутона, а фактическое название звучит как «сцепленная с Х-хромосомой агаммаглобулинемия».
Симптомы
Болезнь Брутона проявляется следующими симптомами:
Лечение
Основное лечение заключается во введении в организм больных иммуноглобулина (Ig). Агрессивное лечение бактериальных инфекций антибиотиками помогает предотвратить долгосрочные осложнения. Вирусные вакцины (например, против кори, эпидемического паротита, краснухи) таким больным противопоказаны, как и членам их семей, поскольку могут вызвать развитие инфекции, связанной с этими вакцинами.
Внутривенное введение иммуноглобулина приводит к улучшению клинической картины болезни и уменьшает прогресс серьезных инфекций, таких как пневмония и менингит.
Пациенты, получающие высокие дозы ВВИГ (400-500 мг/кг каждые 3-4 недели) и у которых уровень иммуноглобулина не опускается ниже 500 мг/дл, значительно реже болеют и попадают в больницу. При бронхоэктазах доза иммуноглобулина может быть выше (до 600 мг/кг). Больные менингитом нуждаются в 1000 мг/кг иммуноглобулина из-за гематоэнцефалического барьера.
Пациентам с хроническими инфекциями заболеваний верхних и нижних дыхательных путей и последующими структурными изменениями в этих органах необходимы антибиотики широкого спектра действия. Прием антибиотиков должен сопровождаться физиотерапией грудной клетки и хирургией носовых пазух (при хроническом синусите). Основным препаратом является триметоприм-сульфаметоксазол. Допустимо использование линезолида по отношению к пенициллинорезистентным пневмококкам.
Вспомогательные препараты это: ингаляционные кортикостероиды, антилейкотриеновые препараты, бронхорасширяющие средства.
Хроническая экзема лечится увлажняющими кремами и актуальными стероидами. Рекомендуемые пищевые добавки: поливитамины и минеральные добавки. Необходимо проведение печеночных проб и, при необходимости, соответствующее лечение гепатита С и аутоиммунного гепатита, а также точное определение этиологии диареи.
5 привычек, которые сокращают продолжительность нашей жизни
Склонность человека к мигрени развивается еще в утробе матери
Любовь к черному шоколаду и горькому кофе определяется генами
6 изменений во внешнем виде ногтей, которые укажут на развивающиеся заболевания
Ученые начали разработку мРНК-вакцины против ВИЧ
Обнаружен фермент, который помогает оставаться здоровым физически активным людям