Гнойный плацентит что это
Медицинские интернет-конференции
Языки
Влияние плацентита на течение и исход беременности.
Влияние плацентита на течение и исход беременности
Научный руководитель: к.м.н., доцент Тебелев Б.Г.
ГБОУ ВПО Саратовский ГМУ им. В.И.Разумовского Минздрава РФ
Кафедра акушерства и гинекологии ФПК И ППС
Цель. Изучить влияние воспаления плаценты на течение и исход беременности
Материалы и методы. Проведен ретроспективный анализ 34 историй болезни родильниц с плацентитом.
Собственные исследования.
Половина родильниц встала на учет только во втором триместре, у 80% эндометрий до беременности был не состоятельный из-за НЛФ, которую устраняли дюфастоном, был поврежден урогенитальной инфекцией, абортами, выкидышами, замершими беременностями, прегравидарное лечение не проводилась.
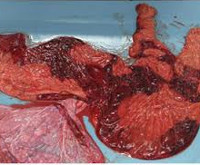
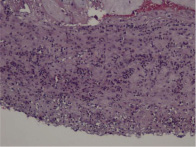
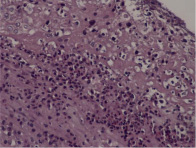
Морфологию плацент поделили на три подгруппы. В первой подгруппе доминируют очаги различной степени зрелости ворсин хориона, с отёчной стромой, с очаговой и диффузной лейкоцитарной инфильтрацией их толщи (виллузит). Во второй сочетаются очаги лейкоцитарной инфильтрации и некроза (гнойно-некротический плацентит), а в третьей воспаление сочетается с артериитом и/или флебитом сосудов плаценты.
Группа №1. 22 (65%)женщины со срочными родами. Беременность в разных триместрах осложнялась угрозой прерывания, вирусной респираторной и половой инфекцией, гестозом, ФПН, ЗВУР. В морфологии плацент отмечены воспалительные очаги у 10(45%), гнойно-некротические у 8(36%), некротические с тромбозом сосудов у 4(19%).
Группа №2. 12 (35%) женщин. У 9 из 11(81%) женщин родам предшествовал преждевременный разрыв околоплодных мембран. В морфологии плацент отмечены изменения: у 6 (54%) воспалительные, у 2(10%) гнойно-некротические, а у 4 (36%)некротические в сочетании с тромбозом сосудов.
Причину отторжения трофобласта и преждевременных родов конкретизировали ретроспективно, сопоставляя морфологию плацент с иммунологическим и бактериологическим поиском возбудителя, с воспалительным ответом женщины лейкоцитарным сдвигом, СРБ, Патогены в посевах не обнаружены. У 40% женщин отмечался умеренный лейкоцитоз, у 19% процентов отмечался сдвиг лейкоцитарной формулы влево. Повышение СРБ отмечалось у 4х женщин(12%)
Выводы.
1. При преждевременных родах в плаценте преобладают воспалительные изменения.
3.Плацентит не всегда острый и бактериальный. Воспаление плаценты имеет иммунное и редко аутоиммунное происхождение, к которому присоединяется инфекция, особенно после разрыва околоплодных мембран.
Гнойный плацентит что это
Основными помехами нормального развития плаценты и эмбриона являются дефицит прогестерона, точечные мутации, алло, аутоиммунные, инфекционные факторы [1, 3, 4, 5]. От инвазии до преждевременных родов на плаценту действуют цитокины, антитела, антигены вне- и внутриклеточной инфекции, а на амнион, коллаген и фибробласты шейки воздействуют молекулы ИЛ-6 и фибронектина плода. При лизисе амниона плацента инфицируется кишечными бактериями, а сокращения матки доставляют эндотоксины не зрелому плоду. Учет конечной патологии плаценты оптимизирует современную тактику [6] родов плодом менее 32 недель, понизит потери детей с низкой массой тела, перинатальную заболеваемость.
Цель. Изучить влияние плацентита на беременность, зрелость и болезни новорожденных.
Материал и характеристика выборки. 34 родильницы с верифицированным воспалением плаценты. Подготовка к беременности не проводилась. Половина родильниц учтена по беременности только со второго триместра. У 80 % эндометрий поврежден урогенитальной инфекцией, абортами, выкидышами, замершими беременностями или лютеиновой недостаточностью. Инфицирование оценивали по цервикальным посевам, ТОРЧ – комплексу; воспалительный ответ учитывали по лейкоцитарной формуле, активности тромбоцитов, гипертермии, белку острой фазы [6,7] воспаления – СРБ, фибриногену, коагулограмме; функцию плаценты учли по УЗИ, КТГ и гипоксии плода. Роженицы поделены на две группы: первая со срочными родами и массой плодов более 2500,0, во вторую отнесены с преждевременными родами массой плодов 1000-1500,0.
Метод. Плаценты, полученные от срочных и преждевременных родов, группировали [2] в три подгруппы с учетом морфологии. В первой, среди ворсин хориона различной степени зрелости, доминировали очаги отёка стромы, слабой и умеренной лейкоцитарной инфильтрации (виллузит). Во второй – сочетались очаги лейкоцитарной инфильтрации и некроза (гнойный и некротический плацентит), в третьей – воспаление сочеталось с инфарктами, артериитом и флебитом сосудов плаценты. В морфологии отмечали якорные ворсины, сопоставляли с осложнениями беременности и родов, со зрелостью и заболеваниями новорожденных, с воспалительными маркерами у женщин и детей. В последних двух подгруппах отмечены острые расстройства кровообращения плода, озноб и гипертермия с началом маточных сокращений или в родах.
Собственные исследования. Группа №1. 22 женщины со срочными родами. В морфологии плацент отмечены воспалительные очаги у 50 %, гнойно – некротические у 30 %, некротические с тромбозом сосудов у 20 %. Только у 5 % женщин при беременности не было осложнений. У половины женщин беременность в разных триместрах осложнялась угрозой прерывания, вирусной респираторной и половой инфекцией, гестозом, ФПН, ЗВУР, что для донашивания потребовало госпитальных лечебных усилий. У большинства женщин роды консервативные, а у 17 % хирургические. Срочные роды обезболивались аналгетиками, не стимулировались, однако у 60 % детей этой группы отмечена церебральная ишемия не смотря на зрелость и отсутствие проблем в родах. Все дети живы и 12 % из них полностью здоровы, но у большинства выявлены сердечнососудистые, энтеральные, дыхательные расстройства с геморрагическим синдром, анемией, отеком диска зрительного нерва. Наиболее тяжелые осложнения у детей возникли при сосудисто-некротических изменениях плаценты. До и после родов инфекционные осложнения предупреждали антибактериальной терапией. У женщин осложнений не было, а у одного ребенка возникла пневмония.
Группа №2. 12 женщин. Токолиз, длительностью 8-10 суток, не предупредил преждевременные роды. В морфологии 90 % плацент отмечены якорные ворсины и изменения: воспалительные у 50 %, у 20 % гнойно – некротические, а у 30 % некротические в сочетании с тромбозом сосудов. Рецидивы угрозы прерывания с первого триместра до преждевременных родов отметили 90 % беременных. Экстремальная и низкая масса тела 50 % незрелых плодов вынуждали максимально прибегать к выжидательной тактике. Разрыв плодных оболочек в родах произошел только у 10 % женщин, а у остальных преждевременно. У большинства безводный период достигал 2-7 суток из-за стремления к увеличению зрелости плодов и глюкокортикоидной подготовки молекул сурфоктанта. У 50 % женщин роды велись на боку с региональной анестезией и КТГ контролем, а у 50 % хирургически из-за незрелой шейки матки. В 1 случае произошла трансплацентарная врожденная передача инфекции незрелому плоду и закончилась летальной пневмонией. У 80 % детей при гнойно-некротических изменениях в плаценте инфекционные заболевания не выявлены, но установлены незрелость, ФПН, геморрагический синдром, анемия. Для инфекции барьерная функция плацент была сохранена, но флебит, артериит, тромбоз и некротические изменения участков плацент привели к изменению кровотока в ее сосудах. У глубоко незрелых плодов возникли системные нарушения циркуляции крови в органах, которые в постнатальном периоде у всех новорожденных этой группы проявились поражением сосудов, кровоизлияниями в желудочки, дыхательными расстройствами, геморрагическим синдром, ишемией и отеком мозга, нарушением ликворогемодинамики. Интенсивная терапия и ИВЛ проводились от 7 до 20 суток.
Обсуждение. При нормальной беременности и отсутствии вредных факторов, воспалительная реакция [8] эндометрия на бластулу стихает, благодаря блокирующим антителам, защищающим антигены отца. Публикации о преждевременных родах, генетической биопсии хориона, ЭКО, выкидышах отмечают латентное воспаление плацентарной площадки в любом сроке беременности. Маркерами иммунного воспаления трофобласта считают: Th1, CD56, APA, ANA, a-ХГЧ, антитела к щитовидной железе, антитела [10] к DQ антигенам, PIBF, MUC1 и др. Бактериальный плацентит активирует: СРБ, фибриноген, прокальцитонин, IL-6. При воспалении сосудов плаценты к маркерам [9] добавляются: д-димеры, фибрин-мономеры, фибриноген, активность и количество тромбоцитов. При целом плодном пузыре маркерами считают фибронектин плода, активности лейкоцитарной эластазы и фагоцитов. Вариабельность не специфических маркеров при беременности затрудняет их использование для диагностики воспаления плаценты. В работе установлено, что при преждевременных родах в 70 % плацент встречаются якорные ворсины хориона, у 80 % в цервикальном канале имеется инфекция: ТОРЧ, бактериальный вагиноз, эпидермальный стафилокок, хламидии. При безводном периоде более 3-4 суток у 60 % женщин к этим патогенам присоединяется колибациллярная флора, что в два раза чаще, чем в группе рожающих в срок. СРБ реагирует на воспаление только у 40 %. Инфекция и маркеры помогают диагностировать плацентит до родов только у половины выборки. У другой половины плацентит верифицирован только морфологически, возбудитель и маркеры не обнаружены. Передача инфекции плоду через плаценту встречалась редко, а геморрагические осложнения отмечены почти у всех доношенных и не доношенных новорожденных. Обширные и тяжелые геморрагические осложнения не доношенных новорожденных требовали длительной интенсивной терапии и ИВЛ, что связано с их незрелостью и повреждением эндотелия бактериальным эндотоксином плаценты.
Выводы
Осложнения у зрелых и незрелых новорожденных зависят от качества диагностики, длительности воспаления плаценты и особенностей плацентации.
Эффективность клинической, лабораторной, инфекционной и УЗИ диагностики плацентита не превышает 40 % от верификации гистологической. Диагноз, частично, маскируют токолитики, антибиотики, дексаметазон.
Плацентит при родах доношенным плодом осложняется у 50 % гипоксией, малым весом, церебральными, дыхательными нарушениями новорожденных, которые редко требуют респираторную поддержку.
Преждевременные роды – повод искать нарушение плацентации в виде якорных ворсин хориона, воспаление плаценты при целом амнионе. Более 15 % плацентит верифицируют при целых водах.
Плацентит на 7-8 сутки безводного периода имеет очаги инфильтрации, инфекции, некрозов, инфарктов, тромбоза, которым иногда сопутствуют СРБ, д – димеры, рост фибриногена, активности тромбоцитов.
Деструкция плаценты и эндотоксины у недоношенного плода создают критическое состояние и гипоксию, а у новорожденного тяжелые геморрагические осложнения ЦНС, требующие интенсивную терапию и длительную респираторную поддержку.
Заключение. Выбор тактики в безводном периоде преждевременных родов до 32 недель должен учитывать маркеры воспаления, инфекции и анамнестические признаки не качественной инвазии. Укороченная шейка матки, отхождение вод и якорные ворсины хориона – признаки нарушенной имплантации и последующего латентного воспаления эндометрия и плаценты с лизисом цервикальной и амниотической соединительной ткани. Безводный период более 3 суток не оправдан. Кесарево сечение обосновано, поскольку предотвращает переход эндотоксинов от инфицированной и разрушающейся плаценты плоду и предупреждает часть геморрагических осложнений у новорожденных, особенно незрелых. Важно улучшать диагностику воспаления маркерами, помощь плоду и готовить женщин к беременности.
Плацентит
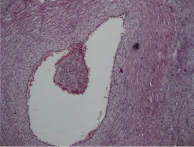
Плацентит – это воспаление плаценты, которое возникает под действием неинфекционных и инфекционных факторов. Патология плаценты может проявиться на любом сроке, симптомы зависят от выраженности воспаления. Плацентит приводит к дисфункции фето-плацентарного комплекса, его исходом становятся плацентарная недостаточность, задержка развития плода, внутриутробное инфицирование. Значительно возрастает риск преждевременных родов и гибели новорожденного. Для диагностики используется УЗИ, которое позволяет заметить нарушение структуры плаценты, плацентарного кровотока. Лечение плацентита проводится антибиотиками, а также препаратами, улучшающими функцию плаценты.
МКБ-10
Общие сведения
Плацентит – инфекционно-воспалительное заболевание, чаще всего является результатом восходящего распространения инфекции. У 98% женщин приводит к неблагоприятному течению беременности и развитию осложнений. Угроза прерывания, ассоциированная с плацентитом, отмечается у 76% беременных. В большинстве случаев плод страдает от внутриутробной гипоксии, 9% детей рождается с признаками гипотрофии. Инфекция вызывает несвоевременное излитие вод у 38% беременных, у трети женщин это приводит к аномалиям родовой деятельности. Риск внутриутробного инфицирования существует у 6% детей, которые развиваются в условиях плацентита.
Причины плацентита
У всех беременных наблюдается физиологическая иммуносупрессия, вызванная повышением выработки прогестерона. При наличии очагов хронической или острой инфекции она может распространиться на плаценту. Чаще всего инфицирование происходит восходящим путем из влагалища через шейку матки. К плацентиту приводят различные виды микроорганизмов и действие неинфекционных факторов:
Патогенез
Воспаление может возникать в различных слоях плаценты. Воспалительная реакция сопровождается миграцией лейкоцитов и инфильтрацией тканей, нарушением кровообращения, которое вызвано микротромбозами межворсинчатого пространства, микроинфарктами, ишемией концевых ворсин. Также определяется полнокровие и отек стромы. В зависимости от вовлеченного слоя различают следующие формы плацентита:
Плацентит не всегда приводит к инфицированию плода, но может сказаться на состоянии эндометрия после родов и ухудшить прогнозы для следующих беременностей. Одновременно внутриутробная инфекция у ребенка может протекать без признаков плацентита. Такой вариант течения наблюдается при некоторых вирусных инфекциях. Для каждого типа возбудителя характерна своя гистологическая картина.
Симптомы плацентита
Патология может быть следствием острой либо хронической инфекции. У нее нет специфических проявлений, при латентном течении симптомы могут вовсе отсутствовать. Учитывая восходящий путь инфицирования, беременную могут беспокоить вагинальные выделения. Они могут быть белыми, с желтоватым или сероватым оттенком, с неприятным запахом или без него. При остром течении вагинита из-за близкого расположения мочеиспускательного канала появляются дизурические расстройства. Женщина жалуется на неприятные ощущения во время мочеиспускания, походы в туалет становятся чаще. Выделения сопровождаются зудом и жжением, покраснением половых губ.
Боль внизу живота является следствием воспаления. При плацентите и возникновении угрозы преждевременных родов боли появляются в нижней части матки. Они тянущие, ноющие, могут отдавать в промежность или поясницу. На появление угрозы прерывания беременности указывает тонус матки, схваткообразная боль. Плод реагирует на недостаток кислорода увеличением двигательной активности или снижением количества шевелений. Настороженность должны вызывать подтекание околоплодных вод или их дородовое излитие. Это повод срочно обратиться за медицинской помощью в гинекологическое отделение на сроке до 22 недель, а на более позднем сроке – в роддом.
Осложнения
Плацентит вызывает осложнения беременности, некоторых из них становятся показанием для досрочного родоразрешения. У каждой 5-ой беременной отмечается преждевременное излитие околоплодных вод. Для беременных с плацентитом характерна плацентарная недостаточность. При декомпенсации состояния у плода развивается острая гипоксия, которая может привести к антенатальной гибели или тяжелым повреждениям центральной нервной системы ребенка. Чем раньше возник плацентит, тем выше вероятность тяжелых осложнений. Течение беременности может осложниться гестозом, внутриутробной инфекцией ребенка, преждевременными родами.
Диагностика
При нарушении самочувствия, боли в животе, появлении выделений из половых путей беременной необходимо обратиться к врачу акушеру-гинекологу, у которого она состоит на учете. Объем диагностических процедур подбирается индивидуально, опираясь на клинические проявления, данные анамнеза и предыдущих исследований. Базовая диагностика плацентита проводится неинвазивными инструментальными методами:
Подтверждается плацентит после родов. Плодное место с оболочками и пуповиной отправляется на гистологическое исследование. По его результатам можно предположить тип инфекции, если обследование не проводилось во время беременности. Для нормального восстановления в послеродовом периоде и профилактики эндометрита назначается лечение.
Лечение плацентита
Женщина с плацентитом госпитализируется для проведения качественного обследования, лечения и выбора акушерской тактики. Консервативная терапия оправдана при недоношенной беременности и признаках незрелого плода, но при сохранении его нормальной гемодинамики. При некупирующейся острой гипоксии плода и в других тяжелых случаях показано досрочное родоразрешение путем кесарева сечения. При плацентите проводится:
Прогноз и профилактика
При плацентите прогноз зависит от срока развития воспаления и способностей организма компенсировать сосудистые нарушения. Для плода плацентраная недостаточность увеличивает риск задержки развития, внутриутробного инфицирования и гипоксии, которая может завершиться внутриутробной гибелью. Профилактика плацентита заключается в прегравидарной подготовке, своевременном лечении хронических воспалительных процессов половых органов. Мазки на чистоту влагалища, которые берутся при постановке на учет, позволяют вовремя заметить воспалительные изменения, провести дополнительное обследование и лечение.
Гнойный плацентит что это
Плацента – важный орган, основное предназначение которого – снабжение кислородом и питательными веществами развивающийся плод во время беременности. При физиологическом течении беременности плацента также обеспечивает иммунологическую толерантность организма матери по отношению к плоду, предотвращая развитие аутоиммунных реакций, являясь своеобразной «подушкой безопасности», а также выполняет эндокринную функцию, синтезируя те гормоны, которые эндокринная система плода не способна синтезировать [1, 2]. Для иммунной системы матери во время беременности баланс между реактивностью и иммуносупрессией склоняется в сторону реактивности. Однако не менее важна барьерная роль плаценты в защите плода от различных микроорганизмов. Локальные иммунные реакции могут потенциально активировать материнский иммунный ответ, что также способствует проникновению патогенных микроорганизмов в амниотическую жидкость, ткань плаценты, проникновение их в ткани, ииммунокомпетентные органы плода. Иммунная система плода ещё незрелая, не готова адекватно распознать болезнетворные бактерии и их эллиминировать. В качестве антигенов могут выступать как микроорганизмы, так и аллоантигены плода, антигены плаценты, аутоантигены матери, которые становятся мишенью для материнского организма. Независимо от их этиологии, в результате сбоя иммунной системы эти факторы могут привести к неблагоприятным результатам, таким как внутриутробная гибель плода, преждевременная роды, задержка роста плода, нарушение развития и дифференцировки внутренних органов.
Одно из первых мест в структуре акушерской патологии занимают инфекционные и воспалительные заболевания беременной, часто скрыто протекающие, достигающие 15–30 % всех преждевременных родов (ПР). Хориоамнионит (ХА) встречается примерно у 15 % беременных [3]. Распространенность ХО составляет в 3–5 % плацент доношенного срока геcтации из которых в 94 % проявляется на 21–24 неделе беременности [4]. В соответствии с современной международной морфологической классификацией повреждений плаценты, разработанной Амстердамской рабочей группой (Amsterdam Placenta Working Group) (2014) [5], воспалительные изменения плаценты делятся на изменения, обусловленные инфекционными агентами и связанные с асептическим воспалением, опосредованные иммунными процессами. В свою очередь воспаление, вызванное инфекционными факторами, бывает с преобладанием воспалительного ответа со стороны матери (преимущественно острым (например, воспаление амниотических оболочек – острый хориамнионит, или со стороны плода (васкулиты сосудов пуповины – фунизит), поражения ворсин плаценты и межворсинчатого пространства – виллиты и интервиллиты), а также децидуальной пластинки, граничащей с полостью матки – децидуит. Воспаление, обусловленное иммунопатологическими процессами, чаще бывает хроническим и представлено хроническим виллитом и хроническим ХА, хроническим децидуитом с инфильтрацией лимфоцитами и плазмоцитами, а также к хроническому воспалению относятся Т-клеточный эозинофильный фетальный васкулит, хронический гистиоцитарный интервиллузит.
Взаимосвязь инфекции влагалища и цервикального канала с ХА, разрывами плодных оболочек и преждевременными родами показано рядом авторов [6]. Однако соответствие гистологических критериев, клинических признаков воспаления и выявление возбудителя (выявленного посредством ПЦР) происходит менее чем в половине случаев [7].
Как и все органы, плацента и плацентарная площадка содержат популяции резидентных воспалительных клеток, которые, как считается, играют решающую роль в развитии и функционировании плаценты. К наиболее важным относятся популяции больших зернистых (гранулярных) лимфоцитов в децидуализированном эндометрии и клетки Гофбауэра стромы ворсин. Первые состоят преимущественно из натуральных киллеров и играют роль в трансформации и ремоделировании спиральных артерий [8], имеют тенденцию к образованию кластеров около желёз эндометрия, и материнских сосудов, но это не сопровождается повреждением тканей. Клетки Гофбауэра представляют собой тканевые макрофаги и, как полагают, принимают участие в васкуляризации ворсин плаценты и защите плода от патогенов и других потенциально опасных медиаторов, которые могут нарушить гемоплацентарный барьер [9], а также играют роль в ангиогенезе, который проявляется на этапе незрелых промежуточных ворсин, когда присутствуют клетки стромы, формирующие пространство будущего кровеносного сосуда с образованием так называемых стромальных каналов, в просвете которых циркулируют макрофаги [10], что особенно важно на ранних сроках гестации. Клетки Гофбауэра обычно по внешнему виду выглядят одинаковыми и, как правило, равномерно распределены в строме ворсин и больше представлены в плаценте на ранних сроках. Выявление в ткани плаценты и матки нейтрофилов, эозинофилов, В- и Т-лимфоцитов, а особенно плазмоцитов составляет основу для патологического воспаления ткани плаценты. Острый воспалительный ответ с преобладанием нейтрофилов наблюдается преимущественно в амниотических оболочках, при ХА, и выявляется примерно в 20 % всех плацент [11]. Хронический хориоамнионит (ХХА) воспаление с преобладанием лимфоцитов встречается в 5–15 % плацент нередко связано инфекцией, но может быть опосредовано аутоиммунными заболеваниями или аллоиммунными реакциями против последствий предыдущих инфекций или инфекций, вызванных еще нераспознанными патогенами, хотя этот вопрос требует дальнейшего изучения.
Хориамниониты являются отражением большого количества факторов риска, при котором гистологические критерии не всегда полно отражают клиническую картину. ХА часто сочетаются с воспалением других частей плацентарного диска (децидуальной оболочки (децидуит), ворсин плаценты (виллит), пупочного канатика (фунизит).
Гистологически острый хориоамнионит (ОХА) определяется как материнская нейтрофильная реакция на бактериальную инфекцию с или без сопутствующего ответа со стороны плода. ХА традиционно имеет место две основных классификации: гистологическую базирующуюся на воспалительной инфильтрации плодных оболочек (нейтрофилами, макрофагами и Т-лимфоцитами). Вторая основана на клинической манифестации локального и системного воспаления:
1) температура более 37,5 °С;
2) наличие болезненности при пальпации матки;
3) боли внизу живота;
4) неприятный запах при влагалищном исследовании;
5) тахикардия у беременной (более 100 ударов в минуту);
6) тахикардия у плода (более 160 ударов в минуту);
7) повышение лейкоцитов крови матери более 15 000 тыс/мм3) [7, 12].
Кроме того, повышение температуры тела может быть ассоциировано также с эпидуральной анальгезией, что затрудняет дифференциальную диагностику [7].
Наибольшим фактором риска в развитии острого ОХА являются микроорганизмы, присутствующие в цервико-влагалищном тракте, нарушение нормальной микрофлоры влагалища, истмико-цервикальная недостаточность, преждевременное раскрытие шейки матки и разрыв плодных оболочек, а также длительный безводный период [7]. Менее распространенными путями заражения, которые нередко не учитываются, но которые не являются менее важными, являются гематогенный путь распространения, например инфекция периодонта, а также патогенная микрофлора органов малого таза (например, инфекция мочевого пузыря, фаллопиевых труб, прямой кишки) может привести к ОХА, после проникновения микроорганизмов в ткань плаценты.
При гистологически подтвержденном ОХА анаэробные бактерии при микробиологическом исследовании выделяются примерно в 50 % случаев. В меньшем проценте наблюдений ОХА ассоциированы с более высокопатогенными организмами, представляющими угрозу жизни и здоровья плода (например, стрептококки, грамотрицательные бациллы и стафилококки), обладающие повышенной способностью к проникновению в организм плода. При ХО, обусловленных этими микрорганизмами, имеет место повышенный риск к развитию внутриутробной инфекции, а также заболеваниям неинфекционной природы, например образование очагов ишемического повреждения головного мозга, которые бывают вызваны Escherichia coli [13]. Распространенность ХО с подтверждёнными гистологическими признаками снижается в зависимости от гестационного возраста: выявляется до 70 % в плаценте от младенцев, рожденных на сроке до 30 недель гестации и приблизительно в 10 % у доношенных новорожденных [11]. Считается, что 25 % всех преждевременных родов обусловлены ХО [14], из которых ХО, ассоциированные с интактными плодными оболочками (без их разрыва) до 45 %, из них только 14–21 % случаев с гистологически подтверждённым ХО. Случаи с преждевременным разрывом плодных оболочек) (ПРО) [14] составляют 30 % наблюдений, из них только от 26 % до 50 % случаев гистологически подтверждённого ХО. Менее 5 % случаев хориоамнионита протекают наиболее тяжело, имеют угрозу для здоровья матери и плода.
Наряду с этим обнаружены микроорганизмы в ткани плаценты, которые могут не вызывать воспалительную реакцию (асимптоматическое течение ХО, однако нередко приводящие к ПРО и преждевременным родам [15]. В исследовании Hillier (1988) до 65 % наблюдений с гистологически подтверждённым ХО из плацент была выделена Ureaplasma urealyticum. Более того, данный микроорганизм был ассоциирован с другими микробными агентами и определялся более, чем в половине наблюдений [16]. Подтверждением этому служит колонизация U. urealyticum дыхательных путей плода, связанная с увеличением хронических заболеваний легких у недоношенных детей [17].
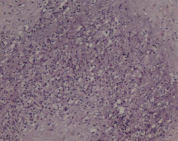
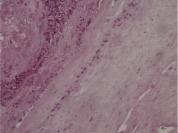
Гистологические критерии острого хориоамнионита. Классификация. Согласно Амстердамской классификации поражений плаценты выделяют материнский и фетальный воспалительный ответ. К материнскому воспалительному ответу относятся поражения плодных оболочек, к фетальному ответу – поражения сосудов пуповины, сосудов стволовых ворсин, васкулиты хориальной пластинки (рис. 1, А–Е).
Рис. 1. Воспалительные изменения хориальной пластинки и плодных оболочек (окраска гем и эоз). А–Б – Инфильтрация хориальной пластинки ПЯЛ, присутствуют лимфоциты, макрофаги и единичные плазмоциты. А – х100, Б – х200. В–Е – Острый хориоамнионит 2–3 стадии, 2 степени В – х100, Г – х200, Д – х100. Е – х400
В материнском воспалительном ответе выделяют стадии, отражающие прогрессию заболевания.
Стадия 1. (острый субхориоамнионит/ранний острый хориоамнионит) = очаговое и диффузное скопление полиморфно-ядерных лейкоцитов (ПЯЛ) в и под хориальной пластинкой и/или в и под амниотической базальной мембраной (отмечаются несколько разбросанных ПЯЛ в менее чем в половине толщины хориальной пластинки и / или в соединительной ткани мембранозной части хориальной пластинки). Воспалительная инфильтрация отмечается лишь под хориальной пластинкой, в последующем нейтрофилы инфильтрируют также как плодный фибриноид под хориальной пластинкой, так и границу децидуальной и хориальной пластинок (острый субхорионит), а затем вовлекаются децидуальные посткапиллярные венулы (острый хорионит). Эта стадия длится обычно менее 12 часов.
Стадия 2. Острый хориоамнионит. Количество нейтрофилов увеличено в хориальной пластинке и / или мембранозной части хориальной пластинке оболочках амниона. Стадия длится в течение 12–24 часов
Стадия 3. Некротический хориоамнионит. Отмечается распад ПЯЛ (кариорексис), утолщение амниотической базальной мембраны, которая становится эозинофильной, присутствует также дистрофия и слущивание амниотического эпителия. После длительной экспозиции инфекции (>48 часов) нейтрофилы подвергаются кариорексису, слущенные амниотические эпителиальные клетки проникают в амниотическую жидкость, что является следствием появления ярко-красной полосы фибриноида на базальной мембране амниона. Это обнаруживается в 50 % случаев и является признаком некротического хориоамнионита.
Спустя несколько дней или недель острые воспалительные инфильтраты стихают и смешанная нейтрофильно-гистиоцитарная инфильтрация сохраняется только в верхних слоях хориона. Этот вариант ХО был назван подострым ХО, который коррелирует с увеличением заболеваемости хроническими заболеваниями легких новорожденных [18]. Важно, что наличие субхориальных микроабсцессов на любой стадии инфекции является проявлением повышенного риска развития тяжелых осложнений, включая сепсис [19].
Степень хориоамнионита (отражает выраженность воспалительных реакций)
Степень 1 (умеренно выраженная): присутствуют единичные или мелкие скопления материнских ПЯЛ, диффузно инфильтрирующих амниотические оболочки, хориальную пластинку и/или расположенный под хориальной пластинкой плодный фибриноид.
Степень 2 (тяжёлая): присутствие трех или более микроабсцессов в хориальной пластинке (не менее 10–20 ПЯЛ), а также между хориальной и децидуальной пластинками в экстраплацентарных оболочках и / или под хориальной пластинкой плацентарного диска. Поражение может иметь вид непрерывной линии из более 10 ПЯЛ, занимающую более половины плодного фибриноида, расположенного под хориальной пластинкой или один оборот в «ролле» плодных оболочек. Хронический (или подострый) ХО диагностируется на основании более выраженной инфильтрации мононуклеарами (обычно макрофагами), в хориальной пластинке (чаще под амнионом). В ряде случаев макрофаги присутствуют как реакция на отложение экзогенных пигментов (например, мекония или гемосидерина).
Фетальный воспалительный ответ
Стадии, отражающие прогрессию заболевания.
Стадия 1 (васкулит хориальных сосудов / флебит пупочной вены): выявление ПЯЛ в стенке сосудов хориальной пластинки или стенке пупочной вены. Проникновение ПЯЛ в вартонов студень допустимо при этой стадии, но пока отсутствуют микроабсцессы и концентрические полосы, окружающие пупочную вену.
Фетальный воспалительный ответ, обусловленной инфильтрацией ПЯЛ на бактериальную инфекцию при беременности, может развиться с 15 недели гестации, но значительно чаще имеет место при доношенных сроках беременности [20]. Фетальный воспалительный ответ начинается с сосудов хориона или пупочной вены, практически всегда сопровождается материнским ответом в виде острого (подострого) хориоамнионита. Острый васкулит фетальных сосудов как изолированное состояние является дискутабельным вопросом.
Стадия 2 (васкулит пупочных сосудов): нейтрофилы присутствуют в стенке одной или обеих пупочных артерий и в пупочной вене. Наличие ПЯЛ в вартоновом студне допустимо при отсутствии микроабсцессов, и концентрических полос, окружающих пупочные сосуды. Фетальные воспалительные реакции в стенке пупочных артерий (пупочный артериит) возникают позже, их развитие коррелирует с повышенным уровнем циркулирующих цитокинов в пупочной крови).
Впоследствии ПЯЛ могут мигрировать в вартонов студень пуповины, где они образуют полоску, выявляемую при гистологическом исследовании, окружающие фетальные сосуды (стадия 3).
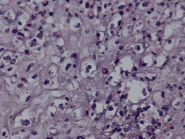
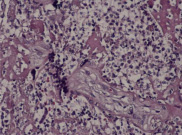
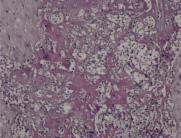
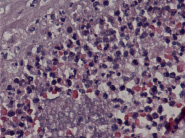
Стадия 3 (некротический фунизит или концентрический периваскулит пупочных сосудов): диагностируют на основании присутствия ПЯЛ, клеточного детрита, эозинофильных преципитатов, и/ или отложений солей кальция, которые визуализируются в виде полоски или ободка, окружающих один или все пупочные сосуды (в большинстве случаев наиболее тяжёлые изменения присутствуют на участках близким к периферии пуповины). Полосу или ободок, который образуют ПЯЛ некоторые авторы называют некротический или субнекротический фунизит и связывают с отложением иммунных комплексов, состоящих из бактериального антигена амниотических оболочек и материнских иммуноглобулинов, диффундирующих из пупочных сосудов [21]. Через несколько недель клетки и эти аркуатные структуры могут исчезнуть, и смениться на эозинофильнуые преципитаты, микрокальцинаты, при этом нередко вовлекаются хориальные сосуды мелкого диаметра (рис. 2, А–Г).
Рис. 2. Воспалительные изменения пуповины и децидуальной пластинки (окраска гем. и эоз.). А–Г – Воспалительные изменения пуповины (воспалительная инфильтрация вартонова студня лимфоцитами, макрофагами и ПЯЛ) А – х40, Б – х100, В – х200, Г – х200. Д–Е – Воспалительные изменения базальной пластинки (очаговая и рассеянная инфильтрация преимущественно ПЯЛ), Д – х100, Е – х200
Степень, отражающая интенсивность воспаления фетального воспалительного ответа
Степень 1 (умеренно выраженная): разбросанные инфильтраты, образованные ПЯЛ, расположены субэндотелиально или стенках хориальных или пупочных сосудов.
Степень 2 (тяжелая): стенки сосудов хориальной пластинки (или сосудов пуповины) с выраженной инфильтрацией ПЯЛ и отёком, наличием повреждения гладкомышечной стенки сосудов на стороне, близкой к амниотической полости. Кроме того, часто отмечаются тромбозы фетальных сосудов (свежие тромбы в сосудах хориальной пластинки или пуповины). Все эти признаки являются отражением картины фетального воспалительного ответа – англ. fetal inflammatory response syndrome (FIRS) – по аналогии с SIRS (англ. Systemic inflammatory response syndrome). Важно отметить, что воспалительный ответ плода не всегда свидетельствует о фетальной инфекции, но является показателем иммунной активации, которая ассоциируется с высокими уровнями цитокинов плода, что приводит к увеличению риска повреждений головного мозга и заболеваний лёгких плода [22–24]. При 2 степени тяжести васкулиты хориальных сосудов ассоциированы с повышенным риском ишемического повреждения головного мозга плода; тромбы в их просвете являются также дополнительном фактором риска [25].
Другие специфические изменения
К другим специфическим изменениям плаценты, ассоциированным с ОХА, относится: периферический фунизит, диагностируемый на основании наличия мелкоточечных абсцессов с участками инфильтрации ПЯЛ на внешней стороне пуповины; острый виллит: присутствие ПЯЛ в строме ворсин и /или под трофобластом; острый интервиллузит / внутриворсинчатый абсцесс – ПЯЛ располагаются в пределах периворсинчатого фибриноида или периворсинчатого пространства, а также в ряде случаев отмечается инфильтрация ПЯЛ децидуальной пластинки (острый децидуит) (рис. 2, Д–Е).
Другие воспалительные изменения, ассоциированные с ОХА, особенно на ранних сроках гестации, включают лимфоплазматический децидуит, и свежие ретроплацентарные гематомы вызывающие диагностическую сложность из-за интенсивной инфильтрации ПЯЛ. В некоторых случаях ОХА могут быть вызваны специфическими микроорганизмами. Так, ОХА с острым интервиллузитом и образованием межворсинчатого абсцесса (так называемые септические инфаркты) чаще всего ассоциируются с Listeria monocytogenes [26, 27]. ОХА с ассоциации с периферическими абсцессами пуповины наиболее часты при инфекции Candida, и часто связаны с преждевременным разрывом плодных оболочек, истмико-цервикальной недостаточностью, а также присутствием внутриматочной спирали или вагинальных колец [28]. ОХА в сочетании с острым виллитом наблюдаются при врождённом бактериальном сепсисе, обычно вызванном стрептококками или грамотрицательными бактериями, в частности E. coli. ОХА в ассоциации с очаговым острым интервиллузитом и периворсинчатым отложением плодного фибриноида могут сочетаться с материнским сепсисом, нередко вызываемого стрептококками и грамотрицательной флорой [29]. Гибель плода редко является следствием непосредственно ОХА, гораздо чаще это происходит при развитии врождённого сепсиса. Преждевременные роды, связанные с ХО, имеют высокий риск рецидива. К возможным причинам этого относят наличие дефектов матки, подострого хронического эндометрита, вызванного стрептококками группы В, бактериального вагиноза, истмико-цервикальной недостаточности.
Изолированный фетальный васкулит может поражать артерии и вены пуповины, хориальной пластинки или крупных стволовых ворсин. Хотя обычно сопровождается острым хориоамнионитом или хроническим виллитом, эти повреждения иногда могут наблюдаться изолированно. Поражения с инфильтрацией ПЯЛ или смешанной воспалительной инфильтрацией (с примесью ПЯЛ) и/или эозинофилами чаще всего обусловлены воздействием мекония, более часто встречаются в стенке пупочной вены [30]. Наблюдения с лимфоцитарной или смешанной лимфоцитарной / эозинофильной инфильтрацией (эозинофильный Т-клеточный хорионический васкулит) имеют место в хориальных или крупных сосудах стволовых ворсин, но данный вопрос является недостаточно изученным [31, 32].
Хронический хориоамнионит (ХХ) встречается в двух различных клинико-патологических вариантах [33]: подострый (хронический) хориоамнионит, является преимущественно затяжной формой инфекционного хориоамнионита и связан чаще с микроорганизмами с низкой патогенностью, такими как микоплазма или вагинальные анааэробы [18]. Один из морфологических вариантов представлен преобладающей воспалительной инфильтрацией гистиоцитами, мононуклеарами с примесью единичных нейтрофилов под амнионом. Этот вариант сочетается с экстремально низкой массой тела детей при рождении и является одной из причин преждевременных родов, часто сочетается с хроническим виллитом. Второй морфологический вариант диагностируется как преобладание лимфоцитарной инфильтрации, по выявленной локализации в хорионе в средней части амниона в виде полос.
Хронический децидуит (ДХ) диагностируется на основании обнаружения инфильтрации мононуклеарами и/или с наличием плазмоцитов [34]. В ряде случаев обнаруживается также большое количество эозинофилов.
Есть предположение, что ДХ может быть результатом эндометритов низкой степени активности и подострых эндометритов, вызванных микоплазмой или другими микроорганизмами с низкой патогенностью, что может быть связано с нарушением микрофлоры влагалища [35]. Это может приводить к преждевременным родам во втором и третьем триместрах. ДХ часто сочетаются с ХО.
Известно, что при отсутствии лечения хронический эндометрит – фактор высокого риска при невынашивании беременности. Кроме того, хронические виллиты сочетаются в 25–30 % случаев с лимфоплазмоцитоидными хроническими децидуитами.
В этих случаях ДХ могут представлять собой неинфекционный воспалительный материнский ответ на аутоантигены или аллоантигены плода [36]. Пациенты с ДХ часто имеют высокий процент аутоиммунных заболеваний различного генеза [37]. Общая перинатальная смертность высока. Антенатальная гибель плода, привычное невынашивание беременности также часто ассоциированы с ДХ. У выживших младенцев нередко отмечается задержка роста и развития. Данное состояние следует также отличать от морфологической картины, при инфицировании Plasmodium falciparum во время беременности.
Децидуальный васкулит/периваскулит диагностируется по наличию выраженности воспалительной инфильтрации вокруг артериол децидуальной пластинки, включая децидуальную пластинку плодных оболочек [3, 38, 39]. Это поражение наиболее часто наблюдается у пациентов с преэклампсией, задержкой развития плода, при невынашивании беременности. Децидуальный васкулит может быть как изолированным, так и сочетаться с острым атерозом и гипертрофией стенок сосудов [39].
Хотя интраамниотическая инфекция обычно считается причиной острого хориоамнионита и фунизита, а также причиной преждевременного разрыва плодных оболочек, однако данные ряда авторов свидетельствуют о том, что «асептическое» внутриамниотическое воспаление (без выявленного микробного агента), может происходить в отсутствии видимых микроорганизмов, и повреждающее действие связано с молекулами повреждения или молекулы «опасности» (DAMP – от англ. Damage-associated molecular pattern или danger-associated molecular patterns), а также интерлейкинами, хемокинами и другими «сигналами опасности». В контексте внутриамниотической инфекции интерлейкины и хемокины (например, интерлейкин-8 и хемотаксические факторы гранулоцитов) создают градиент, который способствует миграции нейтрофилов из системы кровообращения матери или плода в плодные оболочки или пуповину, соответственно. Молекулы повреждения, которые высвобождаются в при повреждении и гибели клеток также в свою очередь могут способствовать высвобождению хемокинов и нейтрофилов [40].
Таким образом, восходящий тип инфекции, обусловленный воспалительным ответом, вызываемый микробными агентами вовлекает 2 типа иммунного ответа: (1) материнский, с инфильтрацией воспалительной инфильтрации (прежде всего ПЯЛ) хориоамниона и хориальной пластинки; и (2) фетальный, определяемый как воспалительная инфильтрация (преимущественно ПЯЛ) вартонова студня, стенок крупных сосудов хориальной пластинки и сосудов пуповины.