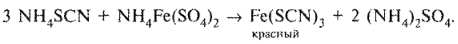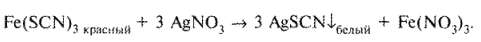лекарственное средство растворимо как в кислотах так и в щелочах
Производные пиримидино-тиазола, фенотиазина. Анализ
» data-shape=»round» data-use-links data-color-scheme=»normal» data-direction=»horizontal» data-services=»messenger,vkontakte,facebook,odnoklassniki,telegram,twitter,viber,whatsapp,moimir,lj,blogger»>
Производные бензодиазепина, пиримидино-тиазола. Анализ
Глава 17. Анализ производных пиримидино-тиазола, птеридина, изоаллоксазина, фенотиазина и бензодиазепина
ЛС, производные изучаемых групп гетероциклических соединений, широко применяются в медицине. Среди них лекарства природного происхождения (витамины) и синтетические (производные фенотиазина и бензодиазепина).
Производные фенотиазина применяются в качестве нейролептических, антигистаминных, коронарорасширяющих и антиаритмических средств, а производные бензодиазепина — в качестве седативных.
ПРОИЗВОДНЫЕ ПИРИМИДИНО-ТИАЗОЛА
Термин «витамин» (буквально «амин жизни») предложен Функом, выделившим фракцию из водного экстракта рисовых отрубей, обладающую выраженными основными свойствами (1911 — 1912). В 1934 г. Вильямс из 1 т рисовых отрубей выделил несколько граммов витамина В1 а в 1936 г. доказал его строение.
Организм животных и человека нуждается в поступлении витамина В1 (тиамина) извне с продуктами питания. Тиамин содержится в отрубях хлебных злаков (особенно в рисовых отрубях), дрожжах.
Тиамин, всасываясь из кишечника, фосфорилируется и превращается в тиамин-пирофосфат (дифосфат). В этой форме он является коферментом декарбоксилаз, участвующих в окислительном декарбоксилировании кетокислот (пировиноградной, α-кетоглугаторовой). Недостаток тиамина ведет к нарушению углеводного обмена, а затем и к другим нарушениям метаболизма (в мышечных тканях накапливаются пировиноградная и молочная кислота), функции нервной системы (проявляются полиневритом и мышечной слабостью), к заболеванию бери-бери, парезам, параличам, кожной патологии.
Применяют препараты тиамина при невритах, невралгиях, радикулите, кожных заболеваниях, а также для профилактики и лечения авитаминоза В1,
Потребность человека в тиамине составляет примерно 1 мг в день.
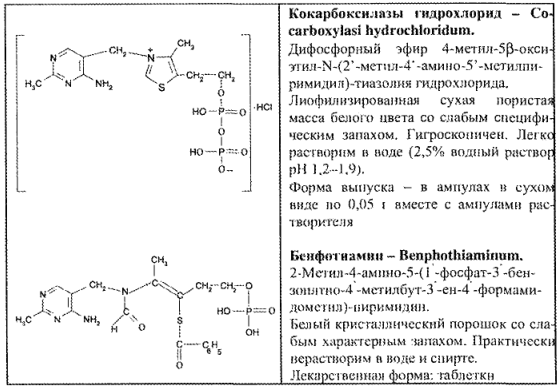
Препараты витамина В1: тиамина бромид (хлорид) и его коферментные формы — кокарбоксилазы гидрохлорид, фосфотиамин и бенфотиамин (табл. 69).
В настоящее время препараты тиамина получают синтетически.
Химические свойства и анализ качества
Общие физико-химические свойства
Тиамин является двукислотным основанием и поэтому образует 2 рода солей – хлориды и гидрохлориды (бромиды и гидробромиды). Фосфотиамин и кокарбоксилаза — сложные эфиры тиамина и фосфорной кислоты, т.е. коферменты.
Эти препараты — белые порошки с характерным запахом, хорошо растворимы в воде, имеют кислую реакцию среды (как соли слабых органических оснований с сильными минеральными кислотами).
Бенфотиамин — синтетический лекарственный препарат, близкий по строению к тиамину и его коферментным формам. В отличие от препаратов-предшественников практически нерастворим в воде.
Стабильность
Тиамин и его производные принадлежат к очень неустойчивым соединениям витаминов. Так, тиамин под действием кислорода воздуха превращается в тиохром и тиаминдисульфид.
Разрушение тиамина вызывают также восстановители, сильно кислая или щелочная среда, свет (особенно УФ-лучи), повышение температуры. В растворах тиамина значение pH не должно превышать 4. За пределами оптимальной области pH повышение температуры больше способствует разложению препарата, чем присутствие кислорода.
Реакции подлинности
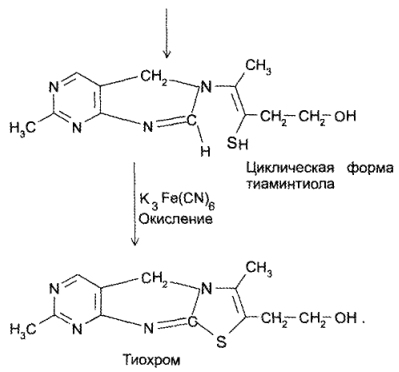
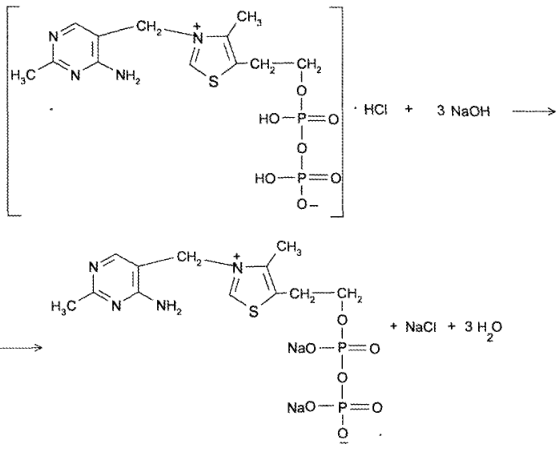
Специфическая общегрупповая реакция подлинности тиамина и его препаратов — образование тиохрома. Сущность испытания заключается в постепенном окислении тиамина в щелочной среде (всего затрачивается 3 эквивалента щелочи) с образованием трициклического производного тиамина (тиохрома), способного давать синюю флюоресценцию в среде бутанола или изоамилового спирта при УФ- облучении.
Реакция идет в несколько стадий. На 1-й стадии происходит частичная нейтрализация препарата как соли галогеноводородной кислоты (1-й эквивалент щелочи):
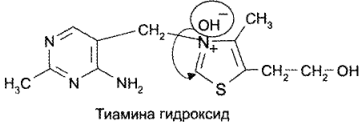
На 2-й стадии образовавшийся тиамина хлорид нейтрализуется (2-м эквивалентом щелочи) как соль четвертичного аммониевого основания до тиамина гидроксида:
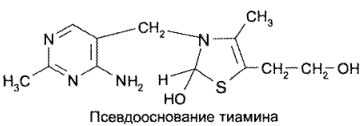
Образовавшийся тиамина гидроксид изомеризуется в псевдооснование тиамина:
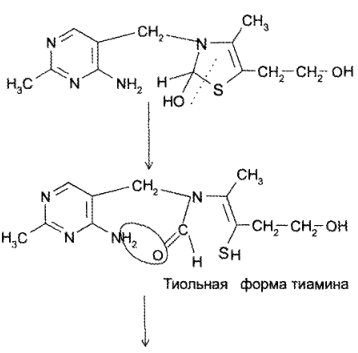
го эквивалента щелочи происходит раскрытие тиазолового кольца с образованием тиольной формы тиамина, которая при дегидратации превращается в циклическую форму тиаминтиола. Окисление последнего приводит к образованию тиохрома:
Тиохром образуют также фосфотиамин и кокарбоксилаза, но не бенфотиамин.
Как соли азотистых оснований препараты тиамина взаимодействуют с общеалкалоидными осадительными реактивами (реактивы Вагнера, Драгендорфа, Майера, гетерополикислотами – кремневольфрамовой, пикриновой, танином и др.) с образованием характерно окрашенных осадков.
Методы количественного определения
Химическая структура лекарственных веществ, производных витамина Вр позволяет применить различные методы их химического и физико-химического количественного определения:
Тиамина бромид количественно определяют гравиметрически в виде комплекса препарата с кремневольфрамовой кислотой.
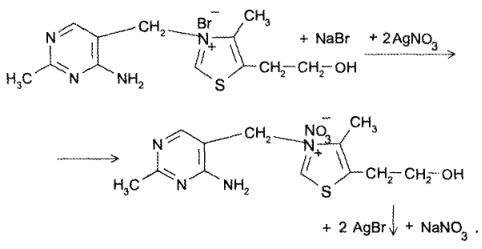
Для количественного определения тиамина бромида применяют также аргентометрическую методику. Определение проводят в 4 стадии. На 1-й стадии осуществляют нейтрализацию тиамина бромида как NН- кислоты 0,1 М раствором натрия гидроксида:
Далее (2-я стадия) готовят индикатор — железа (III) тиоцианат. Для этого к определенному объему 0,1М раствора аммония тиоцианата добавляют раствор железоаммониевых квасцов:
На 3-й стадии сумму бромидов огтитровывают 0,1М раствором серебра нитрата:
На заключительной, 4-й стадии оттитровывают полученный на 2-й стадии железа (III) тиоцианат 0,1 М раствором серебра нитрата:
Объем 0,1 М раствора серебра нитрата, пошедшего на титрование непосредственно тиамина бромида, рассчитывают по разнице между общим объемом титранта и объемами растворов натрия гидроксида и аммония тиоцианата.
Количественное определение тиамина хлорида проводят методом кислотно-основного титрования в среде ледяной уксусной кислоты (как соли двукислотного основания). Для связывания галогенид- иона добавляют ртути (II) ацетат:
Кокарбоксилазы гидрохлорид количественно определяют алкалиметрически (титрант — 0,1 М раствор натрия гидроксида):
ПРОИЗВОДНЫЕ ФЕНОТИАЗИНА
В основе химического строения лекарственных веществ данной группы лежит гетероциклическая система фенотиазина (дибензтиазина), включающая гетероатомы азота и серы.
По фармакологическому действию препараты группы фенотиазина делят на антипсихотические, или нейролептики (к ним относятся 10-алкилпроизводные), и антиаритмические (10-ацилпроизводные).
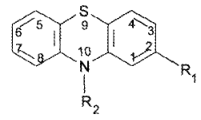
Лекарственные вещества данной группы соответствуют общей формуле:
Антипсихотические средства
Лекарственные вещества фенотиазинового ряда, обладающие антипсихотическим (нейролептическим) эффектом, применяют в клинике около 50 лет для лечения шизофрении, психозов и других ажиотпрованных состояний. Фармакологический эффект производных фенотиазина связан с блокадой дофаминовых рецепторов.
По структуре заместителя при N10 нейролептики ряда фенотиазина подразделяют на содержащие:
Характер заместителя при N10 влияет и ша фармакологический эффект.
В мировой медицинской практике применяют около 40 нейролептиков ряда фенотиазина из синтезированных более 5000 соединений, Поиск новых лекарств этого ряда продолжается.
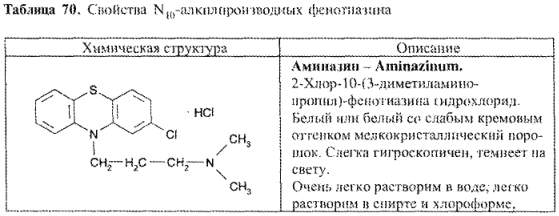
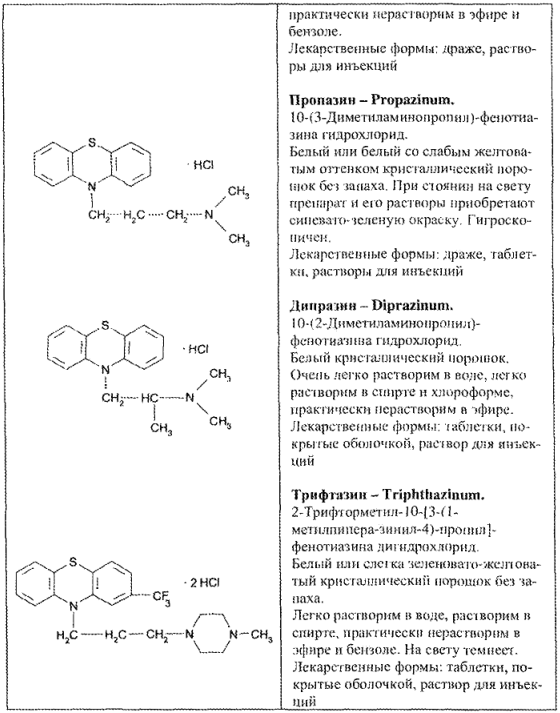
Свойства лекарственных веществ группы N10-алкилпроизводных фенотиазина представлены в табл. 70.
Антиаритмические средства
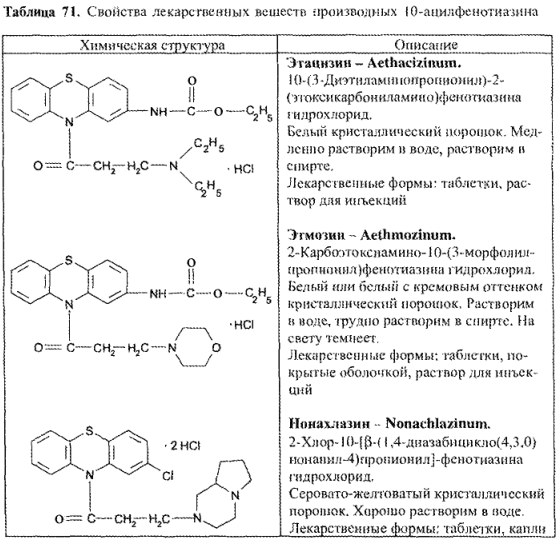
Антиаритмические ЛС группы фенотиазина (этмозин, этацизин, нояахлазин) являются N10-ацилпроизводными. Этмозин и этацизин содержат также карбамидную (в составе уретановой) группу (табл. 71)
Связь между химическим строением и фармакологическим действием
Наряду с психотропным и антиаритмическим фармакологическим эффектом, лекарственные препараты группы фенотиазина обладают и другими видами активности: антигистаминной, холинолитической, гипотермальной и др.
Фармакологический эффект зависит главным образом от строения радикала при N10. Так, нейролептики (аминазин, пропазин, трифтазин и др.) содержат 3 углеродных атома в главной цепи алифатического фрагмента; оказывающий антигистаминное действие дипразин — 2 углеродных атома; у антиаритмических препаратов (этмозин, этапизин, нонахлазин) при N10 находится карбамидная группа. Радикалы при С2 потенцируют фармакологическую активность.
Общие физические свойства
По внешнему виду препараты ряда фенотиазина представляют собой белые кристаллические порошки с оттенками, без запаха. Растворимы в воде, некоторые препараты растворимы и в хлороформе; значения pH водных растворов находятся в пределах 3-4 (алкилпроизводные) и 4-6 (ацилпроизводные).
Характерную Тпл имеют сами препараты (большинство из них – гидрохлориды), их основания и пикраты оснований.
Все препараты группы фенотиазина имеют определенные УФ- и ИК-спектры поглощения. В анализе препаратов данной группы используют и другие физико-химические методы (ЯМР-спектроскопия, ВЭЖХ, тех и др.).
Химические свойства и анализ качества
Кислотно-основные свойства
Большинство лекарственных веществ группы фенотиазина являются солями сильных минеральных кислот и органических азотистых оснований. Основания выделяются из растворов препаратов действием разбавленных растворов щелочей, карбонатов, аммиака.
Как соли азотистых оснований они взаимодействуют с обше- алкалоидными осадительными реактивами (Майера, Драгендорфа, Бушарда, Вагнера, танином, пикриновой кислотой и др.). Некоторые из осадков хорошо кристаллизуются и имеют определенную Тпл. Поскольку основания препаратов группы фенотиазина не кристаллические, а аморфные или маслообразные, определение Тпл комплексов с общеалкалоидными реактивами значимо в анализе их качества. ГФ рекомендует определение Тпл пикрата трифтазина.
Некоторые комплексные соединения препаратов данной группы с реактивом Драгендорфа имеют характерную форму кристаллов, что используют в токсикологической химии.
С палладия хлоридом (II) изучаемые препараты образуют комплексы синего цвета, используемые и для количественного определения лекарственных форм методом ФЭК.
Восстановительные свойства
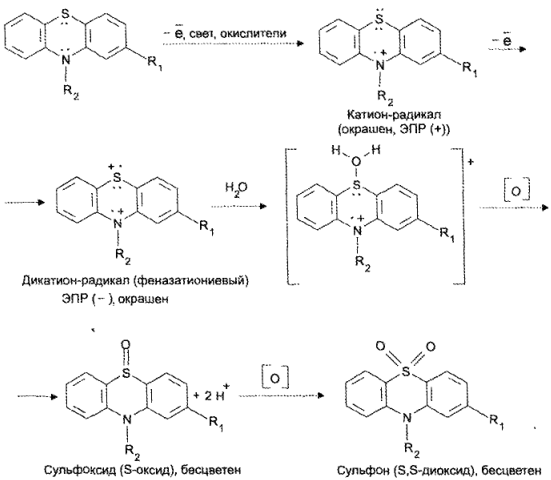
Наиболее важным свойством препаратов группы фенотиазина, определяющим анализ их качества, является чрезвычайно легкая способность к окислению. Процессы окисления сложны. Протекают in vitro и in vivo по следующей схеме:
Окрашивание зависит от характера радикала при С2, и не зависит от характера окислителя. В качестве окислителей национальными фармакопеями используются различные реактивы: бромная вода, раствор калия бромата в кислой среде (ФС), серная кислота концентрированная (Британская фармакопея), железа (III) хлорид в кислой среде и церия (IV) сульфат (Японская фармакопея) и др.
Другие реакции
В препаратах, являющихся гидрохлоридами, определяют хлорид- ион. При этом на раствор препарата действуют раствором щелочи для осаждения основания, а в фильтрате, подкисленном азотной кислотой, определяют хлорид-ион реакцией с серебра нитратом. Непосредственно на препарат действовать серебра нитратом нельзя, так как последний будет окислять систему фенотиазина, и некоторые нитраты (например, аминазина) нерастворимы в воде.
Этмозин и этацизин, содержащие уретановую группировку, подвергаются гидролитическому разложению. По этанольному остатку уретана можно провести йодоформную пробу. Амидная группировка этих же препаратов при N10 позволяет провести гидроксамовую пробу, также гидролиз с последующим определением его продуктов.
Методы количественного определения
Нормативным методом количественного определения индивидуальных препаратов является кислотно-основное титрование в неводной среде.
Возможны и другие способы количественного определения:
Количественное определение препаратов в лекарственных формах (драже, таблетках, растворах для инъекций) осуществляют с помощью различных физико-химических методов (УФ-спектрофотометрии, ФЭК), а также методом Кьельдаля и периметрически.
Стабильность
Чувствительностью препаратов группы фенотиазина к окислению обусловлена необходимость их хранения в герметично закрытых склянках темного стекла, в защищенном от света сухом месте.
Растворы для инъекций стабилизируют добавлением антиоксидантов (смесь натрия сульфита, натрия метабисульфита, кислоты аскорбиновой).
Анализ производных фурана, бензопирана, пиррола, пиразола
» data-shape=»round» data-use-links data-color-scheme=»normal» data-direction=»horizontal» data-services=»messenger,vkontakte,facebook,odnoklassniki,telegram,twitter,viber,whatsapp,moimir,lj,blogger»>
Глава 12. Анализ производных фурана, бензопирана, пиррола, пиразола, имидазола и индола
Нa основе гетероциклических систем создано множество современных ЛС. Получение многих из них стало возможным вследствие изучения биологической активности гетероциклических природных соединений. В свою очередь, изучение их синтетических аналогов служит основой для дальнейшего развития синтеза новых лекарств. В последнее время довольно широко применяется программа компьютерного моделирования лекарств.
ЛС, относящиеся к данной группе, представляют собой разнообразные химические соединения, в которых проявляются закономерности, присущие другим классам и группам химических соединений.
Фуран – пятичленный гетероцикл с гетероатомом кислорода; ему, как и бензолу, присущ ароматический характер. Лекарственные вещества данной группы используют как антибактериальные средства. Строение большинства из них можно представить общей формулой:
По строению эти вещества можно рассматривать как продукт конденсации альдегида 5-нитрофурфурола с соответствующим аминопроизводным:
Таким образом, лекарственные вещества данной группы построены по типу оснований Шиффа и содержат азометиновую связь – СН = И – (табл. 45).


Кислотно-основные свойства
Производные 5-нитрофурана являются веществами кислотного характера. У фурацилина кислотные свойства обусловлены подвижным атомом водорода амидной группы в остатке семикарбазида.
Фурадонин проявляет кислотные свойства за счет кетоенольной и лактим-лактамной таутомерии в гидантоиновом фрагменте:
Лактим-лактамная таутомерия обусловливает также возможность существования фурагина в 2 формах – кислотной (лактамной) и солевой (лактимной).
У фуразолидона кислотные свойства выражены слабее, чем у других лекарственных веществ данной группы.
Кислотные свойства лекарственных веществ группы 5-нитрофурана проявляются в следующих видах взаимодействия:
– с водными растворами щелочей;
– с протофильными растворителями (пиридин, диметилформамид);
– с ионами тяжелых металлов.
Все лекарственные вещества данной группы реагируют с раствором натрия гидроксида, при этом окраска становится более интенсивной. Поэтому реакция со щелочью является общегрупповой для данных веществ. Фурацилин при растворении в 10% растворе натрия гидроксида дает оранжево-красное окрашивание. Происходящее при этом депротонирование NH-кислотного центра вызывает перераспределение электронной плотности, что приводит к ионизации вещества и образованию новой сопряженной системы двойных связей с интенсификацией в результате указанных факторов окраски:
Темно-красное окрашивание при действии раствора натрия гидроксида на фурадонин обусловлено таутомерными превращениями в ядре гидантоина (см. выше), что также приводит к образованию дополнительных двойных связей и ионизации.
Фуразолидон дает бурое окрашивание с 30% раствором щелочи при нагревании, что связано с расщеплением лактонного цикла (ядро оксазолидона) и получением ионизированной соли:
Реакция с групповым реагентом — раствором натрия гидроксида — лежит также в основе количественного фотометрического определения лекарственных веществ группы 5-нитрофурана и их препаратов.
За счет кислотных свойств производные 5-нитрофурана растворяются в протофильных растворителях (пиридин, диметилформамид) с образованием окрашенных анионов, которые с катионами щелочных металлов образуют соли разного цвета, что позволяет дифференцировать данные вещества.
Гидролитическое расщепление
Данное свойство связано с наличием в структуре производных 5-нитрофурана азометиновой, амидной и сложноэфирной групп. Оно используется для отличия фурацилина от других веществ этого ряда. Являясь семикарбазоном, фурацилия подвергается гидролизу как в кислой, так и в щелочной среде при нагревании с образованием соответствующих продуктов:
Методы количественного анализа
При дальнейшем добавлении кислоты серной идет реакция:
Выделившийся йод оттитровывают стандартным раствором натрия тиосульфата:
При расчете М(1/z) фурацилина по данной методике z = 4.
Условия проведения методики (малое количество щелочи и короткое время действия реактива – 1
2 мин) должны обеспечить окисление только гидразина, но не альдегида фурфурола.
ПРОИЗВОДНЫЕ ПИРРОЛА
Витамины группы В12
К ЛС данной группы относятся цианокобаламин, гидроксоко- баламин, кобамамнд. По своей структуре витамин В12 – это кобальтовый комплекс нуклеотида бензимидазола и макроциклической корриновой системы:
Нуклеотидная часть молекулы включает нуклеиновое основание (5,6-диметилбензимидазол), углеводный фрагмент (рибоза) и остаток фосфорной кислоты. Корриновая система состоит из 3 пирролиновых циклов (А, В, С) и 1 пирроллидинового (цикл D):
В центре этой системы находится атом кобальта, который соединен координационными связями с гетероатомами азота 3 пирролиновых циклов и 4-й ковалентной связью – с атомом азота пирролидинового кольца D.
Кроме того, кобальт соединен ковалентной связью с цианогруппой и координационной связью с гетероатомом азота 5,6-диметилбензимидазола нуклеотидной части молекулы. Связь кобальта с остатком кислоты фосфорной является электровалентной, т.е. положительный заряд кобальта частично нейтрализован отрицательным зарядом кислоты фосфорной. Таким образом, цианокобаламин представляет собой одновременно и хелат, и внутреннюю соль, где катионом является корриновый фрагмент, а анионом – нуклеотидная часть.
В корриновой части имеются 3 ацетамидные группы (в положениях 2,1, 18) и 4 пропионамидные (во положениях 3, 8, 13, 17), а также 8 метильных групп. Причем в 17
м положении амидная группа замещена остатком аминоспирта.
Таким образом, нуклеотидная и корриновая части молекулы соединены между собой:
В молекуле цианокобаламина имеется несколько ассиметрических атомов углерода, поэтому лекарственные вещества этой группы оптически активны (левовращающие).
Оксикобаламин отличается от цианокобаламина тем, что атом кобальта связан не с CN-группой, а с оксигруппой. Кроме того, он является солью (гидрохлоридом).
В кобамамиде атом кобальта соединен ковалентной связью не с CN-группой, а с β-5’-дезоксиаденозильным остатком.
Физические и физико-химические свойства
По внешнему виду цианокобаламин, оксикобаламин и кобамамид-кристаллические порошки темно-красного цвета. Цианокобаламин умеренно и медленно растворим в воде, растворим в 95% спирте, практически нерастворим в эфире, хлороформе, ацетоне. Кобамамид трудно растворим в воде; оксикобаламин растворим в воде.
Все указанные лекарственные вещества поглощают свет в УФ- и видимой областях спектра. Поэтому спектрофотометрия широко используется в их анализе: для идентификации, количественной оценки, определения поглощающих примесей. Спектр поглощения цианокобаламина характеризуется 3 полосами поглощения с максимумами при 278, 361 и 550 нм. Поглощение при 278 нм обусловлено наличием фрагмента 5,6-диметилбензимидазола, при 361 нм – корриновой системой с 6 сопряженными двойными связями, при 550 нм – наличием атома кобальта.
Методы анализа
Кроме определения спектральных характеристик, при испытании на подлинность проводят реакции на кобальт и цианогруппу.
Появляется красное окрашивание, сохраняющееся после прибавления кислоты хлороводородной и кипячения. Последнее указывает на прочность комплекса, образованного трехвалентным кобальтом с реактивом:
Определение цианогруппы. Навеску пиан о кобаламина нагревают в пробирке с кислотой щавелевой, под действием которой выделяется кислота циановодородная. Последнюю обнаруживают с помощью фильтровальной бумаги, смоченной раствором бензидина и меди (II) ацетата, в результате чего образуется окрашенное в синий цвет комплексное соединение.
Цианокобаламин (а также оксикобаламин и кобамид) количественно определяют спектрофотометрически с применением стандартного образца лекарственного вещества.
Стабильность и хранение
Цианокобаламин неустойчив в кислой и щелочной средах, так как при этом идет его инактивация как витамина. Наибольшая устойчивость цианокобаламина наблюдается при pH 4,0—6,0. Оксикобаламин и кобамамид устойчивы в слабокислых буферных средах.
Микрофлора поглощает витамины В12, поэтому необходимо предусмотреть хранение в асептических условиях. Окислители, восстановители, соли тяжелых металлов также инактивируют эти вещества.
Цианокобаламин хранят в сухом, защищенном от света месте при комнатной температуре; кобамамид – при температуре не выше 5 °С, а оксикобаламин — при температуре не выше 10 °С (последние два лекарственных вещества являются термолабильными).