марганцовокислый калий что это такое
Марганцовокислый калий
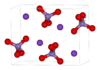
Марганцовокислый калий
| Перманганат калия | |||||||||||||||||||||||
 | |||||||||||||||||||||||
 | |||||||||||||||||||||||
| Общие | |||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Систематическое наименование | Перманганат калия | ||||||||||||||||||||||
| Химическая формула | KMnO4 | ||||||||||||||||||||||
| Отн. молек. масса | 158,03 а. е. м. | ||||||||||||||||||||||
| Молярная масса | 158,03 г/моль | ||||||||||||||||||||||
| Физические свойства | |||||||||||||||||||||||
| Плотность вещества | 2.703 г/см³ | ||||||||||||||||||||||
| Состояние (ст. усл.) | бесцветная жикость | ||||||||||||||||||||||
| Термические свойства | |||||||||||||||||||||||
| Температура разложения | 240 °C | ||||||||||||||||||||||
| Молярная теплоёмкость (ст. усл.) | 119,2 Дж/(моль·К) | ||||||||||||||||||||||
| Энтальпия (ст. усл.) | -813.4 кДж/моль | ||||||||||||||||||||||
| Химические свойства | |||||||||||||||||||||||
| Растворимость в воде | 6.38 (20 °C) г/100 мл | ||||||||||||||||||||||
| Классификация | |||||||||||||||||||||||
| номер CAS | [7722-64-7 | ||||||||||||||||||||||
| Температура, °C | 10 | 20 | 25 | 30 | 40 | 50 | 65 |
| Растворимость, г/100 г воды | 4,22 | 6,36 | 7,63 | 9 | 12,5 | 16,8 | 25 |
Термодинамические свойства
| Стандартная энтальпия образования ΔH | −813,4 кДж/моль (т) (при 298 К) |
| Стандартная энергия Гиббса образования G | −713,8 кДж/моль (т) (при 298 К) |
| Стандартная энтропия S | 171,71 Дж/моль·K (т) (при 298 К) |
| Стандартная мольная теплоёмкость Cp | 119,2 Дж/моль·K (т) (при 298 К) |
Химические свойства
Сильный окислитель. Стандартные окислительно-восстановительные потенциалы приведены в таблице.
В зависимости от pH раствора окисляет различные вещества, восстанавливаясь до соединений марганца разной степени окисления. В кислой среде — до соединений марганца(II), в нейтральной — до соединений марганца(IV), в сильно щелочной — до соединений марганца(VI). Примеры реакций приведены ниже (на примере взаимодействия с сульфитом калия:
Однако надо отметить, что в последняя реакция (в щелочной среде) идёт по указаной схеме только при недостатке восстановителя и высокой концентрации щёлочи, которая обеспечивает замедление гидролиза манганата калия.
При соприкосновении с концентрированной серной кислотой перманганат калия взрывается, однако при аккуратном соединении с холодной кислотой реагирует с образованием неустойчивого оксида марганца(VII):
при этом в качестве промежуточного продукта может образовываться интересное соединение — оксосульфат марганца MnO3HSO4. По реакции с фторидом йода(V) можно получить аналогичный оксофторид:
При нагревании разлагается с выделением кислорода (этим способом пользуются в лаборатории для получения чистого кислорода). Схему реакции упрощённо можно представить уравнением:
На самом деле реакция идёт намного сложнее, например, при не очень сильном нагревании её можно примерно описать уравнением:
Реагирует с солями двухвалентного марганца, например:
Применение
Применение этой соли чаще всего основано на высокой окисляющей способности перманганат-иона, обеспечивающей антисептическое действие.
формула
группа
Медицинское применение
Разбавленные растворы (около 0,1%) перманганата калия нашли широчайшее применение в медицине как антисептическое средство, для полоскания горла, промывания ран, обработки ожогов. В качестве рвотного средства для приёма внутрь при некоторых отравлениях используют разбавленный раствор.
Фармакологическое действие
Показания
Противопоказания
Побочные действия
Способ применения и дозы
Наружно, в водных растворах для промывания ран (0.1-0.5%), для полоскания рта и горла (0.01-0.1%), для смазывания язвенных и ожоговых поверхностей (2-5%), для спринцевания (0.02-0.1%) в гинекологической и урологической практике, а также промывания желудка при отравлениях.
Взаимодействие
Другие сферы применения
Получение
Химическое или электрохимическое окисление соединений марганца, диспропорционирование манганата калия. Например:
Последняя реакция происходит при электролизе концентрированного раствора манганата калия и эндотермична, она является основным промышленным способом получения перманганата калия.
Литература
См. также
Полезное
Смотреть что такое «Марганцовокислый калий» в других словарях:
Марганцовокислый калий — KMnO4, то же, что Перманганат калия … Большая советская энциклопедия
марганцовокислый калий — Калиевая соль марганцовой кислоты, имеющая вид тёмно фиолетовых кристаллов … Словарь многих выражений
марганцовокислый калий — перманганат калия … Cловарь химических синонимов I
Определение массовой доли веществ, восстанавливающих марганцовокислый калий — 3.12. Определение массовой доли веществ, восстанавливающих марганцовокислый калий Метод основан натитровании пробы серной кислоты раствором марганцовокислого калия до появления слабо розовой окраски. Источник: ГОСТ 667 73: Кислота серная… … Словарь-справочник терминов нормативно-технической документации
Калий — (Kalium) К, химический элемент 1 группы периодической системы Менделеева; атомный номер 19, атомная масса 39,098; серебряно белый, очень лёгкий, мягкий и легкоплавкий металл. Элемент состоит из двух стабильных изотопов 39K (93,08%), 41K… … Большая советская энциклопедия
марганцовокислый — ая, ое. марганцовокислый калий … Словарь многих выражений
Калий марганцевокислый — Перманганат калия Общие Систематическое наименование Перманганат калия Химическая формула … Википедия
калий марганцовокислый — сущ., кол во синонимов: 1 • калия перманганат (3) Словарь синонимов ASIS. В.Н. Тришин. 2013 … Словарь синонимов
калий марганцовокислый — kalio permanganatas statusas T sritis chemija formulė KMnO₄ atitikmenys: angl. potassium hypermanganate; potassium permanganate rus. калий марганцовокислый; калия перманганат ryšiai: sinonimas – kalio tetraoksomanganatas … Chemijos terminų aiškinamasis žodynas
марганцовокислый — ая, ое. ◊ Марганцовокислый калий. Калиевая соль марганцовой кислоты, имеющая вид тёмно фиолетовых кристаллов … Энциклопедический словарь
Сильнейший окислитель — перманганат калия
Перманганат калия (в обиходе просто марганцовка) — неорганическое вещество, соль калия и марганцовой кислоты. Формула вещества — KMnO4, химически правильное название — марганцовокислый калий. Массово реактив получают электролизом манганата калия.
Свойства
Марганцовка представляет собой кристаллический 
Перманганат калия — очень сильный окислитель. Активно вступает в реакции с органическими и неорганическими кислотами, вплоть до взрыва. Взаимодействие с химически активными реактивами в порошкообразной форме (алюминием, магнием, кальцием, серой, фосфором) может приводить к самовоспламенению и взрыву. Бурно реагирует с легковоспламеняющимися химикатами, многими органическими веществами (глицерином, сахарозой, танинами и т.п.) — начинается экзотермическая реакция, которая тоже может закончиться взрывом.
Меры предосторожности
Марганцовокислый калий относится к веществам 2 класса опасности как взрывоопасное вещество и к 4-му классу опасности по влиянию на человеческий организм.
Хранят реактив в герметично укупоренных емкостях небольшого объема на крытых сухих складах, вдали от нагревательных приборов. Не допускается совместное хранение с легковоспламеняющимися веществами, органическими веществами.
На производствах, имеющих дело с марганцовкой, помещения должны быть снабжены вентиляцией, работникам следует использовать респираторы и защитные очки.
 |  |  |
| Банка для реактивов 100 мл из темного стекла | Очки защитные закрытые 3Н11 PANORAMA | Квадратная банка из темного стекла, 1000 мл |
Кристаллы химиката и его концентрированные растворы при контакте с кожей или слизистыми оболочками вызывают химический ожог. Проглатывание раствора высокой концентрации вызывает отравление. Его симптомы: сильная боль во рту, гортани, животе; отек гортани, который может привести к удушью. Слизистые рта становятся коричневого или фиолетового цвета. Начинается тошнота, рвота, диарея. Могут появиться судороги, двигательное возбуждение, желудочное кровотечение, проблемы в работе почек, печени сердца. При появлении этих симптомов следует срочно обратиться к врачу.
Применение
Следует отметить, что использование марганцовки требует огромной осторожности, чтобы не нанести себе еще больший вред, пытаясь вылечить что-либо. Именно поэтому, по возможности, стоит предпочесть ей другие лекарственные средства.
ЦЕЛЕБНЫЕ СВОЙСТВА МАРГАНЦОВКИ — ПОЛЕЗНЫЕ СОВЕТЫ
ЛЕЧЕНИЕ МАРГАНЦОВКОЙ — полезные советы
В годы Великой Отечественной войны, как патроны у солдата, она находилась в сумках санитаров, фельдшеров и широко использовалась при лечении ран в госпиталях.
Первое, к чему прибегают при заболеваниях горла, расстройствах кишечника, отравлениях — это марганцовка (перманганат калия, марганцовокислый калий).
В годы Великой Отечественной войны, как патроны у солдата, она находилась в сумках санитаров, фельдшеров и широко использовалась при лечении ран в госпиталях.
В основе действия перманганата калия — его способность окислять органические вещества, выделяя при этом кислород. Этим обусловлено антимикробное и антисептическое действие марганцовки.
Водный раствор перманганата калия обладает противовоспалительными свойствами. В различных концентрациях этот раствор применяют для промывания ран, полоскания рта и горла, для смазывания язвенных и ожоговых поверхностей, спринцеваний. Диапазон применения перманганата калия достаточно широк. Даже при наличии многих новых синтетических средств он и сейчас незаменим «в» гинекологической, урологической, дерматологической практике.
В таблице противоядий при отравлениях перманганат калия является одним из важнейших средств оказания первой помощи.
Однако при всех достоинствах марганцовокислого калия обращаться с ним надо осторожно. В больших концентрациях он прижигает и вызывает отек слизистых оболочек рта, глотки, пищевода, желудка, кишок, рвоту и понос. Поэтому применять раствор следует с осторожностью.
Еще наши бабушки знали полезные в быту свойства марганцовки: ей промывали раны, лечили отравление, обеззараживали, купали младенцев и даже использовали в борьбе с вредителями в огороде. Такое широкое применение марганцовки объясняет главное ее свойство – это противогрибковый, противомикробный препарат. За счет активных процессов окисления марганцовка убивает вредные микробы – возбудителей различных инфекций как на поверхности кожи, так и внутри организма.
Целебные свойства марганцовки (перманганата калия)
Перманганат калия — один из видов перманганатов (от лат. manganum — «марганец») — марганцовокислых солей. Это химическое вещество широко используют как для домашних нужд, так и для медицины. Перманганат калия — кристаллы темно-фиолетового цвета, хорошо растворимые в воде (в зависимости от концентрации цвет может быть от светло-розового до красно-фиолетового), метиловом спирте, уксусной кислоте и ацетоне. В быту марганцовокислый калий, растворенный в воде, называют марганцовкой.
Лечение марганцовкой в медицине
Нейтрализация синильной кислоты (ядовитого вещества) марганцовкой происходит лишь в щелочной среде. Калия перманганат — сильный окислитель. Водный раствор марганцовки оказывает сильное дезинфицирующее и подсушивающее действие, его широко используют в дерматологической и хирургической практике.
При появлении первых признаков гастрита и гастроэнтероколита в первую очередь надо промыть желудок, используя для этого слабый (слегка розовый) раствор марганцовки. Для промывания желудка у взрослых и даже детей зондом пользоваться необязательно, достаточно просто дать выпить больному приготовленный раствор в количестве 0,5 — 2 л, после чего рефлекторно вызвать рвоту.
При отравлениях, когда нужно как можно быстрее вызвать рвоту, пострадавшему дают выпить розовый раствор марганцовки, который является также лекарственным, дезинфицирующим желудочно-кишечный тракт средством.
Раствор зачастую готовят «на глаз», но основные рекомендации — это 10 кристаллов на 1 литр воды, дальнейшую крепость раствора можно корректировать по его цвету. Очень важно, чтобы перед применением все кристаллы растворились в воде, иначе в процессе соприкосновения с кожей или внутренними органами нерастворенные кристаллы могут вызвать ожог.
Наиболее популярен раствор марганцовки при отравлении. При первых признаках, в том числе при диарее больному предлагают раствор марганцовки, который стимулирует очищение кишечника.
Марганцовка для применения внутрь при отравлении готовится в соотношении 2 кристалла на чашку воды, такой раствор выпивается. Благодаря своим антисептическим свойствам подобное лекарство останавливает очаг инфекции в желудке.
Марганцовка – применение в урологии, гинекологии
За счет своих антисептических, противомикробных способностей раствор марганцовки применяют при лечении грибковых, бактериальных заболевания в урологии и гинекологии. Марганцовка имеет применение при молочнице, когда слабый раствор назначают для ежедневных спринцеваний. При урологических проблемах у мужчин, связанных с наружными воспалительными процессами, назначают промывания раствором марганцовки.
При применении в урологии и гинекологии важно соблюдать правила приготовления раствора, следить за тем, чтобы кристаллы марганцовки полностью растворились. В противном случае при попадании на слизистую кристаллы могут вызвать еще большее раздражение.
Марганцовка — противопоказания
Не рекомендуется применять раствор марганцовки при индивидуальной непереносимости. Это сразу можно понять по наличию побочных эффектов – отек, изменение цвета слизистых, резкая боль при применении внутрь, судороги и др. При наличии подобных или других неприятных симптомов прием марганцовки следует прекратить.
Марганцовка за счет своих окислительных свойств абсолютно несовместима с применением угля, сахара и другими веществами, которые легко окисляются. Важно хранить кристаллы перманганата калия вдали от легкоокисляющихся веществ, иначе их соприкосновение может привести к взрыву и даже пожару.
Лечение марганцовкой (перманганатом калия) в народной медицине
Лечение марганцовкой в народной медицине для устранения болей, вызванных мозолями. Для этого в раствор марганцовки розового цвета добавляют поваренную соль и, налив раствор в тазик, опускают в него ноги на 20 мин, после процедуры ноги не нужно вытирать. Через некоторое время боль в области мозолей пройдет. Ни в коем случае для лечения марганцовкой нельзя пользоваться сильно концентрированным раствором (фиолетового цвета), так как это может повлечь за собой вред здоровью, получение ожогов кожи и слизистых, отравление.
Хороший лечебный эффект при опрелостях, в том числе и у грудных детей, оказывают гигиенические ванны с марганцовкой: вода должна быть розового цвета и теплой.
При повышенной потливости нижних конечностей, неприятных запахах, гнойных мозолях поможет теплая ножная ванна с солью и марганцовкой, после процедур ноги следует хорошо вытереть и посыпать тальком.
Лечение перманганатом калия активно используется для промывания открытых ран, в том числе и гноящихся. При дерматитах, характеризующихся появлением пузырей, кожу следует обмыть розовым раствором перманганата калия.
Если при постановке банок их слишком долго держать, на коже могут образоваться багровые пятна и даже пузырьки, наполненные сукровичной жидкостью. В подобных случаях пораженные места полезно смазать 5 — 10%-ным раствором марганцовокислого калия.
Лечение перманганатом калия на практике: лучшие рецепты
В запущенных случаях геморроя можно приготовить целебный раствор.
1 ч. л. пищевой соды,
1 ст. л. любого растительного масла,
марганцовка,
3 л воды.
В горячую воду всыпать столько марганцовки, чтобы получить розовый цвет, добавить соду, масло, раствор влить в ванну.
Применение. Принимать ванну в течение 20 мин на ночь. Процедуру проводить ежедневно в течение недели.
В народной медицине есть рецепт для лечения марганцовкой от дизентерии.
В состав этого средства входят несколько кристаллов марганцовки на 0,5 л воды. Советуют увеличивать концентрацию раствора в зависимости от возраста (грудничкам — бледно-розовый, а взрослым людям — малиновый раствор).
Рекомендуется принимать такой раствор внутрь, совмещая это с процедурой постановки клизмы.
Надо иметь в виду, что перманганат калия при взаимодействии с различными органическими веществами становится взрывоопасным. Поэтому его кристаллы надо хранить в чистой стеклянной посуде с притертыми пробками, а раствор — в склянках из темного стекла, так как под действием солнечных лучей и дневного света он легко разлагается.
При пользовании раствором часто остаются трудно смываемые пятна на коже и белье. Чтобы устранить их, кожу можно обмыть раствором сернистого аммония в концентрации 1:5, а затем горячей водой. С белья пятна выводят раствором щавелевой кислоты (1:9), 2-процентным раствором соляной кислоты, уксусом или лимонным соком..
Источник
Понравилась статья? Подпишитесь на канал, чтобы быть в курсе самых интересных материалов
Калий марганцевокислый
Калий марганцевокислый
| Перманганат калия | |||||||||||||||||||||||
 | |||||||||||||||||||||||
 | |||||||||||||||||||||||
| Общие | |||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Систематическое наименование | Перманганат калия | ||||||||||||||||||||||
| Химическая формула | KMnO4 | ||||||||||||||||||||||
| Отн. молек. масса | 158,03 а. е. м. | ||||||||||||||||||||||
| Молярная масса | 158,03 г/моль | ||||||||||||||||||||||
| Физические свойства | |||||||||||||||||||||||
| Плотность вещества | 2.703 г/см³ | ||||||||||||||||||||||
| Состояние (ст. усл.) | бесцветная жикость | ||||||||||||||||||||||
| Термические свойства | |||||||||||||||||||||||
| Температура разложения | 240 °C | ||||||||||||||||||||||
| Молярная теплоёмкость (ст. усл.) | 119,2 Дж/(моль·К) | ||||||||||||||||||||||
| Энтальпия (ст. усл.) | -813.4 кДж/моль | ||||||||||||||||||||||
| Химические свойства | |||||||||||||||||||||||
| Растворимость в воде | 6.38 (20 °C) г/100 мл | ||||||||||||||||||||||
| Классификация | |||||||||||||||||||||||
| номер CAS | [7722-64-7 | ||||||||||||||||||||||
| Температура, °C | 10 | 20 | 25 | 30 | 40 | 50 | 65 |
| Растворимость, г/100 г воды | 4,22 | 6,36 | 7,63 | 9 | 12,5 | 16,8 | 25 |
Термодинамические свойства
| Стандартная энтальпия образования ΔH | −813,4 кДж/моль (т) (при 298 К) |
| Стандартная энергия Гиббса образования G | −713,8 кДж/моль (т) (при 298 К) |
| Стандартная энтропия S | 171,71 Дж/моль·K (т) (при 298 К) |
| Стандартная мольная теплоёмкость Cp | 119,2 Дж/моль·K (т) (при 298 К) |
Химические свойства
Сильный окислитель. Стандартные окислительно-восстановительные потенциалы приведены в таблице.
В зависимости от pH раствора окисляет различные вещества, восстанавливаясь до соединений марганца разной степени окисления. В кислой среде — до соединений марганца(II), в нейтральной — до соединений марганца(IV), в сильно щелочной — до соединений марганца(VI). Примеры реакций приведены ниже (на примере взаимодействия с сульфитом калия:
Однако надо отметить, что в последняя реакция (в щелочной среде) идёт по указаной схеме только при недостатке восстановителя и высокой концентрации щёлочи, которая обеспечивает замедление гидролиза манганата калия.
При соприкосновении с концентрированной серной кислотой перманганат калия взрывается, однако при аккуратном соединении с холодной кислотой реагирует с образованием неустойчивого оксида марганца(VII):
при этом в качестве промежуточного продукта может образовываться интересное соединение — оксосульфат марганца MnO3HSO4. По реакции с фторидом йода(V) можно получить аналогичный оксофторид:
При нагревании разлагается с выделением кислорода (этим способом пользуются в лаборатории для получения чистого кислорода). Схему реакции упрощённо можно представить уравнением:
На самом деле реакция идёт намного сложнее, например, при не очень сильном нагревании её можно примерно описать уравнением:
Реагирует с солями двухвалентного марганца, например:
Применение
Применение этой соли чаще всего основано на высокой окисляющей способности перманганат-иона, обеспечивающей антисептическое действие.
формула
группа
Медицинское применение
Разбавленные растворы (около 0,1%) перманганата калия нашли широчайшее применение в медицине как антисептическое средство, для полоскания горла, промывания ран, обработки ожогов. В качестве рвотного средства для приёма внутрь при некоторых отравлениях используют разбавленный раствор.
Фармакологическое действие
Показания
Противопоказания
Побочные действия
Способ применения и дозы
Наружно, в водных растворах для промывания ран (0.1-0.5%), для полоскания рта и горла (0.01-0.1%), для смазывания язвенных и ожоговых поверхностей (2-5%), для спринцевания (0.02-0.1%) в гинекологической и урологической практике, а также промывания желудка при отравлениях.
Взаимодействие
Другие сферы применения
Получение
Химическое или электрохимическое окисление соединений марганца, диспропорционирование манганата калия. Например:
Последняя реакция происходит при электролизе концентрированного раствора манганата калия и эндотермична, она является основным промышленным способом получения перманганата калия.
Литература
См. также
Полезное
Смотреть что такое «Калий марганцевокислый» в других словарях:
Марганцевокислый калий — Перманганат калия Общие Систематическое наименование Перманганат калия Химическая формула … Википедия
МАРГАНЦЕВОКИСЛЫЙ КАЛИЙ — химическое соединение, имеющее вид мелких темно фиолетовых с металлическим отливом кристаллов; обладает обеззараживающими свойствами. Слабые водные растворы (0,5 2% от розового до малинового цвета) применяются гл. обр. для промывания половых… … Сельскохозяйственный словарь-справочник
АБОРТИВНЫЕ ВЕЩЕСТВА — АБОРТИВНЫЕ ВЕЩЕСТВА, или плодогонные вещества, лекарственные средства, к которым прибегают, чтобы прервать беременность в течение ее первых 28 недель. А. в. в научной медицине до сих пор не получили полного признания, потому что действие их не… … Большая медицинская энциклопедия
Швеция — (Sverige) Королевство Швеция (Konungariket Sverige). I. Общие сведения Ш. государство в Северной Европе, на В. и Ю. Скандинавского полуострова. Граничит на З. и С. с Норвегией, на С. В. с Финляндией. На Ю. и В.… … Большая советская энциклопедия
АНТИСЕПТИКА — обеззараживание ран, ссадин и пр. при помощи химических веществ, убивающих микробов, попавших в рану. Средствами А. в ветеринарии являются: креолин, лизол, карболовая кислота, йодная настойка, марганцевокислый калий, перекись водорода (3%),… … Сельскохозяйственный словарь-справочник
АПТЕЧКА ВЕТЕРИНАРНАЯ — набор медикаментов и инструментов для подачи первой помощи заболевшим жив. А. в д. б. в каждом совхозе, колхозе и ферме. А. в. включает дезинфекционные средства (креолин, марганцевокислый калий, настойку иода, нафталин, зеленое мыло и др.),… … Сельскохозяйственный словарь-справочник
ХОЛЕРА ПТИЦ — острая заразная болезнь, обычно протекающая очень быстро (1 2 дня). Иногда птицы падают внезапно, без всяких предшествующих признаков, иногда же болезнь протекает хронически. Заражение происходит от поедания птицами испражнений больных, через… … Сельскохозяйственный словарь-справочник
ОТБЕЛИВАНИЕ ФОТОГРАФИЧЕСКОЕ — удаление из фотослоя серебра путём образования с ним соединений, растворимых в воде или образующих прозрачные (белые) структуры в эмульсии. Осуществляется в р ре, содержащем окислитель серебра (железосинеродистый двухромовокислый или… … Большой энциклопедический политехнический словарь
Дезодорант — Палочковый дезодорант Дезодоранты (от фр. dés приставка, означающая удаление, и лат. odor запах) … Википедия
Дезодорация — Дезодоранты женские Дезодоранты мужские Палочковый дезодорант Дезодоранты косметические изделия, применяемые для устранения запаха (дезодорация, от дез лишение, устранение, и лат. odor запах, т.е. устранение запаха). Наиболее часто дезодоранты… … Википедия