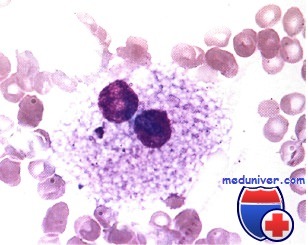
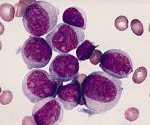
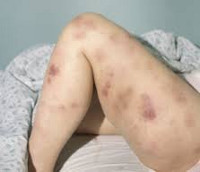
миелобласты в крови что это значит
Миелобласты в крови что это значит
На основании общеклинического анализа крови сложно дать оценку состояния гемопоэза. Более полное представление дает изучение костного мозга (цитологическое, цитохимическое и др.).
Цитологический анализ костного мозга играет большую роль в диагностике заболеваний кроветворной системы. Подсчет миелограммы дает представление о характере эритропоэза (нормобластический или мегалобластический), позволяет обнаружить клетки, характерные для различных заболеваний системы крови (множественной миеломы, острых лейкозов, хронического миелолейкоза, хронического лимфолейкоза, лейкемизированных неходжкинских лимфом, болезни Гоше, Ниманна-Пика, метастазов рака в костном мозге и др.).
Данные миелограммы необходимы для проведения дифференциального диагноза с лейкемоидными реакциями. Сопоставление данных костномозгового кроветворения с картиной периферической крови и клинической симптоматикой позволяет уточнить причину анемии.
Имеются абсолютные и относительные показания к стернальной пункции.
Абсолютные показания: все анемии (кроме типичной железодефицитной), различные цитопении (одноростковая, двуростковая, панцитопения), острые лейкозы, хронические лейкозы в начальной стадии (для подтверждения диагноза и исключения лейкемоидных реакций), выраженное изолированное увеличение СОЭ (для исключения множественной миеломы и макроглобулинемии Вальденстрема), подозрение на метастазы злокачественной опухоли в костном мозге.
Относительные показания: железодефицитные анемии, хронические лейкозы в развернутой стадии.
Аспирационная биопсия костного мозга является технически простым, безопасным и легкодоступным методом. Наиболее часто используется стернальная пункция, предложенная в 1927 г. М. И. Аринкиным и впервые выполненная на кафедре факультетской терапии Военно-медицинской академии. При необходимости можно пунктировать гребень или бугристость подвздошной кости, у детей — пяточную кость. Пункция грудины выполняется иглой И. А. Кассирского с предохранительным щитком. После взятия аспирата костного мозга производят подсчет количества миелокариоцитов, мегакариоцитов, ретикулоцитов, готовят мазки для подсчета миелограммы.
Нормальная миелограмма
| Показатели миелограммы | Среднее значение (%) | Пределы колебаний (%) |
| Ретикулярные клетки | 0,9 | 0,1-1,6 |
| Недифференцированные бласты | 0,6 | 0,1-1,1 |
| Миелобласты | 1,0 | 0,2-1,7 |
| Промиелоциты | 2,5 | 1,0-4,1 |
| Миелоциты нейтрофильные | 9,6 | 7,0-12,2 |
| Метамиелоциты нейтрофильные | 11,5 | 8,0-15,0 |
| Палочкоядерные нейтрофилы | 18,2 | 12,8-23,7 |
| Сегментоядерные нейтрофилы | 18,6 | 13,1-24,1 |
| Всего клеток нейтрофильного ряда | 60,8 | 52,7-68,9 |
| Миелоциты эозинофильные | 0,1 | 0,0-0,2 |
| Метамиелоциты эозинофильные | 0,2 | 0,1-0,4 |
| Эозинофилы | 2,8 | 0,4-5,2 |
| Всего клеток эозинофилъного ряда | 3,2 | 0,5-5,8 |
| Миелоциты базофильные | 0,1 | 0-0,3 |
| Базофилы | 0,1 | 0-0,3 |
| Всего клеток базофильного ряда | 0,2 | 0-0,5 |
| Лимфобласты | 0,1 | 0-0,2 |
| Пролимфоциты | 0,1 | 0-0,2 |
| Лимфоциты | 8,8 | 4,3-13,3 |
| Всего клеток лимфоидного ряда | 9,0 | 4,3-13,7 |
| Монобласты | 0,1 | 0-0,2 |
| Моноциты | 1,9 | 0,7-3,1 |
| Плазмобласты | 0,1 | 0-0,2 |
| Проплазмоциты | 0,1 | 0,1-0,2 |
| Плазматические клетки | 0,9 | 0,1-1,8 |
| Эритробласты | 0,6 | 0,2-1,1 |
| Нормобласты базофильные | 3,6 | 1,4-5,8 |
| Нормобласты полихроматофильные | 12,9 | 8,9-16,9 |
| Нормобласты оксифильные | 3,2 | 0,8-5,6 |
| Всего клеток эритроидного ряда | 20,5 | 14,5-26,5 |
| Мегакариоциты | 0,4 | 0,2-0,6 |
Миелокариоциты миелограммы. У здоровых людей количество миелокариоцитов (всех ядросодержащих клеток костного мозга) в камере Горяева составляет 50-250•10 9 /л.
Мегакариоциты миелограммы. Нормальное количество мегакариоцитов в камере Фукса-Розенталя составляет 0,05-0,1•10 6 /л. Необходимо также определять количество мегакариоцитов в окрашенных мазках в 250 полях зрения под малым увеличением и при подсчете миелограммы в процентах.
Следует помнить, что снижение уровня миелокариоцитов и мегакариоцитов в миелограмме отмечается также при разведении аспирата периферической кровью (технические погрешности при выполнении стернальной пункции).
Ретикулоциты миелограммы. Нормальное количество ретикулоцитов в костном мозге составляет 20-30%о. Увеличение их числа наблюдается при гемолитических и постгеморрагических анемиях.
Морфологический анализ клеток костного мозга (подсчет миелограммы) производят на 500 клеток костного мозга, после чего вычисляют процентное содержание каждого вида клеток.
При анализе миелограммы необходимо оценить клеточность костного мозга (нормо-, гипо- или гиперклеточный), дать качественную характеристику всех клеточных рядов с определением индексов созревания, лейкоэритробластического соотношения, характера эритропоэза (нормобластический, мегалобластический или с мегалобластоидными чертами) и количества митозов. Отдельно следует оценить мегакариоцитопоэз (количество и функция мегакариоцитов).
Костномозговой индекс созревания нейтрофилов определяется по формуле: (промиелоциты + миелоциты + метамиелоциты)/ (палочкоядерные + сегментоядерные нейтрофилы)
В норме костномозговой индекс созревания нейтрофилов равен 0,6-0,8.
Индекс созревания эритроидных клеток определяется по формуле: (полихроматофильные + оксифильные нормоциты)/(эритробласты + базофильные + полихроматофильные + оксифильные нормоциты)
В норме индекс созревания эритроидных клеток равен 0,8-0,9.
Уменьшение индекса свидетельствует о задержке гемоглобинизации и/или преобладании молодых базофильных нормоцитов, дает возможность ориентировочно оценить запасы и обмен железа в организме.
Лейкоэритробластическое соотношение определяется по формуле: (гранулоциты): (ядросодержащие клетки эритроидного ряда) и в норме составляет 3-4:1.
Количество митозов в норме составляет 3,5 на 1000 для клеток гранулоцитарного ряда и 5 на 1000 — для клеток эритроидного ряда.
Заключение по миелограмме не должно быть категоричным, поскольку для постановки диагноза необходимо учитывать клинические данные и показатели периферической крови.
Для более полной характеристики гемопоэза, особенно мегакариоцитопоэза, в ряде случаев требуется гистологическое исследование костного мозга методом трепанобиопсии.
Определение сидеробластов и сидероцитов в миелограмме
При железодефицитных и сидеробластных анемиях важно определять количество сидероцитов и сидеробластов — эритроцитов и эритробластов, содержащих в цитоплазме железо в виде гемосидерина и ферритина (зернышки синего цвета при окраске по Перлсу диаметром 0,2-1,5 мкм). У здоровых людей в периферической крови содержится 1,1-3,0% (в среднем 1,6%) сидероцитов. Содержание сидеробластов в костном мозге составляет 15-40% от всех клеток эритроидного ряда; количество гранул в них обычно 1-2 (не более 4).
Клиническое значение. При хронических железодефицитных анемиях отмечается снижение количества сидероцитов и сидеробластов в костном мозге, гранулы железа в них практически выявить не удается.
Увеличение количества сидеробластов с большим количеством гранул железа в каждом из них, появление кольцевых форм сидеробластов наблюдается при наследственных и приобретенных сидеробластных анемиях (интоксикация свинцом, один из вариантов миелодиспластического синдрома — рефрактерная анемия с кольцевыми сидеробластами).
Наряду с исследованием крови и костного мозга для диагностики специфических поражений и осложнений проводимой терапии в ряде случаев необходим анализ биологических жидкостей (мочи, кала, мокроты, экссудатов, ликвора).
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Миелобласты в крови что это значит
Лейкоз – это злокачественное заболевание, при котором в костном мозге нарушается процесс кроветворения. В результате в кровь попадает большое количество незрелых лейкоцитов, которые не справляются со своей основной функцией – защитой организма от инфекций. Постепенно они вытесняют здоровые клетки крови, а также проникают в различные органы, нарушая их работу.
Рак крови – одно из самых распространенных онкологических заболеваний, которое встречается как у детей, так и у взрослых. Прогноз заболевания зависит от множества факторов: типа лейкоза, возраста пациента, сопутствующих заболеваний. За последние десятилетия были разработаны и постоянно совершенствуются методы эффективного лечения лейкемии.
Лейкемия, белокровие, рак крови.
Leukemia, leucosis, bloodcancer.
Симптомылейкоза могут развиваться остро или постепенно. Они неспецифичны, зависят от типа лейкоза и на начальных этапах могут напоминать грипп или другое инфекционное заболевание.
Симптомами лейкоза являются:
Общая информация о заболевании
Все клетки крови – лейкоциты, эритроциты, тромбоциты – образуются в костном мозге – специфической кроветворной ткани, которая находится в костях таза, грудине, позвонках, ребрах, длинных трубчатых костях. Он содержит стволовые клетки, которые дают начало всем клеткам крови. В процессе деления из них сначала формируются лимфоидные и миелоидные стволовые клетки. Из лимфоидных стволовых клеток образуются лимфобласты, а из миелоидных – миелобласты, а также предшественники эритроцитов и тромбоцитов. Из лимфобластов и миелобластов получаются лейкоциты. Бласты отличаются от зрелых лейкоцитов строением и функциями и должны пройти через ряд последовательных делений, в ходе которых образуются все более специализированные клетки-предшественники. После последнего деления из предшественников формируются зрелые, функциональные клетки крови. Таким образом, из лимфоидных стволовых клеток образуются лимфоциты (разновидность лейкоцитов), а из миелоидных – эритроциты, тромбоциты и остальные виды лейкоцитов (нейтрофилы, базофилы, эозинофилы и моноциты). Это зрелые клетки крови, способные выполнять свои специфические функции: эритроциты доставляют кислород к тканям, тромбоциты обеспечивают свертываемость крови, лейкоциты – защиту от инфекций. После выполнения своей задачи клетки погибают.
Весь процесс деления, гибели и созревания клеток крови заложен в их ДНК. При ее повреждении нарушается процесс роста и деления клеток крови, преимущественно лейкоцитов. В кровь попадает большое количество незрелых лейкоцитов, не способных выполнять свою функцию, и в результате организм не справляется с инфекциями. Незрелые клетки очень активно делятся, живут дольше, постепенно вытесняя другие клетки крови – эритроциты и тромбоциты. Это приводит к анемии, слабости, частым длительным кровотечениям, кровоизлияниям. Незрелые лейкоциты также могут проникать в другие органы, нарушая их функцию, – в печень, селезенку, лимфатические узлы, головной мозг. В результате пациент жалуется на боли в животе и в голове, отказывается от еды, худеет.
В зависимости от того, какой тип лейкоцитов вовлечен в патологический процесс и как быстро развивается заболевание, различают следующие виды лейкозов.
Таким образом, при острых лейкозах в костном мозге и крови накапливается большое количество незрелых, бесполезных лейкоцитов, что требует незамедлительного лечения. При хронических лейкозах заболевание начинается постепенно, в кровь попадают более специализированные клетки, способные какое-то время выполнять свою функцию. Они могут протекать годами, не проявляя себя.
Кто в группе риска?
Основные методы диагностики лейкемии
Изменение уровня лейкоцитов, эритроцитов, тромбоцитов, внешний вид лейкоцитов, степень их зрелости позволяют врачу заподозрить у пациента лейкоз. Похожие изменения в соотношении клеток крови возможны и при других заболеваниях – инфекциях, иммунодефицитных состояниях, отравлениях токсическими веществами, – однако при них в крови отсутствуют бласты – предшественники лейкоцитов. Бласты имеют характерные признаки, хорошо различимые под микроскопом. Если они обнаружены в крови, велика вероятность того, что у пациента один из видов лейкоза, поэтому необходимо дальнейшее обследование.
Дополнительно врач может назначить:
Тактика лечения лейкоза определяется типом заболевания, возрастом пациента и его общим состоянием. Оно проводится в специализированных гематологических отделениях больниц. Лечение острого лейкоза необходимо начинать как можно раньше, хотя в случае хронического лейкоза при медленном прогрессировании заболевания и хорошем самочувствии терапия может быть отложена.
Существует несколько методов лечения лейкемии.
Прогноз заболевания зависит от типа лейкоза. При остром лимфобластном лейкозе более 95 % пациентов излечивается, при остром миелобластном – около 75 %. При хронических лейкозах на прогноз влияет стадия заболевания, на которой начато лечение. Этот тип лейкоза прогрессирует медленно, и средняя продолжительность жизни пациентов составляет 10-20 лет.
Специфическая профилактика лейкозов отсутствует. Для своевременной диагностики заболевания необходимо регулярно проходить профилактические медицинские осмотры.
Рекомендуемые анализы
Острый миелоидный лейкоз
Острый миелоидный лейкоз – злокачественное заболевание системы крови, сопровождающееся неконтролируемым размножением измененных лейкоцитов, снижением количества эритроцитов, тромбоцитов и нормальных лейкоцитов. Проявляется повышенной склонностью к развитию инфекций, лихорадкой, быстрой утомляемостью, потерей веса, анемией, кровоточивостью, образованием петехий и гематом, болями в костях и суставах. Иногда выявляются изменения кожи и припухлость десен. Диагноз устанавливается на основании клинических симптомов и данных лабораторных исследований. Лечение – химиотерапия, трансплантация костного мозга.
МКБ-10
Общие сведения
Острый миелоидный лейкоз (ОМЛ) – злокачественное поражение миелоидного ростка крови. Неконтролируемая пролиферация лейкозных клеток в костном мозге влечет за собой подавление остальных ростков крови. В результате количество нормальных клеток в периферической крови уменьшается, возникают анемия и тромбоцитопения. Острый миелоидный лейкоз является самым распространенным острым лейкозом у взрослых. Вероятность развития болезни резко увеличивается после 50 лет. Средний возраст пациентов составляет 63 года. Мужчины и женщины молодого и среднего возраста страдают одинаково часто. В старшей возрастной группе наблюдается преобладание лиц мужского пола. Прогноз зависит от вида острого миелоидного лейкоза, пятилетняя выживаемость колеблется от 15 до 70%. Лечение осуществляют специалисты в области онкологии и гематологии.
Причины острого миелоидного лейкоза
Непосредственной причиной развития ОМЛ являются различные хромосомные нарушения. В числе факторов риска, способствующих развитию таких нарушений, указывают неблагоприятную наследственность, ионизирующее излучение, контакт с некоторыми токсическими веществами, прием ряда лекарственных препаратов, курение и болезни крови. Вероятность возникновения острого миелоидного лейкоза увеличивается при синдроме Блума (низкий рост, высокий голос, характерные черты лица и разнообразные кожные проявления, в том числе гипо- или гиперпигментация, кожная сыпь, ихтиоз, гипертрихоз) и анемии Фанкони (низкий рост, дефекты пигментации, неврологические расстройства, аномалии скелета, сердца, почек и половых органов).
Острый миелоидный лейкоз достаточно часто развивается у больных с синдромом Дауна. Прослеживается также наследственная предрасположенность при отсутствии генетических заболеваний. При ОМЛ у близких родственников вероятность возникновения болезни повышается в 5 раз по сравнению со средними показателями по популяции. Самый высокий уровень корреляции выявляется у однояйцевых близнецов. Если острый миелоидный лейкоз диагностируется у одного близнеца, риск у второго составляет 25%. Одним из важнейших факторов, провоцирующих ОМЛ, являются заболевания крови. Хронический миелоидный лейкоз в 80% случаев трансформируется в острую форму болезни. Кроме того, ОМЛ нередко становится исходом миелодиспластического синдрома.
Ионизирующее излучение вызывает острые миелоидные лейкозы при превышении дозы 1 Гр. Заболеваемость увеличивается пропорционально дозе облучения. На практике имеет значение пребывание в зонах атомных взрывов и аварий на атомных электростанциях, работа с источниками излучения без соответствующих защитных средств и радиотерапия, применяемая при лечении некоторых онкологических заболеваний. Причиной развития острого миелоидного лейкоза при контакте с токсическими веществами является аплазия костного мозга в результате мутаций и поражения стволовых клеток. Доказано негативное влияние толуола и бензола. Обычно ОМЛ и другие острые лейкозы диагностируются спустя 1-5 лет после контакта с мутагеном.
В числе лекарственных средств, способных провоцировать острые миелоидные лейкозы, специалисты называют некоторые препараты для химиотерапии, в том числе ингибиторы ДНК-топоизомеразы II (тенипозид, этопозид, доксорубицин и другие антрациклины) и алкилирующие средства (тиофосфамид, эмбихин, циклофосфамид, хлорамбуцил, кармустин, бусульфан). ОМЛ также может возникать после приема хлорамфеникола, фенилбутазона и препаратов мышьяка. Доля лекарственных острых миелоидных лейкозов составляет 10-20% от общего количества случаев заболевания. Курение не только повышает вероятность развития ОМЛ, но и ухудшает прогноз. Средняя пятилетняя выживаемость и продолжительность полных ремиссий у курильщиков ниже, чем у некурящих.
Классификация острого миелоидного лейкоза
Классификация острого миелоидного лейкоза по версии ВОЗ очень сложна и включает в себя несколько десятков разновидностей заболевания, разделенных на следующие группы:
Тактика лечения, прогноз и продолжительность ремиссий при разных видах ОМЛ могут существенно различаться.
Симптомы острого миелоидного лейкоза
Клиническая картина включает в себя токсический, геморрагический, анемический синдромы и синдром инфекционных осложнений. На ранних стадиях проявления острого миелоидного лейкоза неспецифичны. Отмечается повышение температуры без признаков катарального воспаления, слабость, утомляемость, потеря веса и аппетита. При анемии присоединяются головокружения, обморочные состояния и бледность кожных покровов. При тромбоцитопении наблюдаются повышенная кровоточивость и петехиальные кровоизлияния. Возможно образование гематом при незначительных ушибах. При лейкопении возникают инфекционные осложнения: частые нагноения ран и царапин, упорные повторные воспаления носоглотки и т. д.
В отличие от острого лимфобластного лейкоза при остром миелоидном лейкозе отсутствуют выраженные изменения со стороны периферических лимфатических узлов. Лимфоузлы небольшие, подвижные, безболезненные. Иногда выявляется увеличение лимфатических узлов в шейно-надключичной области. Печень и селезенка в пределах нормы или незначительно увеличены. Характерны признаки поражения костно-суставного аппарата. Многие больные острым миелоидным лейкозом предъявляют жалобы на боли различной степени интенсивности в области позвоночника и нижних конечностей. Возможны ограничения движений и изменения походки.
В числе экстрамедуллярных проявлений острого миелоидного лейкоза – гингивит и экзофтальм. В отдельных случаях наблюдаются припухлость десен и увеличение небных миндалин в результате инфильтрации лейкозными клетками. При миелоидной саркоме (составляет около 10% от общего количества случаев острого миелоидного лейкоза) на коже пациентов появляются зеленоватые, реже – розовые, серые, белые или коричневые опухолевидные образования (хлоромы, кожные лейкемиды). Иногда при поражениях кожи обнаруживается паранеопластический синдром (синдром Свита), который проявляется воспалением кожных покровов вокруг лейкемидов.
В развитии острого миелоидного лейкоза выделяют пять периодов: начальный или доклинический, разгара, ремиссии, рецидива и терминальный. В начальном периоде острый миелоидный лейкоз протекает бессимптомно или проявляется неспецифической симптоматикой. В периоде разгара токсический синдром становится более выраженным, выявляются анемический, геморрагический и инфекционный синдромы. В период ремиссии проявления острого миелоидного лейкоза исчезают. Рецидивы протекают аналогично периоду разгара. Терминальный период сопровождается прогрессирующим ухудшением состояния больного и завершается летальным исходом.
Диагностика и лечение острого миелоидного лейкоза
Решающую роль в процессе диагностики играют лабораторные анализы. Используют анализ периферической крови, миелограмму, микроскопические и цитогенетические исследования. Для получения образца тканей выполняют аспирационную биопсию костного мозга (стернальную пункцию). В анализе периферической крови больного острым миелоидным лейкозом обнаруживается снижение количества эритроцитов и тромбоцитов. Количество лейкоцитов может быть как повышенным, так и (реже) пониженным. В мазках могут выявляться бласты. Основанием для постановки диагноза «острый миелоидный лейкоз» становится обнаружение более 20% бластных клеток в крови либо в костном мозге.
Основой лечения острого миелоидного лейкоза является химиотерапия. Выделяют два этапа лечения: индукцию и консолидацию (постремиссионную терапию). На этапе индукции выполняют лечебные мероприятия, направленные на уменьшение количества лейкозных клеток и достижение состояния ремиссии. На этапе консолидации устраняют остаточные явления болезни и предотвращают рецидивы. Лечебную тактику определяют в зависимости от вида острого миелоидного лейкоза, общего состояния больного и некоторых других факторов.
Наиболее популярная схема индукционного лечения – «7+3», предусматривающая непрерывное внутривенное введение цитарабина в течение 7 дней в сочетании с одновременным быстрым периодическим введением антрациклинового антибиотика в течение первых 3 дней. Наряду с этой схемой в процессе лечения острого миелоидного лейкоза могут применяться другие лечебные программы. При наличии тяжелых соматических заболеваний и высоком риске развития инфекционных осложнений в результате подавления миелоидного ростка (обычно – у больных старческого возраста) используют менее интенсивную паллиативную терапию.
Программы индукции позволяет добиться ремиссии у 50-70% пациентов с острым миелоидным лейкозом. Однако без дальнейшей консолидации у большинства больных наступает рецидив, поэтому второй этап лечения рассматривается, как обязательная часть терапии. План консолидационного лечения острого миелоидного лейкоза составляется индивидуально и включает в себя 3-5 курсов химиотерапии. При высоком риске рецидивирования и уже развившихся рецидивах показана трансплантация костного мозга. Другие методы лечения рецидивных ОМЛ пока находятся в стадии клинических испытаний.
Прогноз острого миелоидного лейкоза
Прогноз определятся разновидностью острого миелоидного лейкоза, возрастом больного, наличием или отсутствием миелодиспластического синдрома в анамнезе. Средняя пятилетняя выживаемость при разных формах ОМЛ колеблется от 15 до 70%, вероятность развития рецидивов – от 33 до 78%. У пожилых людей прогноз хуже, чем у молодых, что объясняется наличием сопутствующих соматических заболеваний, являющихся противопоказанием для проведения интенсивной химиотерапии. При миелодиспластическом синдроме прогноз хуже, чем при первичном остром миелоидном лейкозе и ОМЛ, возникшем на фоне фармакотерапии по поводу других онкологических заболеваний.
Миелобласты в крови что это значит
Миелолейкоз – это злокачественное заболевание крови и костного мозга, при котором образуется избыточное количество гранулоцитов (нейтрофилов, эозинофилов и базофилов) и их предшественников. Гранулоциты являются разновидностью лейкоцитов и отвечают за защиту организма от инфекций. При миелолейкозе они перестают выполнять свои функции и вытесняют из крови и костного мозга нормальные клетки крови, проникают в другие органы, нарушая их работу.
Существует множество разновидностей миелолейкоза, различаемых в зависимости от скорости развития патологического процесса, зрелости лейкозных клеток, изменений в хромосомах. Чаще всего выделяют два основных типа заболевания: острый миелобластный лейкоз и хронический миелоидный лейкоз.
При любом типе миелолейкоза применяется комплексное и достаточно длительное лечение. С каждым годом появляются все более эффективные методы терапии этого вида рака крови. Прогноз заболевания зависит от типа миелолейкоза, стадии болезни, на которой начато лечение, возраста пациента. В целом прогноз при остром миелолейозе благоприятный, особенно у детей. При хроническом миелолейкозе прогноз хуже, однако при своевременном начале лечения современные методы терапии позволяют надолго приостановить прогрессирование патологического процесса.
Лейкемия миелоидная, Ph-положительный хронический миелолейкоз, лейкоз гранулоцитарный, миелоидный лейкоз, миелолейкоз, миелоз, миеломная болезнь, острый миелобластный лейкоз, острый нелимфобластный лейкоз, острый нелимфобластный лейкоз у взрослых.
Childhoodacutemyeloidleukemia, adultacutemyeloidleukemia, acutemyeloidleukemia, acutemyeloblasticleukemia, acutegranulocyticleukemia, acutenonlymphocyticleukemia, chronicmyeloidleukemia, chronicgranulocyticleukemia.
Острый миелолейкоз обычно развивается стремительно – в течение нескольких недель. Его основными симптомами являются:
Хронический миелолейкоз развивается постепенно и проходит 3 стадии:
1) хроническая – симптомы обычно отсутствуют;
2) прогрессирующая – появляются слабость, боли в животе;
3) бластный криз – на этом этапе заболевание протекает со всеми симптомами острого миелолейкоза.
Общая информация о заболевании
Все клетки крови развиваются из единой стволовой клетки, которая затем дает начало миелоидным и лимфоидным стволовым клеткам. Из лимфоидных формируются лимфоциты, миелоидные дают начало предшественникам эритроцитов, тромбоцитов и миелобластам. Именно из миелобластов в результате цепочки последовательных делений формируются гранулоциты и моноциты.
Гранулоциты представляют собой разновидность лейкоцитов и называются так из-за своего вида – под микроскопом в них видны характерные темные гранулы, а также ядро, состоящее из нескольких сегментов. Существует несколько видов гранулоцитов – эозинофилы, базофилы и нейтрофилы. Моноциты также имеют сегментированное ядро, но их гранулы светлые. Основная задача гранулоцитов и моноцитов – борьба с вредными для организма чужеродными агентами (вирусами, бактериями).
При миелолейкозе костный мозг вырабатывает избыточное количество патологических гранулоцитов. Постепенно они вытесняют из крови и костного мозга нормальные клетки крови, что приводит к появлению характерных симптомов. При подавлении деления и роста эритроцитов возникают симптомы анемии – бледность, головокружение, слабость, – при подавлении роста тромбоцитов – нарушения свертываемости крови, частые кровотечения. Лейкозные клетки могут проникать в другие органы – печень, селезенку, лимфатические узлы, головной и спинной мозг, – вызывая нарушение их функций и характерные проявления. Патологические миелоидные клетки также могут образовывать скопления в надкостнице, средостении, органах желудочно-кишечного тракта (хлоромы).
Злокачественные нарушения кроветворения происходят из-за повреждения ДНК миелоидных клеток. ДНК клетки содержит информацию о ее росте, делении и гибели и представлена в клетке в виде хромосом. Факторы, повреждающие ДНК миелоидных клеток, до конца не изучены. Доказано вредное воздействие ионизирующей радиации, предшествующей химиотерапии, токсических веществ, например бензола. Выявлены также характерные изменения структуры и количества хромосом при определенных видах миелолейкоза.
При остром миелолейкозе часто наблюдаются повреждения 8-й, 15-й, 16-й, 17-й и 21-й хромосом. Характерным признаком хронического миелолейкоза считается наличие филадельфийской хромосомы. Она встречается в 95 % всех случаев хронического миелолейкоза и образована в результате присоединения к 22-й хромосоме участка 9-й хромосомы. Филадельфийская хромосома активирует синтез специальных белков тирозинкиназ, которые нарушают деление миелоцитов. В результате в крови появляются как зрелые гранулоциты, так и бластные клетки.
Острый миелолейкоз встречается как у взрослых, так и у детей. При нем в крови и костном мозге находят большое количество миелобластов. При хроническом миелолейкозе миелоидные клетки более зрелые и «специализированные». Средний возраст пациентов с хроническим миелолейкозом – 55-60 лет.
Кто в группе риска?
Лабораторные методы обследования
Другие методы обследования
Специфической профилактики миелолейкоза нет. Для своевременной диагностики необходимо регулярно проходить профилактические осмотры, а при возникновении тревожных симптомов сразу обращаться к врачу.