нарушения в регуляции инфламмасом связаны с рядом таких заболеваний как
Инфламмасома
Вы будете перенаправлены на Автор24
Понятие, состав и функция инфламмасом
Термин происходит от английского слова «inflammasome», которое в свою очередь связано с другим английским словом – «inflammation», что переводится как «воспаление».
Как уже было сказано, образуются инфламмасомы в миелоидных клетках. В составе инфламмасомы могут находиться такие белки, как NLRP, PYCARD, каспаза 1 и иногда каспаза 5, которая также известна как ICH-3 или каспаза 11.
Также встречаются инфламмасомы, сформированные рецепторами, которые содержат повторы, богатые лейцином и нуклеотид-связывающий олигомеризационный домен и AIM2-подобные рецепторы.
Состав каждой отдельно взятой инфламмасомы определяется активатором, который запустил ее формирование. Так, например, состав инфламмасом, образование которых было активировано двуцепочечной РНК (дцРНК), отличается от состава инфламмасом, которые были сформированы под действием асбеста.
Воспалительные реакции с участием инфламмасом играют важную роль в системе врожденного иммунитета, а нарушения их функционирования приводят к развитию различных заболеваний. Например, при подагре при контакте иммунных клеток с кристаллами мочевой кислоты активируются инфламмасомы криопиринового типа, вызывая характерное воспаление.
Главной функцией инфламмасом является обеспечение врожденного иммунитета, основанного на быстром распознавании и уничтожении клетками иммунной системы патогенных микроорганизмов, которые воспринимаются ими как чужеродные агенты и инородные тела.
Готовые работы на аналогичную тему
Распознавание патогенных микробов инфламмасомами осуществляется с помощью нескольких видов рецепторов:
Все эти рецепторы предназначены для опознавания паттернов, особых молекул на поверхности патогенов.
Механизм активации инфламмасом
Воспалительный каскад при активации инфламмасом выглядит следующим образом:
Роль инфламмасом в развитии различных заболеваний
Одним из распространенных тяжелых заболеваний, в развитии которых участвуют инфламмасомы, является болезнь Альцгеймера.
Это нейродегенеративное заболевание, характеризующееся накоплением в тканях головного мозга амилоидного бета белка (амилоид-β-пептида). Этот белок формируется в мозговой ткани регулярно путем расщепления белка амилоидного предшественника, но при нарушении данного процесса из этого белка могут образовываться неправильно упакованные прион-подобные олигомеры. Бета-амилоид – это первая выявленная молекула, ассоциированная с нейродегенеративными заболеваниями, которая была обнаружена при активации инфламмасомы мыши, что приводило к выработке интерлейкина-1β.
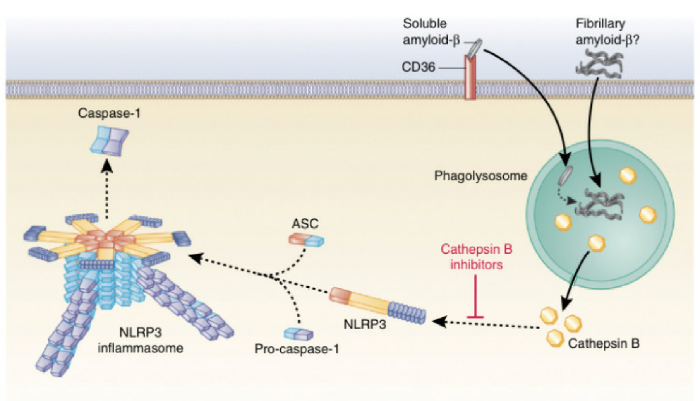
Опыты с мышами показали, что фибриллярный амилоид-β способствует индуцукции NLRP3 инфламмасомы, которая зависит от активации каспазы-1 через механизм, заключающийся в эндосомальном разрыве и высвобождении катепсина В в LPS-инициированные макрофаги подопытных животных.
При этом после введения ингибиторов катепсина В отмечалось значительное улучшение памяти и уменьшение накопления амилоидного белка, в связи с чем было сделано предположение о потенциальном терапевтическом подходе к лечению болезни Альцгеймера, в котором мишенью для воздействия является инфламмасома.
С нарушениями в регуляции инфламмасом также связаны и некоторые аутоиммунные заболевания, такие как сахарный диабет 1-го и других типов, подагрический артрит, о котором уже говорилось ранее, рассеянный склероз, воспалительная болезнь кишечника, витилиго, а также многие хронические воспалительные болезни. Все эти заболевания так или иначе связаны либо с недостаточной, либо с избыточной секрецией провоспалительных цитокинов, за которую ответственны инфламмасомы.
Инфламмасома — белковый комплекс, зачинщик воспаления
Воспаление — это защитный иммунный ответ, эволюционно установленный врожденной иммунной системой в ответ на вредоносные стимулы, такие как: патогены, мертвые клетки или раздражители, и оно жестко регулируется хозяином. Недостаточное воспаление может привести к хроническому течению инфекции, в то время как чрезмерное воспаление может привести к системным воспалительным заболеваниям.
Функция врожденного иммунитета зависит от распознавания ассоциированных с патогенами молекулярных структур (PAMP-pathogen-associated molecular patterns), полученных из патогенных микроорганизмов, и от связанных c дистресс-ассоциированными молекулярными структурами (DAMP), которые индуцируются в результате эндогенного стресса путем распознавания образов посредством зашифрованных зародышевых линий рецепторов (PRR-pattern-recognition receptors). Активация PRR с помощью PAMP или DAMPs триггеров посылает нисходящие сигнальные каскады и приводит к продукции интерферонов типа I (интерферон-α и интерферон-β) и провоспалительных цитокинов. Следует отметить, что воспаление, вызванное DAMP, которые особенно важны в воспалительных заболеваниях, называется стерильным, если это происходит в отсутствие каких-либо чужеродных патогенов.
Активация инфламмасом является ключевой функцией, опосредованной врожденной иммунной системой, а недавние успехи значительно увеличили понимание макромолекулярной активации воспалительных заболеваний. Несколько семейств PRR являются важными компонентами комплекса инфламмасом, включая нуклеотид-связывающий домен, лейцин-насыщенные повторы. При обнаружении определенных раздражителей соответствующий NLR или AIM2 может олигомеризоваться в каспаза-1-активирующий каркас. Активная каспаза-1 впоследствии участвует в расщеплении провоспалительного семейства цитокинов IL-1 в их биологически активные формы IL-1β и IL-18 и вызывает пироптоз — тип воспалительной гибели клеток.
Механизмы активации инфламмасом
NLRP3 inflammasome
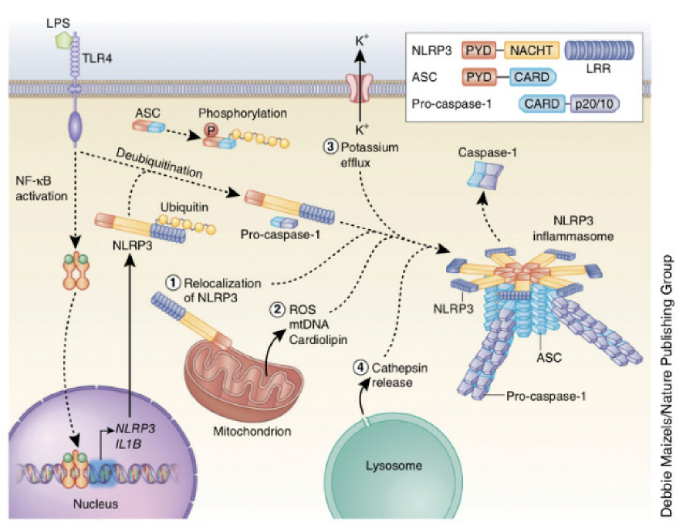
NLRP3 инфламмасома активируется в ответ на широкий набор стимулов, и этот факт приводит к теории, которая предполагает, что агонисты разной природы вызывают подобные процессы, ощущаемые NLRP3. Механизмы активации NLRP3, поддерживаемые большинством исследований, включают в себя: отток калия из клетки, образование митохондриальных активных видов кислорода (ROS — reactive oxygen species), транслокация NLRP3 в митохондрии, выделение митохондриальной ДНК, или кардиолипина, и выделение катепсинов в цитозоль после лизосомальной дестабилизации. Однако не все эти события индуцируются агонистами NLRP3, поэтому точный механизм активации NLRP3 все еще стоит под вопросом.
В дополнение к этому увеличение концентрации внутриклеточного кальция может активировать NLRP3 инфламмасому, но это не является обязательным требованием для всех агонистов NLRP3. Хотя многие опубликованные исследования поддерживают участие лизосомальных катепсинов, протеаз, которые расщепляют внутренние белки, при активации NLRP3 инфламмасом, важно отметить, что не обошлось без разногласий. В большинстве типов клеток NLRP3 должен быть инициирован, а примером такого инициирующего события является связывание липополисахарида (LPS) с TLR4. Известно, что инициация увеличивает клеточную экспрессию NLRP3 через cигнальный каскад NF-κB. Однажды возбудившись, NLRP3 может воздействовать на раздражители и собирать NLRP3 инфламмасому. Кроме того, ASC (apoptosis-associated speck-like protein containing a CARD) должен быть линейно убиквитирован (прим. — убиквитинирование — это посттрансляционное присоединение ферментами убиквитинлигазами одного или нескольких мономеров убиквитина с помощью ковалентной связи к боковым аминогруппам белка-мишени) для сборки NLRP3 инфламмасомы.
Существующие стимулы распознаются как агонисты NLRP3, которые индуцируют образование NLRP3 инфламмасомы, включающие в себя: АТФ, порообразующие токсины, кристаллические вещества, нуклеиновые кислоты, гиалуроновые и грибковые, бактериальные или вирусные патогены. Эти стимулы могут обнаружиться во время инфекции, или продуцироваться патогенами, или же отделиться от поврежденной клетки-хозяина. Кроме того, патологические состояния в организме могут способствовать формированию этих раздражителей в отсутствие инфекции; примером является образование воспалительных форм кристаллов холестерола. Недавние исследования показали, что NLRP3 NBD олигомеризует NLRP3 PYD, который служит в качестве каркаса для синтеза белков ASC через PYD-PYD взаимодействия.
Это приводит к преобразованию ASC в прион-подобную форму и преобразует короткие цепи в активные длинные нити ASC, которые имеют решающее значение в активации инфламмасомы. Pro-caspase-1 затем взаимодействует с ASC как CARD-CARD и формирует свои собственные прион-подобные нити, которые отделяются от нитей ASC. Близость белков прокаспазы-1 затем индуцирует аутопротеолитическое созревание прокаспазы-1 в активную каспазу-1. Кроме того, увеличение числа доказательств определило решающую роль для каспазы-8 при активации инфламмасомы и процессинга (созревания) про-IL-1β. Каспаза-8 представляет собой проапоптотическую протеазу, которая инициирует внешний апоптозный путь в ответ на внешние раздражители, такие как FasL и TNF (фактор некроза опухоли), и защищает от воспалительной формы клеточной смерти — некроптоза.
В настоящее время также признано, что каспаза-8 требуется для транскрипционной инициации и активации типичных и нетипичных NLRP3 инфламмасом в ответ на патогенные стимулы и лиганды, стимулирующие различные TLRs (Toll-like receptors). Таким образом, воспалительные заболевания, в которых образуются TLR-лиганды, могут привести к каспазой-8-опосредованному NLRP3 инициации или активации инфламмасомы. Важно отметить: каспаза-8 также имеет известную роль в активации NLRC4 и AIM2 инфламмасом, и даже было показано, что непосредственно влияет на процессинг про-IL-1β в комплексе неканонической каспаза-8-инфламмасома, вызванным связыванием некоторых внеклеточных патогенов в dectin-1.
AIM2 inflammasome
Не-NLR AIM2 может также образовывать каспаза-1-содержащую инфламмасому, но, в отличие от NLR, домен HIN-200 AIM2 может напрямую связывать его стимул, цитозольную dsDNA(двуцепочеченую ДНК), которые могут встречаться в цитозоле во время патогенной инфекции. Автоингибирующая конформация AIM2 создается взаимодействием из двух его доменов и освобождена от сахарофосфатного остова dsDNA. AIM2 не может взаимодействовать с ASC, если автоингибирование не прекращено, и, таким образом, AIM2 поддерживает себя в неактивном состоянии, пока его лиганд не свяжется. Интересно, что AIM2, похоже, не распознает определенную последовательность или структуры dsDNA, но вместо этого требуется цепочка dsDNA длиною не менее 80 пар оснований для оптимальной активации инфламмасомы. Аналогично NLRP3, олигомеризованные AIM2 собирают вокруг ядра ASC через PYD-PYD взаимодействия и преобразуют ASC в свою прионную форму, что приводит к образованию длинных PYD-PYD ASC нитей. Недавно была показана нетипичная инфламмасома AIM2 для защиты от Francisella novicida. F. novicida обнаруживается посредством cGAS и STING, индуцируя экспрессию транскрипционного фактора IRF1. IRF1 увеличивает экспрессию гуанилатсвязывающих белков, которые увеличивают внутриклеточное уничтожение бактерии. Этот процесс вызывает высвобождение dsDNA в цитозоль и индуцирует активацию AIM2 инфламмасомы.
Роль инфламмасомы в различных заболеваниях (например, болезнь Альцгеймера AD)
Источники
Нарушения в регуляции инфламмасом связаны с рядом таких заболеваний как
Какая бы беда ни была с организмом — инфекции, рак, инфаркт или ожирение — это всегда связано с воспалением, ответной реакцией организма на патоген или измененные белки наших клеток и т.д.
Воспаление (прежде всего хроническое воспаление) связано не только с болезнями, но и со старением, на скорость которого оно влияет.
Одно из центральных звеньев воспаления — инфламмасома. Именно она запускает сигнальный каскад, приводящий к клеточной смерти. Инфламмасомы — самособирающиеся белковые платформы, были обнаружены сравнительно недавно, в 2002 году. Сейчас известны разные типы инфламмасом. Например, NLRP1, NLRP3, NLRP6 и NLRC4 — все они представители семейства NLR-белков (NOD-like receptor).
Сейчас наибольший интерес ученых направлен на инфламмасому NLRP3 — она лучше изучена, и известно, что ее активирует большое количество разных стимулов. То есть она начинает свой танец смерти с полоборота.
NLRP3 — это белковый комплекс (включает несколько белковых доменов: лиганд-распознающий LRR домен, нуклеотид-связывающий NOD домен, и PYD-домен активирующий белок каспазу-1), который регулирует иммунный ответ.
Активация NLRP3 приводит к запуску сигнального каскада, в частности, каспазы-1, увеличивающей продукцию провоспалительных цитокинов IL-1β и IL-18, а также к активации «белка смерти» гасдермина (GSDMD), который образует поры в мембране воспаленной клетки и уничтожает ее в результате клеточной гибели, получившей название пироптоз [1].
Это и отличает NLRP3 от других инфламмасом, как наиболее перспективную мишень для модуляции врожденного иммунитета и воспаления при различных заболеваниях.
Преимущество ингибиторов инфламмасомы перед другими лекарственными средствами (например, блокаторами цитокинов) состоит в том, что они тормозят воспаление на более раннем этапе и препятствуют образованию провоспалительных цитокинов. А учитывая, что на NLRP3 влияет множество стимулов, применять ингибиторы инфламмасомы можно при самых разных заболеваниях, связанных с воспалением и повреждением клеток и тканей.
Когда инфламмасома проявляет чрезмерную активность, это может приводить к различным заболеваниям, таким как болезни Альцгеймера и Паркинсона, воспалительные заболевания кишечника, подагра, остеоартроз, заболевания печени, почек и сердечно-сосудистые патологии. Многие из этих болезней считаются возрастными. Кроме того, инфламмасома замечена и в случае с COVID-19 и при других тяжелых инфекциях, о чем мы писали ранее [2].
Нарушения в регуляции инфламмасом связаны с рядом таких заболеваний как
Повреждение нервной ткани инициирует патологический процесс, регулируемый в том числе факторами врожденного иммунитета и называемый нейровоспалением. В ходе этого процесса происходит активация клеток микроглии и астроцитов, несущих на своей поверхности специализированные «паттернраспознающие рецепторы» (pattern-recognizing receptors — PRR). Эти рецепторы связываются с определенными молекулярными конфигурациями (комплексами) микробных клеток или с высокомолекулярными (паттернгенерирующими) продуктами деструкции тканей организма. К семейству PRR принадлежат расположенные на внешней мембране клеток Toll-подобные рецепторы и цитозольные NOD-подобные рецепторы (также называемые NLR — nucleotide-binding leucine-rich repeat containing, т. е. связывающие нуклеотид и содержащие обогащенные лейцином повторы). NLR — это разновидность цитозольных сенсоров микробных молекул или молекулярных структур, образующихся при повреждении компонентов ткани. У человека описаны более 20 видов NLR. Наиболее интенсивно изучаются NLR, формирующие инфламмасомы: NLRP1, NLRP3, NLRC4, NLRC5, NLRP6, NLRP7 и NLRP12, а также не относящийся к NLR рецептор AIM2 (absent in melanoma-2) [1].
Термином «инфламмасома» обозначают макромолекулярные комплексы, образуемые разными видами NLR после их активации. Эти комплексы представляют собой молекулярную платформу для активации каспазы-1 (цистеиновой протеазы, опосредующей протеолиз и активацию цитокинов IL-1 и IL-18). В типичных случаях инфламмасома содержит 3 компонента: 1) белок NLR; 2) белок-адаптер с доменом активации каспазы — ASC (apo ptosis-associated speck-like protein containing a. caspase recruitment domain); 3) молекулы каспазы-1 (каспазы-эффектора).
Инфламмасомы обозначают по типу белка NLR, входящего в их состав. Из всех упомянутых типов инфламмасом наиболее изучена NLRP3, которая не только участвует в иммунном ответе против бактерий (золотистый стафилококк, гонококк), вирусов (vaccinia, influenza), грибов (Candida albicans) [2], но и распознает сигналы опасности (АТФ, кристаллы урата, повышенная генерация активных форм кислорода, амилоид-β (Аβ) [3], окисленные липопротеины низкой плотности и кристаллы холестерина [4]), опосредуя развитие стерильной воспалительной реакции при различных заболеваниях [5].
В молекуле NLRP3 выделяют 3 домена: LRR (С-концевой, содержащий обогащенные лейцином повторы), центральный домен NACHT (обладает АТФазной активностью и обеспечивает олигомеризацию протеинов) и N-концевой эффекторный (пириновый) домен — PYD. ASC состоит из N-концевого PYD и С-концевого домена рекрутирования каспазы (CARD). Каспаза-1 включает домен CARD и домен с каспазной активностью. Под действием стимула (сигнала «опасности») инфламмасомы начинают образовывать комплексы путем аутоолигомеризации через взаимодействие своими NACHT-доменами [6]. Домен LRR в составе NLRP3 служит для распознавания сигналов, запускающих процесс сборки активного инфламмасомного комплекса, в ходе которой различные компоненты инфламмасомы (NLRP3, ASC, прокаспаза-1) реагируют между собой аналогичными участками посредством гомофильных PYD-PYD и CARD-CARD взаимодействий (см. рисунок). 
Для начала сборки инфламмасомы NLRP3 необходимы два сигнала. Источник первого — инициирующего сигнала — продукты микроорганизмов и цитокины. TNFα, IL-1β и IL-1α, лиганды Toll-подобного рецептора (липополисахарид), или рецептора NLR (в частности, мурамил дипептид), вызывают активацию сигнального пути NF-κB и усиленную экспрессию белка NLRP3, а также обеспечивают up-регуляцию pro-IL-1β [4]. Второй сигнал передают внеклеточные молекулы АТФ, порообразующие токсины, кристаллы различных веществ (пирофосфат кальция [7], холестерин [8], микробные РНК [9]). Эти агенты активируют белок NLRP3, вызывая олигомеризацию его и затем — молекулы ASC, что заканчивается образованием инфламмасомы NLRP3. Внутри сформированной инфламмасомы аутопротеолиз прокаспазы-1 приводит к образованию активной каспазы-1, после чего про-IL-1β расщепляется до активной формы IL-1β, а про-IL-18 — до IL-18. Эти цитокины инициируют и стимулируют разнообразные сигнальные системы, которые управляют воспалительным ответом ткани. IL-1β играет важную роль в повреждении нейронов, а также стимулирует продукцию нейротоксичных факторов, таких как NO и TNF-α [10].
Активация каспазы-1 запускает программу пироптоза — особой формы гибели клетки в очаге воспаления. Пироптоз характеризуется быстрым разрушением плазматической мембраны, фрагментацией ДНК и выделением флогогенного содержимого цитозоля клетки во внешнюю среду [11]. По морфологическим признакам и механизмам развития пироптоз отличается от апоптоза, некроза и других форм гибели клетки. Установлено, что каспаза-1 расщепляет белок гасдермин D (GSDMD) с образованием гасдермин-N-домена GSDMD (GSDMD-NT), который непосредственно связывает фосфоинозитиды и кардиолипин [12, 13]. Затем GSDMD-NT ассоциируется с плазматической мембраной и олигомеризируется, формируя неселективные поры, которые приводят к набуханию и лизису клетки [13, 14]. Пироптоз может развиваться как в клетках глии, так и в нейронах под действием разнообразных стимулов [15, 16].
Высокие концентрации IL-1β и IL-18 регистрировали в цереброспинальной жидкости (ЦСЖ), ткани мозга и плазме крови пациентов с инфекцией ЦНС, травмой мозга, нейродегенеративными заболеваниями и рассеянным склерозом (РС) [17, 18]. Оба эти интерлейкина реагируют со специфическими рецепторами на внешней мембране клеток микроглии, астроцитов, нейронов, эндотелия и запускают сложный комплекс сигнальных событий, результатом которых становится вторичная экспрессия множества генов, регулирующих воспалительный процесс. IL-1β также вызывает пролиферацию макрофагов, микроглии и астроцитов [19]. Последние привлекаются в очаг повреждения или воспаления нервной ткани, выступая в роли характерного признака (сигнатуры) процесса.
Маловероятно, что при таком разнообразии факторов активации NLRP3-инфламмасомы все они непосредственно взаимодействуют с NLRP3. В настоящее время обсуждаются три основных механизма активации NLRP3-инфламмасомы: генерация активных (свободнорадикальных) форм кислорода (АФК), усиление выходящего из клетки тока К+ и разрыв мембраны лизосом [20].
Усиленная генерация АФК происходит, главным образом, в митохондриях [21]. Одним из сенсоров АФК является тиоредоксинвзаимодействующий протеин (TXNIP), который, связываясь с NLRP3, активирует его и способствует присоединению ASC и каспазы-1 с образованием активного комплекса NLRP3-инфламмасомы [22].
Дестабилизация лизосом, возникающая при фагоцитозе некоторых кристаллов и частиц, приводит к выходу содержимого этих органелл в цитозоль [25]. Один из компонентов лизосом — катепсин В стимулирует активацию NLRP3-инфламмасомы, а ингибитор этого фермента CA-074-Me ее подавляет [26].
Непропорциональная или длительная активация инфламмасом может представлять собой важный механизм нейровоспаления, лежащего в основе травматического и ишемического поражения головного мозга, нейродегенеративных заболеваний, а также ряда психических расстройств, включая болезни зависимости.
Травматическое повреждение мозга (ТПМ). Сильное механическое воздействие на головной мозг вызывает первичное повреждение и вторичный каскад реакций, приводящий к гибели компонентов ткани. Первичное повреждение сопровождается некрозом клеток, за которым следует вторичная волна альтерации, опосредованная эксайтотоксичностью выделяемых возбуждающих нейромедиаторов, активацией окислительного стресса, дисфункцией митохондрий, притоком астроцитов и микроглии в очаг повреждения, разрушением гематоэнцефалического барьера и воспалением [27]. Последнему придают большое значение в развитии вторичного повреждения [28].
Существенное повышение концентрации IL-18 отмечено в ЦСЖ у людей в течение первых 10 сут после черепно-мозговой травмы и у мышей в первые 7 дней после экспериментальной ТПМ [29]. Парентеральное введение мышам белка, связывающего и ингибирующего IL-18 (IL-18BP), за 1 ч до ТПМ снижало содержание IL-18 в ЦСЖ и улучшало неврологические показатели на 7-е сутки после травмы. В другом эксперименте [30] с механической травмой незрелого мозга у крыс и мышей на 7-е сутки их жизни, пик гибели нейронов приходился на период 12—24 ч после ударного воздействия. Это событие предварялось значительным повышением содержания мРНК и самого белка каспазы-1, IL-1β и IL-18 в ткани мозга в течение 2—12 ч после травмы. У трансгенных мышей, дефицитных по IL-18 (IL-18–/–), масштабы травматического повреждения мозга были меньше, чем у дикого фенотипа. ТПМ инициирует сборку NLRP3-инфламмасомы, экспрессию ASC, активацию каспазы-1, процессинг IL-1β и IL-18 в коре головного мозга [31].
Имеются сообщения [32], что NLRP1 также является важным компонентом воспалительного процесса при ТПМ, так как разрушение ткани мозга потенцирует синтез NLRP1-инфламмасомы, распад связанного с Х-хромосомой белка — ингибитора апоптоза (XIAP), активирует каспазу-1 и процессинг IL-1β. В другом исследовании [33] показали, что высокое содержание NLRP1 в ЦСЖ коррелирует с худшим прогнозом по сравнению с низким содержанием этого инфламмасом-образующего белка. Можно предположить, что NLRP1 и NLRP3 одновременно активируются в очаге травматического повреждения мозга. В этом случае оба типа инфламмасом можно рассматривать как мишень для разработки новых методов терапии последствий ТПМ.
Отмечена прямая корреляция между повышенными уровнями ДНК в плазме крови и тяжестью ТПМ [34]. Цитозольным сенсором для двухцепочечной ДНК (dsDNA) является AIM2 [34, 35]. AIM2-инфламмасома тоже может вовлекаться в патогенез ТПМ. В пользу этого свидетельствует то, что натриевая соль поли (дезоксиаденил-дезокситимидиловой кислоты) вызывала пироптоз эмбриональных корковых нейронов, а также повышенное содержание AIM2 и активированной каспазы-1 в нейронах, инкубированных в присутствии ЦСЖ от пациентов с ТПМ по сравнению с контрольной ЦСЖ [36].
Цереброваскулярные заболевания. Ишемический инсульт. Гибель нейронов и глиальных клеток головного мозга при ишемическом инсульте опосредована такими механизмами, как расстройство их энергетического обеспечения, окислительный стресс, эксайтотоксичность, действие возбуждающих нейромедиаторов, а также факторов воспалительного процесса [37, 38]. В последнем случае важную роль может играть NLRP3-инфламмасома.
В эксперименте введение мышам препарата «внутривенный иммуноглобулин» (IVIg) существенно сокращало зону ишемического инфаркта мозга и почти полностью нивелировало смертность. При этом IVIg уменьшал содержание NLRP3, NLRP1, каспазы-1, IL-1β и IL-18 в корковых нейронах [39]. В другом исследовании прерывистое голодание (ежедневно 16 ч в течение 4 мес), оказывая защитное действие на нервную ткань, вызывало снижение экспрессии NLRP1, NLRP3, а также предшественников IL-1β и IL-18 в очаге ишемического некроза посредством угнетения сигнальных путей NF-κB и MAPK [40]. В нейронах, подвергшихся кислородной и глюкозной депривации, накапливалась dsRNA (двухцепочечная РНК), которая активирует NLRP3 и продукцию провоспалительных цитокинов, способствующих прогрессированию воспаления и повреждению ткани при ишемии мозга [41].
Таким образом, регуляция инфламмасом на уровне пути NF-κB и транскрипции генов и их компонентов может служить мишенью для терапевтического воздействия в условиях ишемии мозга. Показано, что куркумин ингибирует зависимую от TXNIP активацию NLRP3-инфламмасомы, ослабляя стресс эндоплазматической сети и защищая нейроны от нейротоксичности глутамата во время ишемического инсульта [42]. Ресвератрол — природный фитоалексин, а также делеция гена TXNIP оказывают нейропротекторный эффект при эмболической модели инфаркта мозга у мышей за счет восстановления редокс-равновесия и подавления зависимой от TXNIP активации NLRP3-инфламмасом [43].
Другие компоненты инфламмасомного комплекса также рассматривают как точки контроля при ишемическом повреждении мозга. В одном из исследований эстроген и прогестерон снижали содержание ASC и NLRP3 в нейронах, окружающих зону инфаркта мозга [44]. Синтетический олигодезоксинуклеотид А151 уменьшал выраженность ишемического повреждения мозга за счет угнетения созревания каспазы-1 и IL-1β [45].
В экспериментах на трансгенных мышах получены данные об участии AIM2- и NLRC4-инфламмасом в развитии повреждения мозга при окклюзии средней мозговой артерии. Рецептор AIM2 взаимодействует с двухцепочечной ДНК (dsDNA) самого организма или патогенного агента. Он состоит из пиринового домена и HIN-домена. Таким образом, AIM2 нуждается в ASC для рекрутирования и активации каспазы-1 [46]. NLRC4 содержит CARD-домен и может непосредственно взаимодействовать с прокаспазой-1, однако в присутствии ASC образование NLRC4-инфламмасомы ускоряется [47]. У мышей нокаутных линий AIM2–/– и NLRC4–/– с выключенными генами соответственно AIM2 и NLRC4 масштабы повреждения мозга, величина активации клеток микроглии, локальное скопление нейтрофилов и расстройства поведения после окклюзии средней мозговой артерии были значительно менее выражены, чем у мышей дикого генотипа [48]. Аналогичные данные получены при сравнении линий ASC–/–, нокаутной по гену ASC, и дикого генотипа. Важно, что выключение гена NLRP3 не давало защитного эффекта в условиях данной модели ишемического повреждения мозга.
Геморрагический инсульт. Неврологическая дисфункция при кровоизлиянии в мозг обусловлена такими факторами, как образование гематомы, отек мозга, воспаление его, активация микроглии. Накапливаются сведения о том, что образование NLRP3-инфламмасомы вносит существенный вклад в этот процесс. С использованием экспериментальной модели геморрагического инсульта показано, что выключение гена NLRP3 с помощью коротких интерферирующих РНК ограничивало степень отека мозга, снижало активность миелопероксидазы (нейтрофильную и мононуклеарную инфильтрацию) в зоне гематомы, а также уменьшало тяжесть неврологических нарушений. Такой же эффект давало предварительное введение животным ингибитора генерации АФК в митохондриях Mito-TEMPO [49].
Ингибирование сигнального пути пуринергического рецептора P2X7R под действием бриллиантового синего G (BBG) может иметь терапевтическое значение при вторичном повреждении мозга на фоне мозгового кровоизлияния [50]. Усиление экспрессии микро-РНК miR-223 снижало скорость образования белка NLRP3 за счет связывания с 3′-нетранслируемой областью (3′UTR) соответствующей мРНК, что ограничивало нейровоспаление и улучшало неврологические функции после кровоизлияния в мозг у экспериментальных животных [51].
Еще один тип геморрагического инсульта связан с субарахноидальным кровоизлиянием (САК). Повреждение мозга в этих условиях опосредовано такими механизмами, как снижение церебрального кровотока, увеличение внутричерепного давления, окислительный стресс, апоптоз клеток и воспаление. Показано, что NLRP3-инфламмасома представляет собой ключевой регулирующий воспаление фактор при САК. Введение животным с этой формой патологии препарата миноциклина снижало активацию NLRP3-инфламмасомы и выраженность отека мозга на его раннем этапе. Этот эффект был опосредован ингибированием процесса образования АФК в митохондриях [52]. Кроме того, продемонстрирован down-регулирующий эффект обогащенного водородом изотонического раствора натрия хлорида при активации NLRP3-инфламмасомы в опытах по моделированию САК [53]. В последнем случае имело существенное значение торможение сигнального пути NF-κB. Протективное действие мелатонина при раннем повреждении мозга в условиях САК также связано с подавлением активации NLRP3-инфламмасомы и последующего апоптоза [54].
Опухоль мозга. Инфламмасомы, включая их NLRP3, играют определенную роль в канцерогенезе. Множество экзо- и эндогенных факторов, запуская хроническое воспаление, могут выступать как сигналы, способствующие образованию непосредственных промоторов канцерогенеза (ростовых факторов). Активация NLRP3-инфламмасомы служит промежуточным звеном этого процесса. Кроме того, NLRP3-инфламмасома подавляет активность натуральных киллеров — важного звена системы противоопухолевой защиты [55]. Клетки мультиформной глиобластомы подобно макрофагам вырабатывают и секретируют IL-1β, причем процессинг про-IL-1β осуществляется инфламмасомой NLRP3 и стимулируется самим же IL-1β [56]. В мультиформной глиобластоме IL-1β активирует фактор транскрипции Stat3, который способствует превращению клеток глиомы в более агрессивный мезенхимальный подтип. С помощью моделирования глиобастомы у мышей подтвердили, что ингибирование NLRP3-инфламмасомы тормозит рост опухоли и увеличивает срок выживаемость животных после радиационной терапии [57]. Генную сигнатуру NLRP3 предлагают рассматривать как перспективный биомаркер глиомы. В то же время для оценки значения NLRP3-инфламмасомы в опухолевой прогрессии глиом человека необходимы дальнейшие исследования.
Нейродегенеративные заболевания. Результаты ряда экспериментальных работ свидетельствуют, что активация нативного иммунитета и нейровоспаление составляют важное звено патогенеза нейродегенеративной патологии. В рамках этой парадигмы воспалительный ответ является следствием одних и причиной других патологических изменений в головном мозге [58]. При этом запуск воспалительного каскада обусловлен активацией NLRP3-инфламмасомы. Имеются факты, указывающие на существенный вклад IL-1β и IL-18 в развитие болезни Альцгеймера (БА) и нарушений когнитивной функции [59]. Причем источником IL-1β и IL-18 служат не только астроциты и клетки микроглии, но и нейроны, в которых обнаружили экспрессию инфламмасом, отвечающих за созревание этих интерлейкинов [60]. Повышение концентрации IL-1β отметили как в сыворотке крови, так и в ЦСЖ и ткани мозга пациентов с БА [61, 62]. Аналогично содержание IL-18 существенно увеличено в плазме крови пациентов с БА [63], а также в стимулированных мононуклеарных клетках и макрофагах периферической крови лиц, страдающих БА, по сравнению со здоровыми людьми [64]
Патогенез БА связан с накоплением β-амилоида (в виде сенильных бляшек), который способен активировать NLRP3-инфламмасому. Инкубация клеток микроглии в среде, содержащей фибриллярный Аβ, стимулировала секрецию IL-1β, активацию каспазы-1 и образование комплексов, содержащих ASC [25]. Микроинъекция Аβ в ткань головного мозга трансгенных мышей с инактивированными генами ASC (Asc–/–) и Casp1 (Casp1–/–) вызывала значительно меньшее локальное скопление клеток микроглии по сравнению с таковым у мышей дикого генотипа. Таким образом, IL-1β, производимый NLRP3-инфламмасомой, рекрутирует клетки микроглии в участки ткани, где имеются сенильные бляшки. В последующем показано, что у мышей трансгенной линии APP/PS1/Nlrp3–/–, т. е. имеющих в геноме два гена, связанных с семейными формами БА у человека, и дополнительно гомозиготных по нокаутному гену NLRP3, снижены активация каспазы-1 в головном мозге и плотность депозитов Аβ по сравнению с таковыми у мышей линии APP/PS1 [65]. В той же работе у лиц с БА, БА с ранним началом и у страдающих умеренными когнитивными нарушениями обнаружили признаки активации каспазы-1 в лизатах гиппокампа и фронтальной коры головного мозга, что указывает на роль NLRP3-инфламмасом в развитии этих форм патологии. В эксперименте при моделировании БА установлено, что ингибирование NLRP3 защищает животных от нарушений памяти и снижает отложение Аβ в ткани мозга [66].
Инкубация культуральных астроцитов с Аβ сопровождалась интенсивным зависимым от ASC синтезом IL-1β только после предварительного прайминга липополисахаридом, который стимулировал экспрессию про-IL-1β [67]. Действие только Аβ было недостаточным для экспрессии про-IL-1β, что указывает на потенциальную роль инфекции ЦНС в развитии БА.
Поиск гена-кандидата у представителей китайского этноса (северные хань) выявил два однонуклеотидных полиморфизма гена NLRP3 — rs2027432 и rs10754558, сочетание которых увеличивало риск развития БА с поздним началом [68].
NLRP3 не единственный рецептор семейства NLR, который имеет отношение к развитию Б.А. Инкубация in vitro культуры корковых нейронов с Аβ приводила к активации опосредованного NLRP1 и зависимого от каспазы-1 пироптоза [16].
В той же работе блокирование трансляции гена NLRP1 с помощью малых интерферирующих РНК (si-RNA) при моделировании БА на мышах линии APPswe/PS1d1 сопровождалось уменьшением активации каспазы-1, интенсивности пироптоза и объема когнитивной дисфункции. Ген NLRP1 активно экспрессируется в нейронах и олигодендроцитах [69].
Показано, что ингибирование экспрессии NLRC4 (другое обозначение — IPAF) в астроцитах после действия на них пальмитиновой кислоты вызывает снижение секреции IL-1β. Кроме того, в первичных нейронах существенно уменьшалось накопление β42-амилоида после содержания их в среде, полученной после инкубации обработанных пальмитатом астроцитов с блокированным NLRC4 [70]. В том же исследовании — в посмертных образцах мозга пациентов со спорадической формой БА — обнаружили повышенную экспрессию NLRC4 и ASC. Предполагается, что пальмитиновая кислота, потенциально имеющая отношение к патогенезу БА, стимулирует экспрессию NLRC4 в астроцитах [71].
Таким образом, большое число фактов свидетельствует, что активация инфламмасом имеет значение для инициации Б.А. Однако четкая связь между нарастанием тяжести БА и активацией инфламмасом прослеживается не всегда. Например, у трансгенных мышей с активным геном IL-1β проявляются постоянная экспрессия этого цитокина и инфильтрация гиппокампа иммунными клетками, но нарастания нейродегенерации обнаружить не удалось [72].
При болезни Паркинсона (БП) в нейронах образуются тельца Леви, состоящие в основном из фибриллярного белка α-синуклеина. Агрегаты последнего активируют NLRP3-инфламмасомы в клетках микроглии, действуя на TLR2-рецептор [73]. В той же работе показано, что агрегаты синуклеина фагоцитируются моноцитами, что приводит к дестабилизации лизосом с выделением катепсина В в цитозоль, а также к усилению генерации АФК. Как обсуждалось выше, дестабилизация лизосом и АФК являются сигналом для сборки NLRP3-инфламмасомы.
БП моделируют на мышах посредством введения нейротоксина 1-метил-4-фенил-1,2,3,6-тетрагидропиридина (МФТГ), который разрушает дофаминергические нейроны черной субстанции. Мыши нокаутной по гену NLRP3 линии резистентны к БП, инициируемой МФТГ [74]. Дофамин негативно регулирует активацию NLRP3 в клетках первичной микроглии и астроцитах с помощью сигнального пути D1-рецептора (DRD1) — цАМФ [74]. Более того, цАМФ непосредственно связывается с NLRP3 и способствует его деградации убиквитиновым комплексом, включающим Е3-убиквитин лигазу MARCH7. Мыши, дефицитные по гену DRD1, подвержены МФТГ-индуцированному нейровоспалению в большей степени, чем представители их дикого генотипа, что проявляется усиленной активацией NLRP3, увеличенной секрецией IL-1β и IL-18, а также более интенсивной потерей дофаминергических нейронов [74].
Другой способ моделирования БП — введение пестицида ротенона, который ингибирует электронно-транспортную цепь митохондрий и усиливает генерацию АФК. Действие ротенона не избирательно, однако в малых дозах он преимущественно повреждает дофаминергические нервные окончания нигростриатной системы [75]. Ротенон потенцирует активацию NLRP3, экспрессию ASC и образование IL-1β в культуре клеток микроглии после прайминга липополисахаридом [76]. Предварительная обработка микроглиальных клеток антиоксидантом с избирательным эффектом на митохондрии — митоапоцинином (mito-apocynin) — подавляла генерацию АФК и синтез IL-1β под действием ротенона, что указывает на роль АФК митохондрий в активации NLRP3-инфламмасомы.
При боковом амиотрофическом склерозе (БАС) мутации гена супероксиддисмутазы-1 приводят к образованию в нейронах агрегатов белков с нарушенной пространственной структурой (аномальной упаковкой). Такие белки играют ведущую роль в патогенезе БАС [77]. У пациентов, страдающих БАС, и у мышей, моделирующих данную патологию, в астроцитах обнаружили повышенную экспрессию NLRP3, ASC, активной каспазы-1, IL-1β и IL-18 [78]. Основным компонентом нейронных агрегатов белков у больных БАС является TDP-43 (ДНК-связывающий протеин трансактивного ответа-43, transactive response DNA-binding protein-43) [79]. Показано, что TDP-43 может активировать клетки микроглии снаружи через CD14-рецептор и инициировать сборку активной NLRP3-инфламмасомы [80]. В результате секретируемые микроглией IL-1β и другие токсичные медиаторы воспаления вызывают необратимое повреждение соседних мотонейронов.
Обсуждают роль NLRP3-инфламмасомы и при других нейродегенеративных заболеваниях — фронтотемпоральной деменции, болезни Гентингтона [58]. В патогенезе нейродегенеративных заболеваний активация нативного иммунитета может быть начальным звеном, что указывает на перспективу разработки противовоспалительной терапии для указанных форм патологии, даже если она не будет влиять на этиологический фактор.
Рассеянный склероз (РС) относят к нейровоспалительным демиелинизирующим заболеваниям. Наряду с дефектом Т-системы иммунитета в патогенезе РС следует выделить такие элементы, как разрушение гематоэнцефалического барьера, демиелинизацию, нарушение функции олигодендроцитов и нейронов. Клинические исследования свидетельствуют о связи увеличенной экспрессии каспазы-1, IL-1β и IL-18 с прогрессированием и тяжестью РС у пациентов [81]. IL-1β способствует дифференциации наивных T-лимфоцитов CD4+ в Th17 [82]. IL-18 был первоначально идентифицирован как фактор, потенцирующий секрецию IFNγ и, синергично с IL-12, способствующий дифференциации наивных T-лимфоцитов CD4+ в Th1-клетки. Оба типа Т-лимфоцитов (Th1 и Th17) играют важную роль в развитии патологии при РС.
Предварительные исследования на моделях РС показали, что наличие ассоциированных с инфламмасомой белков, таких как ASC, каспаза-1, IL-1β и IL-18, обостряет течение РС [83]. Более поздние работы позволили сделать вывод о существенном вкладе NLRP3-инфламмасом в ускорение демиелинизации. Это наблюдалось как при классическом, зависимом от Т-лимфоцитов и связанным с усиленной реакцией Th1- и Th17-клеток, моделировании РС, так и на купризоновой, не зависимой от Т-лимфоцитов, модели РС [84, 85].
Терапевтический эффект IFNβ при лечении РС связывают с его угнетающим действием на сигнальные пути инфламмасом NLRP3 и NLRP1, что сопровождается снижением продукции IL-1β [86]. Позже, на модели аутоиммунного энцефаломиелита подтвердили, что у мышей с нокаутированным геном NLRP3 терапия препаратом IFNβ неэффективна [87]. В клиническом исследовании у пациентов с положительным результатом лечения IFNβ обнаружили повышенную экспрессию NLRP3 и IL-1β, которую не выявили у пациентов с негативным результатом терапии этим препаратом [88]. Недавно синтезировали небольшую молекулу — МСС950. Она способна в наномолярных концентрациях селективно ингибировать активацию NLRP3. Введение MCC950 животным с аутоиммунным энцефаломиелитом (экспериментальная модель РС) приводило к снижению продукции IL-1β и уменьшало патологические неврологические проявления [89].
Показано, что в условиях стерильного нейровоспаления активатором NLRP3-инфламмасомы и NLRC4-инфламмасомы в клетках микроглии и астроцитах служит лизофосфатидилхолин — продукт деацилирования фосфатидилхолина клеточных мембран, тесно связанный с процессами нейродегенерации и демиелинизации [90]. При сравнении интенсивности скопления клеток микроглии и астроцитов в ткани мозга мышей различных линий, подвергнутых действию купризона (модель демиелинизации), выяснилось, что минимальный уровень клеточной инфильтрации по сравнению с диким генотипом был у трансгенной линии, нокаутированной по двум генам — NLRP3 и NLRC4; линии Nlrp3–/– и Nlrc3–/–, т. е. нокаутированные только по одному гену, занимали по этому показателю промежуточное положение.
В настоящее время из всех типов инфламмасом в патогенезе РС убедительно показана только роль NLRP3. Инфламмасомы NLRP1 и NLRC4 тоже могут иметь значение для развития РС, но долю их участия еще предстоит установить.
Инфекционные заболевания ЦНС. Имеется множество фактов о причастности NLRP3-инфламмасомы к развитию инфекционного процесса в ЦНС. Первую линию защиты от микробной инвазии формируют клетки микроглии. Инфламмасомы в них активируются под действием Legionella pneumophila [91]. Отмечено, что у нокаутированных по гену NLRP3 мышей, инфицированных пневмококком, менингит протекает менее тяжело, чем у животных дикого генотипа, и с меньшей выраженностью воспаления мозга [91]. Пневмолизин, порообразующий цитолизин пневмококка, индуцирует зависимый от каспазы-1 пироптоз и стимулирует образование IL-1β посредством АТФ-зависимой дестабилизации лизосом и усиленной генерации АФК [92]. Золотистый стафилококк также активирует NLRP3-инфламмасому по АТФ- и катепсин В-зависимым каналам [93].
Вирус японского энцефалита — частая причина энцефалита в Японии. При контакте с вирусом клетки микроглии усиливают секрецию как про-, так и противовоспалительных цитокинов, включая IL-1β и IL-18. Как показано на экспериментальных моделях и изолированных клетках микроглии, вирус японского энцефалита активирует NLRP3-инфламмасому через усиление выходящего тока К+ и генерацию АФК [94]. NLRP3-инфламмасоме приписывают ключевую роль в защите от вируса гриппа. Однако длительная активация NLRP3-инфламмасомы вызывает состояние гипервоспаления, способствуя развитию патологии и смерти [95]. При заражении вирусом гриппа экспрессия NLRP3 в мозге мышей усиливается [96]. То же происходит и у ВИЧ-инфицированных на стадии выраженного иммунодефицита (СПИД) [97]. Аналогично активацию в мозге NLRP3-инфламмасомы, которая сопровождалась гибелью нейронов и неврологическими симптомами, обнаружили у кошек при моделировании иммунодефицитного состояния на фоне вирусной инфекции, а также у трансгенных мышей — носителей гена Vpr (акцессорный белок ВИЧ-1) [97, 98].
Эпилепсия. При моделировании эпилептической активности путем внедрения электрода в миндалевидное тело обнаружили, что через 6 и 12 ч после периода эпилептического статуса в мозге крыс возрастало содержание IL-1β и компонентов NLRP3-инфламмасомы [99]. В то же время блокада экспрессии генов NLRP3 или каспазы-1 приводила к существенному уменьшению потери нейронов в зонах гиппокампа СА1 и СА3 спустя 6 нед после воспроизведения эпилептического статуса. Эти данные впервые продемонстрировали up-регуляцию NLRP3-инфламмасомы в мозге при формировании в нем эпилептогенного очага.
Депрессия. Исследования, выполненные в последнее десятилетие, позволяют сделать вывод, что нейровоспаление является важным компонентом патогенеза депрессии [100]. У пациентов, страдающих депрессией, в периферической крови и некоторых областях мозга обнаружили повышенное содержание провоспалительных цитокинов — IL-1β, IL-6, и IFNγ [101]. В посмертных образцах мозга жертв суицида, страдавших депрессией, выявили повышенную экспрессию IL-1β, TNFα, IL-6 и Toll-подобных рецепторов (TLR3 и TLR4) [102, 103]. Метаанализ результатов исследований привел к заключению, что IL-1β, TNFα и С-реактивный белок являются наиболее надежными биомаркерами воспалительного процесса у пациентов с депрессией [102]. Установлена связь между полиморфизмом генов IL-1β, TNFα, С-реактивного белка и наличием депрессии, а также результатами ее медикаментозного лечения [104]. Более того, введение провоспалительных цитокинов, например TNFα, или стимуляторов их синтеза, например эндотоксина, вызывало появление симптомов депрессии, которые ранее отсутствовали [105, 106]. Напротив, блокада эффектов цитокинов или компонентов сигнального пути, обеспечивающих развитие воспалительной реакции, таких как циклоксигеназа-2, вызывала редукцию проявлений не только соматогенной депрессии, но и большого депрессивного расстройства [107, 108].
У пациентов с биполярным расстройством (БР) наряду с признаками хронического воспаления часто обнаруживают дисфункцию комплекса I дыхательной цепи митохондрий [111]. Такая аномалия сопровождается усиленным образованием супероксидного аниона, который выходит из митохондрий и превращается в другие АФК, способные активировать NLRP3-инфламмасому. О потенциальной роли NLRP3-инфламмасомы в развитии депрессии свидетельствуют результаты исследований, показавших связь повышенной экспрессии NLRP3 и каспазы-1 в мононуклеарных клетках и высокой концентрации IL-1β и IL-18 в периферической крови пациентов с депрессией и корреляцию содержания IL-1β и IL-18 в крови с выраженностью депрессивной симптоматики [112, 113.]
Эксперименты на животных показали, что стрессорные воздействия повышают содержание IL-1β в нескольких областях мозга, в том числе в гиппокампе — ключевой структуре для таких функций, как память и эмоции [114]. В результате сложилось представление, что воспаление ткани гиппокампа и усиленная локальная продукция IL-1β вносят существенный вклад в механизм депрессивного расстройства [115].
В литературе есть также сообщения, что блокада рецептора для IL-1β (IL-1RI) редуцирует ангедоническое поведение при моделировании подобного депрессии состояния у животных — при хроническом непредсказуемом стрессе (ХНС) [116, 117]. ХНС — это форма моделирования депрессии на животных, при которой они подвергаются умеренным стрессорным воздействиям в непредсказуемой последовательности, например, 40-часовой водной депривации, пищевой депривации, воздействию высокой температуры окружающей среды (40 °С), нарушению цикла день—ночь, встряхиванию клетки в течение 30 мин, плаванию в холодной воде (5 мин при температуре 4 °С) и т. п. У крыс, подвергавшихся ХНС в течение 3 нед, появлялись признаки депрессивного и тревожного поведения, а в ткани гиппокампа нарастали концентрации внеклеточной АТФ, каспазы-1 и IL-1β [118]. Антагонисты пуринергического рецептора 7 (P2X7R) — активатора NLRP3-инфламмасомы, предотвращали депрессивное поведение, развивавшееся под влиянием ХНС, а агонисты P2X7R при их микроинъекции в гиппокамп провоцировали такое поведение и в отсутствие ХНС. У линии мышей, нокаутных по гену P2X7R, признаки депрессии в конце периода ХНС отсутствовали. Авторы эксперимента пришли к заключению, что депрессивное поведение под действием ХНС опосредовано активацией NLRP3-инфламмасомы в клетках микроглии гиппокампа сигналом, идущим от P2X7R-рецептора.
Связь между активацией NLRP3-инфламмасомы и депрессивным поведением была подтверждена и в другом эксперименте. Мышам вводили липополисахарид, после чего в ткани гиппокампа обнаружили повышение экспрессии NLRP3, ASC и каспазы-1, а также увеличение концентрации IL-1β, IL-18 и TNFα, уменьшение содержания IL-10 и повышенную активацию микроглии. Это сопровождалось признаками депрессивного поведения и нарушением когнитивной способности (дефицитом распознавания) [119]. Описанные изменения блокировались ингибитором NLRP3-инфламмасомы Ac-Tyr-Val-Ala-Asp-хлорметилкетоном.
При исследовании роли NLRP3-инфламмасомы в опосредовании эффектов иммобилизационного стресса мышей дикого генотипа и линии, нокаутной по NLRP3, фиксировали на 2 ч в течение 30 дней. В результате у животных дикого генотипа уменьшались предпочтение сахарозы и показатель социального взаимодействия, но увеличивалось время неподвижности в тесте с вынужденным плаванием [120]. Инициированное стрессом депрессивное поведение полностью нивелировалось у нокаутных мышей. Кроме того, выключение ген