Выберите формулу которая составлена неправильно если известно что валентность хлора равна i
Валентность хлора
Валентность хлора.
Валентность хлора:
Валентность (от лат. valēns – «имеющий силу») – способность атомов химических элементов образовывать определённое число химических связей.
Валентность – это мера (численная характеристика) способности химических элементов образовывать определённое число химических связей.
Значения валентности записывают римскими цифрами I, II, III, IV, V, VI, VII, VIII.
Валентность определяют по числу химических связей, которые один атом образует с другими.
Первоначально за единицу валентности была принята валентность атома водорода. Валентность другого элемента можно при этом выразить числом атомов водорода, которое присоединяет к себе или замещает один атом этого другого элемента. Определенная таким образом валентность называется валентностью в водородных соединениях или валентностью по водороду: так, в соединениях HCl, H2O, NH3, CH4 валентность по водороду хлора равна единице, кислорода – двум, азота – трём, углерода – четырём.
Валентность кислорода, как правило, равна двум. Поэтому, зная состав или формулу кислородного соединения того или иного элемента, можно определить его валентность как удвоенное число атомов кислорода, которое может присоединять один атом данного элемента. Определенная таким образом валентность называется валентностью элемента в кислородных соединениях или валентностью по кислороду: так, в соединениях K2O, CO, N2O3, SiO2, SO3 валентность по кислороду калия равна единице, углерода – двум, азота – трём, кремния – четырём, серы – шести.
С точки зрения электронной теории валентность определяется числом неспаренных (валентных) электронов в основном или возбужденном состоянии.
Известны элементы, которые проявляют постоянную валентность. У большинства химических элементов валентность переменная.
| Валентность хлора в соединениях | |
| I | NaCl, NaClO, Cl2O |
| III | NaClO2 |
| IV | ClO2 |
| V | KClO3 |
| VI | Cl2O6 |
| VII | KClO4, Cl2O7 |
Валентность хлора
Общие сведения о валентности хлора
Хлор – активный окислитель.
Молекула хлора двухатомна Cl2.
Валентность хлора в соединениях
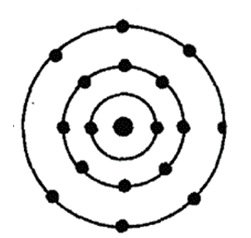
Хлор — семнадцатый по счету элемент Периодической таблицы Д.И. Менделеева. Он находится в третьем периоде в VIIA группе. В ядре атома хлора содержится 17 протонов и 18 нейтронов (массовое число равно 35). В атоме хлора есть три энергетических уровня, на которых находятся 17 электронов (рис. 1).
Рис. 1. Строения атома хлора.
Электронная формула атома хлора в основном состоянии имеет следующий вид:
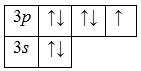
А энергетическая диаграмма (строится только для электронов внешнего энергетического уровня, которые по-другому называют валентными):
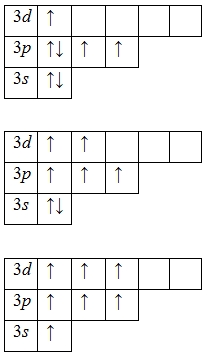
Наличие трех, пяти и семи неспаренных электронов в возбужденном состоянии свидетельствует о том, что хлор проявляет в своих соединениях валентности III (NaCl III O2), V (KCl V O3) и VI (KCl VII O4, Cl VII 2O7) (высшая валентность).
Формально хлор может проявлять валентности IV (ClO2) и VI (Cl2O6).
Примеры решения задач
| Задание | Какой объем хлора надо взять для реакции с 10 л водорода? Газы находятся при одинаковых условиях. |
| Решение | Запишем уравнение реакции взаимодействия хлора с водородом: |
Рассчитаем количество вещества водорода, вступившего в реакцию:
n (H2)= 10 / 22,4 = 0,45 моль.
Согласно уравнению, n (H2)= n (Cl2)= 0,45 моль. Тогда, объем хлора, вступившего в реакцию взаимодействия с водородом равен:
Тест с ответами: “Валентность”
1. Валентность:
а) способность присоединять атомы +
б) способность обмениваться атомами
в) способность отделять атомы
2. К элементам с постоянной валентностью относится:
а) сера
б) водород +
в) марганец
3. К элементам с переменной валентностью не относится:
а) железо
б) марганец
в) водород +
4. Какая связь происходит за счет образования общих электронных пар:
а) ковалентная связь +
б) металлическая связь
в) водородная связь
5. Какое из утверждений является верным:
а) валентность не имеет знака и может быть равной нулю
б) валентность имеет знак и не может быть равной нулю
в) валентность не имеет знака и не может быть равной нулю +
6. Как выглядит формула хлористого водорода, если известно, что валентность хлора равна единице:
а) HCl2
б) HCl +
в) HCl4
7. Какая валентность у марганца в данном соединении – Mn2O7:
а) II
б) IV
в) VII +
8. Какова валентность у углерода в формуле CH4:
а) IV +
б) VII
в) VI
9. Один из видов валентности:
а) непостоянная
б) временная
в) постоянная +
10. Один из видов валентности:
а) временная
б) переменная +
в) непостоянная
11. Сколько атомов водорода присутствует в молекуле воды:
а) 2 +
б) 3
в) 1
12. Степень окисления:
а) число, равное количеству электронов внешнего уровня атома
б) условный заряд атома, вычисленный на основе предположения, что соединение построено по ионному типу +
в) число химических связей, образуемых атомом химического элемента
13. Максимальная валентность атома фосфора:
а) V +
б) IV
в) +5
17. Этимологию термина валентность возможно отследить, начиная с этого года:
а) 1525
б) 1542
в) 1425 +
18. В этом году Хиггинс опубликовал работу, в которой высказал предположение о существовании связей между мельчайшими частицами вещества:
а) 1709
б) 1789 +
в) 1889
19. Точное и позже полностью подтверждённое понимание феномена валентности было предложено в этом году:
а) 1952
б) 1825
в) 1852 +
20. Решающую роль в создании теории валентности сыграл:
а) Менделеев
б) Кекуле +
в) Ломоносов
21. Огромным достоинством теории валентности явилась возможность наглядного изображения:
а) молекулы +
б) атома
в) частицы
22. В 1860-х годах появились первые:
а) молярные модели
б) молекулярные модели +
в) ионные модели
23. Первоначально за единицу валентности была принята валентность атома:
а) гелия
б) кислорода
в) водорода +
24. Валентность кислорода, как правило, равна:
а) трем
б) двум +
в) одному
25. У большинства элементов значения валентности в водородных и в кислородных соединениях:
а) равные
б) одинаковы
в) различны +
26. В монооксиде углерода валентность углерода равна:
а) 3
б) 2 +
в) 4
27. В соединениях с такими связями валентность атомов определяется числом образовавшихся двухэлектронных двухцентровых связей:
а) ковалентными +
б) валентными
в) ионными
28. В современной химии активно используется метод молекулярных орбиталей, в котором отсутствуют какие-либо аналоги понятия валентности:
а) частицы
б) ядра
в) атома +
29. В неорганической химии во многих случаях понятие валентности элемента теряет:
а) определённость +
б) однозначность
в) неопределенность
30. По валентности элементов можно составлять такие формулы соединений:
а) правдивые
б) истинные +
в) настоящие
Валентность хлора
Таблица валентностей химических элементов.Таблица валентности. Стандартные, высшие, низшие, редкие валентности, исключения. Максимальная валентность, минимальная валентность. Версия для печати
Валентность химических элементов – это способность у атомов химических элементов образовывать некоторое число химических связей. Определяется числом электронов атома затраченых на образование химических связей с другим атомом. Справочно: Электронные формулы атомов химических элементов.
Числовое значение положительной валентности элемента равно числу отданных атомом электронов, а отрицательной валентности – числу электронов, которые атом должен присоединить для завершения внешнего энергетического уровня. В неорганической химии обычно применяется понятие степень окисления, а в органической химии — валентность, так как многие из неорганических веществ имеют немолекулярное строение, а органических — молекулярное..
Степень окисления хлораСтепень окисления — это условный заряд атома в соединении: связь в молекуле между атомами основана на разделении электронов, таким образом, если у атома виртуально увеличивается заряд, то степень окисления отрицательная (электроны несут отрицательный заряд), если заряд уменьшается, то степень окисления положительная. Хранение хлораПроизводимый хлор хранится в специальных «танках» или закачивается в стальные баллоны высокого давления. Баллоны с жидким хлором под давлением имеют специальную окраску — болотный цвет. Следует отметить что при длительной эксплуатации баллонов с хлором в них накапливается чрезвычайно взрывчатый треххлористый азот, и поэтому время от времени баллоны с хлором должны проходить плановую промывку и очистку от хлорида азота. Электронная конфигурация атомаКакую электронную формулу имеет хлор? Валентность связана с особенностями внешнего энергетического уровня, поэтому запишем конфигурацию данного элемента. В невозбужденном состоянии на первом уровне у хлора располагаются всего два электрона, второй занимают восемь, на третьем уровне их 10 штук. Отметим, что на последнем уровне есть незаполненная d-орбиталь, которая и характеризует валентные возможности данного галогена. В данном случае валентность хлора равна I. Это характерно при взаимодействии с металлами (образуются хлориды). Высшую валентность VII хлор имеет в соединениях с неметаллами, например, в оксиде хлора (7), а также в хлорной кислоте. Приведем в качестве примеров формулы соединений хлора, в которых он проявляет такую валентность: HClO4, Cl2O7. Последний электронный уровень называют в неорганической химии валентным, так как именно он объясняет способность элемента вступать в химические взаимодействия с другими атомами. Примеры решения задачЗадание Какой объем хлора надо взять для реакции с 10 л водорода? Газы находятся при одинаковых условиях. Решение Запишем уравнение реакции взаимодействия хлора с водородом: Cl2 + H2 = 2HCl. Рассчитаем количество вещества водорода, вступившего в реакцию: n = V / Vm; n (H2)= V (H2) / Vm; n (H2)= 10 / 22,4 = 0,45 моль. Согласно уравнению, n (H2)= n (Cl2)= 0,45 моль. Тогда, объем хлора, вступившего в реакцию взаимодействия с водородом равен: V = n × Vm; V (Cl2) = n (Cl2) × Vm; V (Cl2) = 0,45 × 22,4 = 10,08л. Ответ Объем хлора равен 10,08 л. Тренировочное задание по химии для учащихся 8 класса по теме «Валентность»1. Определить валентности азота, фосфора, хлора, кремния и серы в следующих соединениях: NH3, PH3, HCl, H2S, SiH4, PCl3. 2. Составить формулы соединений с кислородом следующих элементов: азота (III), фосфора (V), магния (II), алюминия (III), натрия (I), серы (IV), железа (III). 3. Железо образует с кислородом оксиды состава FeO и Fe2O3. Установите валентность железа в каждом из двух соединений. Составьте формулы хлоридов железа (соединений железа с хлором), в которых железо будет проявлять такие же значения валентности, как и в указанных оксидах. 1. Определить валентность элементов в следующих соединениях: ZnS, Cu2S, Al2S3, K2S, P2S5, SnS2. 2. Составить формулы соединений с водородом следующих элементов: азота (III), хлора (I), фосфора (III), серы (II), кремния (IV), фтора (I), лития (I). 3. Золото образует с серой сульфиды состава Au2S и Au2S3. Определите валентность золота в каждом сульфиде. Составьте формулы оксидов золота, в которых золото будет проявлять такие же значения валентности, как и в указанных сульфидах. 1. Запишите формулы химических формул следующих соединений: 2. Выпишите формулы сложных веществ: 3. Определите валентность элементов в соединениях: 4. Составьте химические формулы соединений: б) железо (III) и кислород в) кремний (IV) и водород г) сера (VI) и кислород 1. Запишите формулы химических формул следующих соединений: 2. Выпишите формулы сложных веществ: 3. Определите валентность элементов в соединениях: 4. Составьте химические формулы соединений: б) углерод (IV) и водород в) алюминий и кислород г) сера (IV) и кислород Какие из перечисленных явлений относят к химическим? Замерзание воды Таянье льда Плавление свинца Ржавление гвоздя Горение газа Плавление алюминия Поднятие дрожжевого теста Кипение воды Помутнение микстуры лекарства Плавление воска Определите валентность каждого элемента в соединениях? Составьте формулы соединений серного ангидрида состоящего их атома серы (VI) и кислорода. И сероводородной кислоты, состоящей из водорода и серы (II). Рассчитайте массовые доли каждого элемента в этих соединениях, сравните массовые доли серы в этих соединениях? Определите валентность азота в следующих соединениях? Предложите схему разделения следующей смеси веществ? Вода+ Песок + Сахар+ Железные кнопки+ Бензин Контрольная работа № 1 по теме: «Основные химические понятия» Какие из перечисленных явлений относят к химическим? Таянье льда Горение дров Плавление меди Позеленее памятника Прогоркание масла Сжижение кислорода Прокисание молока Испарение спирта Замерзание воды Плавление стекла Определите валентность каждого элемента в соединениях? Расставьте коэффициенты в реакции и определите её тип? Составьте формулы соединений- оксида азота состоящего их атома азота(IV) и кислорода. И аммиака, состоящего из азота (III) и водорода. Рассчитайте массовые доли каждого элемента в этих соединениях, сравните массовые доли азота в этих соединениях? Определите валентность серы в следующих соединениях? Предложите схему разделения следующей смеси веществ? Вода+ Нефть+ Спирт+ Глина+ Железные опилки Если Вы считаете, что материал нарушает авторские права либо по каким-то другим причинам должен быть удален с сайта, Вы можете оставить жалобу на материал. Курс повышения квалификации Дистанционное обучение как современный формат преподаванияКурс профессиональной переподготовки Методическая работа в онлайн-образованииКурс повышения квалификации Современные педтехнологии в деятельности учителяИщем педагогов в команду «Инфоурок» Найдите материал к любому уроку, указав свой предмет (категорию), класс, учебник и тему:также Вы можете выбрать тип материала: Общая информацияПохожие материалыЗадание по химии для учащихся 8 класса по теме «Химические формулы»Контрольная работа № 1 «Строение атома и периодический закон Д. И. Менделеева» (11 класс)Коррозия металлов под деи ствием микроорганизмов.Рабочая программа элективного курса по химии в 11 классеКонспект урока «Предмет химии. Вещества»Презентация по химии на тему «Повторение и обобщение знаний по теме «Первоначальные химические понятия и теоретические представления»Административная контрольная работа по химии (I четверь)Не нашли то что искали? Воспользуйтесь поиском по нашей базе из Вам будут интересны эти курсы:Оставьте свой комментарийАвторизуйтесь, чтобы задавать вопросы. Минпросвещения разработает внеучебные курсы для школьников Время чтения: 1 минута Учителям предлагают 1,5 миллиона рублей за переезд в Златоуст Время чтения: 1 минута Путин поручил не считать выплаты за классное руководство в средней зарплате Время чтения: 1 минута ДНР полностью перешла на стандарты и программы России в образовании Время чтения: 1 минута Россияне чаще американцев читают детям страшные и печальные книжки Время чтения: 1 минута Утверждено стратегическое направление цифровой трансформации образования Время чтения: 2 минуты Подарочные сертификатыОтветственность за разрешение любых спорных моментов, касающихся самих материалов и их содержания, берут на себя пользователи, разместившие материал на сайте. Однако администрация сайта готова оказать всяческую поддержку в решении любых вопросов, связанных с работой и содержанием сайта. Если Вы заметили, что на данном сайте незаконно используются материалы, сообщите об этом администрации сайта через форму обратной связи. Все материалы, размещенные на сайте, созданы авторами сайта либо размещены пользователями сайта и представлены на сайте исключительно для ознакомления. Авторские права на материалы принадлежат их законным авторам. Частичное или полное копирование материалов сайта без письменного разрешения администрации сайта запрещено! Мнение администрации может не совпадать с точкой зрения авторов.
|