Гемосидерин что это в щитовидной железе
Предраковые поражения и опухоли щитовидной железы
Рак щитовидной железы считается очень серьезной и тяжелой болезнью, которая может привести к летальному исходу. Чаще всего он выявляется у людей в возрасте старше сорока лет, но в последнее время заболевание особенно «помолодело». Рак является серьезной патологией щитовидной железы, поэтому в последнее время постоянно оказывается в фокусе внимания онкологов и эндокринологов. Более, чем в 30 % случаев, рак щитовидной железы преодолевает пределы данного органа, и появляются отдаленные метастазы. Чтобы избежать риск заболеть раков щитовидной железы, необходимо вовремя отследить предраковую стадию. Важно понимать, что опухоли щитовидной железы — самые внешне благополучные и «коварные» заболевания. В 10% случаев после операции в гистологическом материале находят признаки злокачественной опухоли, в связи с чем возникает необходимость в проведении повторной расширенной операции с удалением прилежащих лимфатических узлов.
Сегодня предраковые изменения щитовидной железы определяются в 15-20% случаев при иммуногистохимическом изучении послеоперационного материала. Если высокодифференцированные опухолевые образования своевременно выявить и начать качественное хирургическое лечение, можно забыть о данном заболевании.
Предраковые заболевания щитовидной железы представлены третьей степенью дисплазии, которую сложно отличить от рака. Это можно сделать только после получения иммуногистохимических анализов, определяющих наличие онкомаркеров. Для этого проводится пункционная тонкоигольная биопсия узлов щитовидной железы.
Предраковые заболевания щитовидной железы представлены узловым и эндемическим зобом, доброкачественным новообразованием — аденомой, кистой. Стоит отметить наличие наследственной предрасположенности к заболеваниям, в том числе и злокачественным.
Атипия щитовидной железы при эндемическом зобе
Эндемический зоб считается предраковым заболеванием щитовидной железы, возникающим по причине воздействия внешних факторов и требующим постоянного контроля. Именно данная патология опасна по вероятности озлокачествления. В регионах, относящихся к эндемическим по зобу, зафиксировано значительное число случаев рака щитовидной железы. Внешние факторы, повышающие риск формирования предракового состояния в рак щитовидной железы обусловлены радиационным воздействием, несбалансированным питанием, вредом от бытовой химии. Например, после аварии на Чернобыльской АЭС произошло увеличение частоты заболеваемости раком щитовидной железы.
Атипия щитовидной железы при узловатом зобе
Диагностика рака щитовидной железы чаще всего происходит у пациентов с узловатыми формами зоба. Если фиксируют резкий и значительный рост узла, надо серьезно отнестись к этому. Это может быть свидетельством перехода в злокачественную форму заболевания.
Атипия щитовидной железы при кисте и аденоме
Под кистой понимается образование, возникшее в щитовидной железе и достигающее в размерах более 15 миллиметров. Кисту, саму по себе, нельзя относить к причинам рака, так как к нему приводят причины, из-за которых образовалась киста. Согласно статистике, озлокачествление кист приходится только на 10 % всех случаев.
Аденома считается зрелой, доброкачественной опухолью щитовидной железы. Сложно прощупать переход доброкачественного поражения в злокачественное, в связи с чем стараются удалить аденому хирургическим путем до того, как произойдет атипия клеток щитовидной железы.
Атипия щитовидной железы: признаки озлокачествления
В начале перехода атипии щитовидной железы в стадию рака не наблюдаются никакие характерные симптомы, и у врача есть возможность лишь прощупать уплотнение с достаточно четкими границами. Соответственно в случае обнаружения узла в щитовидной железе врач обязан исключать процесс озлокачествление и решать вопрос, касающийся удаления узлов.
Следует обратить пристальное внимание на самочувствие пациентов, жалующихся на общую нарастающую слабость, отсутствие или снижение аппетита, потерю веса. Как правило, опухолевидное образование разной плотности и размеров определяется на передней поверхности шеи в месте расположения щитовидной железы. Помимо этого, у пациента может возникнуть ощущение «тугого воротничка» — чувства сдавления в области шеи больного.
Предраковые поражения и опухоли щитовидной железы
Рак щитовидной железы считается очень серьезной и тяжелой болезнью, которая может привести к летальному исходу. Чаще всего он выявляется у людей в возрасте старше сорока лет, но в последнее время заболевание особенно «помолодело». Рак является серьезной патологией щитовидной железы, поэтому в последнее время постоянно оказывается в фокусе внимания онкологов и эндокринологов. Более, чем в 30 % случаев, рак щитовидной железы преодолевает пределы данного органа, и появляются отдаленные метастазы. Чтобы избежать риск заболеть раков щитовидной железы, необходимо вовремя отследить предраковую стадию. Важно понимать, что опухоли щитовидной железы — самые внешне благополучные и «коварные» заболевания. В 10% случаев после операции в гистологическом материале находят признаки злокачественной опухоли, в связи с чем возникает необходимость в проведении повторной расширенной операции с удалением прилежащих лимфатических узлов.
Сегодня предраковые изменения щитовидной железы определяются в 15-20% случаев при иммуногистохимическом изучении послеоперационного материала. Если высокодифференцированные опухолевые образования своевременно выявить и начать качественное хирургическое лечение, можно забыть о данном заболевании.
Предраковые заболевания щитовидной железы представлены третьей степенью дисплазии, которую сложно отличить от рака. Это можно сделать только после получения иммуногистохимических анализов, определяющих наличие онкомаркеров. Для этого проводится пункционная тонкоигольная биопсия узлов щитовидной железы.
Предраковые заболевания щитовидной железы представлены узловым и эндемическим зобом, доброкачественным новообразованием — аденомой, кистой. Стоит отметить наличие наследственной предрасположенности к заболеваниям, в том числе и злокачественным.
Атипия щитовидной железы при эндемическом зобе
Эндемический зоб считается предраковым заболеванием щитовидной железы, возникающим по причине воздействия внешних факторов и требующим постоянного контроля. Именно данная патология опасна по вероятности озлокачествления. В регионах, относящихся к эндемическим по зобу, зафиксировано значительное число случаев рака щитовидной железы. Внешние факторы, повышающие риск формирования предракового состояния в рак щитовидной железы обусловлены радиационным воздействием, несбалансированным питанием, вредом от бытовой химии. Например, после аварии на Чернобыльской АЭС произошло увеличение частоты заболеваемости раком щитовидной железы.
Атипия щитовидной железы при узловатом зобе
Диагностика рака щитовидной железы чаще всего происходит у пациентов с узловатыми формами зоба. Если фиксируют резкий и значительный рост узла, надо серьезно отнестись к этому. Это может быть свидетельством перехода в злокачественную форму заболевания.
Атипия щитовидной железы при кисте и аденоме
Под кистой понимается образование, возникшее в щитовидной железе и достигающее в размерах более 15 миллиметров. Кисту, саму по себе, нельзя относить к причинам рака, так как к нему приводят причины, из-за которых образовалась киста. Согласно статистике, озлокачествление кист приходится только на 10 % всех случаев.
Аденома считается зрелой, доброкачественной опухолью щитовидной железы. Сложно прощупать переход доброкачественного поражения в злокачественное, в связи с чем стараются удалить аденому хирургическим путем до того, как произойдет атипия клеток щитовидной железы.
Атипия щитовидной железы: признаки озлокачествления
В начале перехода атипии щитовидной железы в стадию рака не наблюдаются никакие характерные симптомы, и у врача есть возможность лишь прощупать уплотнение с достаточно четкими границами. Соответственно в случае обнаружения узла в щитовидной железе врач обязан исключать процесс озлокачествление и решать вопрос, касающийся удаления узлов.
Следует обратить пристальное внимание на самочувствие пациентов, жалующихся на общую нарастающую слабость, отсутствие или снижение аппетита, потерю веса. Как правило, опухолевидное образование разной плотности и размеров определяется на передней поверхности шеи в месте расположения щитовидной железы. Помимо этого, у пациента может возникнуть ощущение «тугого воротничка» — чувства сдавления в области шеи больного.
Запишитесь на прием, позвонив по номеру телефона Волгограда +7 (8442) 52-03-03 или онлайн.
Гемосидероз
БЕСПЛАТНАЯ КОНСУЛЬТАЦИЯ: поможем врачам и владельцам клиник выбрать оборудование для лечения гемосидероза
Оглавление
Гемосидерозы кожи (поттравматические гемосидерозы, пигментные капилляриты, геморрагически-пигментные дерматозы, пигментные пурпурные дерматозы) — это состояние, возникающее после травмы с попаданием крови в мягкие ткани (появлением гематомы), либо в результате заболеваний, общим проявлением которых является отложение гемосидерина в коже.
В нашей компании Вы можете приобрести следующее оборудование для лечения гемосидерозов кожи:
Гемосидерин представляет собой пигмент темно-желтого цвета, состоящий из оксида железа. Он образуется при распаде двух белков — гемоглобина и ферритина, например после попадания крови в ткани организма. Это может происходить после травмы (ушиба, инъекции), когда под кожей формируется гематома. Макрофаги не всегда успевают утилизировать «подкожную» кровь, в результате чего в области повреждения начинает скапливаться гемосидерин. Он формирует довольно стойкие локальные изменения окраски, которые могут вызывать эстетический дискомфорт у пациентов.
Гемосидерозами также являются следующие заболевания:
Ниже будет сделан упор на наиболее часто встречающихся состояниях и патологиях.
Этиология и патогенез
Посттравматический гемосидероз
Его появлению предшествует травма — ушиб, инъекция, надрез кожи и др. В результате кровь попадает в мягкие ткани, где происходит окисление гемоглобина и ферритина с последующим накоплением гемосидерина. Другими причинами и предрасполагающими факторами являются:
Пигментный прогрессирующий дерматоз Шамберга
Впервые описан в 1901 году английским дерматологом Джеем Франком Шамбергом. Основной причиной дерматоза считается повышенная проницаемость мелких сосудов и капилляров, располагающихся у поверхности кожи, через которые могут проходить эритроциты. Попав в ткани, они разрушаются, в результате чего из эритроцитов высвобождается гемоглобин и в дальнейшем — железо. Оно постепенно накапливается в определенной области, формируя специфический оттенок кожи.
Кольцевидная телеангиэктатическая пурпура Майокки
Описана итальянским дерматологом Доминико Майокки в конце XIX века. Этиологию заболевания связывают с несколькими факторами: повышение артериального давления, нарушение кровообращения в ногах, хронический спазм мелких сосудов, диапедез (просачивание) форменных элементов крови в ткани.
Лихеноидный пурпурозный пигментный дерматит Гужеро-Блюма
Описан дерматологами Генри Гужеро и Полом Блюмом в 1925 году. Точная причина заболевания неизвестна, определенную роль играет венозная гипертензия, системные болезни, инфекции, прием разжижающих кровь лекарственных препаратов, повышенная ломкость капилляров и др.
Экзематидоподобная пурпура Дукаса-Капетанакиса
Этиология неизвестна. Возможно участие в патогенезе повышенной проницаемости мелких сосудов с последующим диапедезом форменных элементов крови.
Клинические проявления
Посттравматический гемосидероз
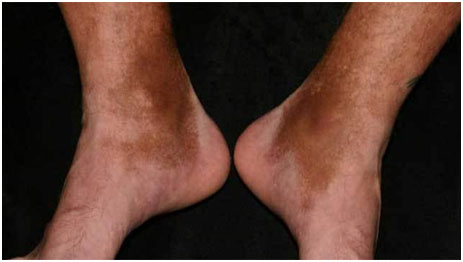
Пятна могут быть любого размера и формы, цвета от желтого до коричневого или черного. Они возникают в любой области тела (даже вокруг глаз), но чаще на нижних конечностях (рис. 1).
Пигментный прогрессирующий дерматоз Шамберга
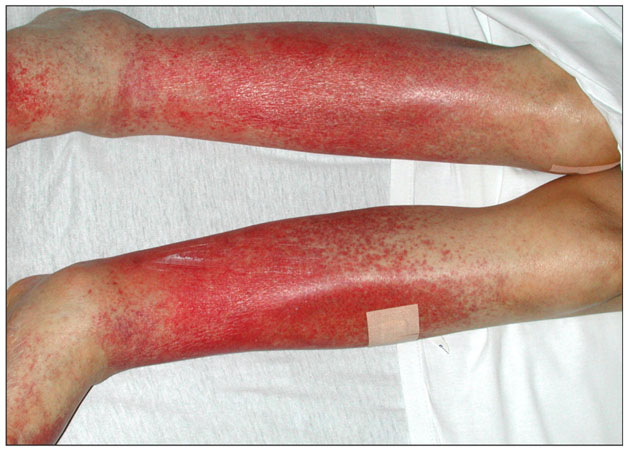
Проявляется в виде точек красно-коричневого или желто-бурого оттенка диаметром в несколько миллиметров, которые сам Шамберг сравнивал с размолотыми зернами кайенского перца. Эти точки чаще всего расположены на ногах, но могут встречаться и на других участках тела (рис. 2). Высыпания несколько возвышаются над поверхностью кожи и со временем могут сливаться в более крупные элементы неправильной формы. Постепенно они бледнеют, а на их месте формируются очаги кожной атрофии. Субъективные ощущения отсутствуют, в редких случаях может присутствовать небольшой зуд в области поражений.
Кольцевидная телеангиэктатическая пурпура Майокки
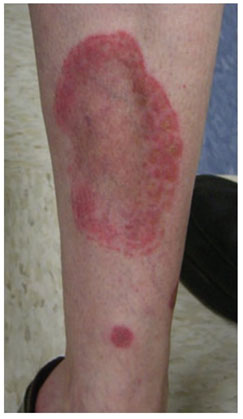
На коже появляются розоватые или красноватые пятна неправильной формы диаметром от одного до нескольких сантиметров. По мере их роста края пятен становятся более темными, а центр, наоборот, светлеет (рис. 3). Постепенно в центральной части развивается атрофия кожи с выпадением мелких волос. Субъективные ощущения отсутствуют.
Лихеноидный пурпурозный пигментный дерматит Гужеро-Блюма
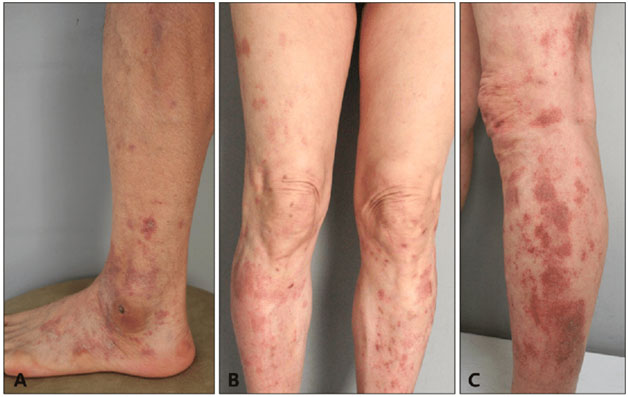
Характеризуется появлением небольших лихеновидных узелков с мелкими высыпаниями среди них. Отмечается точечное расширение мелких подкожных сосудов с локальным потемнением кожи из-за гемосидероза (рис. 4А). Типичная локализация — в нижней части ног, реже на бедрах и туловище.
Экзематидоподобная пурпура Дукаса-Капетанакиса
На коже голеней появляются отдельные петехии со склонностью к объединению в крупные пятна. Сперва они красного цвета, но постепенно становятся желтыми или коричневыми, бледнеют и со временем могут исчезнуть. Иногда поражения переходят на бедра, туловище и руки (рис. 4В,С). Дополнительно отмечаются явления паракератоза, зуд и гиперпигментация.
В табл. 1 представлены наиболее часто встречающиеся гемосидерозы и основные различия между ними.
Табл. 1. Дифференциальный диагноз наиболее часто встречающихся гемосидерозов кожи
Характеристика
Посттравматический гемосидероз
Пурпура Майокки
Дерматоз Шамберга
Дерматит Гужеро-Блюма
Пурпура Дукаса-Капетанакиса
Частота встречаемости
Самый частый тип гемосидерозов
Пик заболеваемости
В любом возрасте, но по мере старения организма вероятность растет
Подростки и молодые люди
Люди среднего возраста
Динамика поражений
Поражения возникают в месте предшествующей травмы. Чаще они бывают на ногах вследствие эндокринных патологий, нарушений работы венозной системы и других факторов
Поражения возникают сперва симметрично на ногах, далее могут распространяться на туловище и руки
Поражения чаще всего образуются симметрично в области голеней, но могут быть и только на одной ноге. Болезнь может затрагивать область бедер, ягодицы, туловище или руки
Чаще в нижней части ног и очень редко — бедрах и на туловище
На ногах, постепенно переходя на бедра, туловище и руки
Клинические проявления
Пятна различного размера и формы, цвета от желтого до коричневого или черного
Различное число кольцевидных эритематозных бляшек и пятен, часто с побледнением и атрофией в центре
Отдельные красно-коричневые пятна, не выступающие над кожей и выглядящие как зерна молотого кайенского перца
Мельчайшие лихеноидные папулы с тенденцией к объединению в крупные бляшки различного оттенка
Поражения, как правило, обширны. Пациенты жалуются на сильный зуд
Гистология
Расширение капилляров в сосочковом слое дермы, диапедез, пролиферация эндотелия капилляров с отложением гемосидерина в виде глыбок в межуточном веществе, гистиоцитах, эндотелиальных клетках. Незначительный неспецифический периваскулярный инфильтрат
Периваскулярная лимфоцитарная инфильтрация, которая распространяется на эпидермис. Вакуолярное изменение базального слоя, спонгиоз. Выявляются нагруженные гемосидерином макрофаги, внутри лихеноидного инфильтрата отмечается экстравазация эритроцитов
Периваскулярная мононуклеарная инфильтрация в верхней дерме, отек сосудистого эндотелия. Наличие экстравазальных эритроцитов и нагруженных гемосидерином макрофагов
Периваскулярная лимфоцитарная инфильтрация. Лихеноидная тканевая реакция. Отек эндотелия и сужение просвета мелких сосудов
Спонгиоз (отек шиповатого слоя эпидермиса) с воспалительными изменениями
Вероятность ремиссии
Течение чаще хроническое, но возможна спонтанная ремиссия
Возможна как спонтанная ремиссия, так и внезапное обострение заболевания
Лечение
Топические кортикостероиды, аппаратные методики
Заболевание является врожденным и проходит самостоятельно. Однако через некоторое время поражения могут появиться снова
Системные кортикостероиды, антигистаминные препараты, витамин С, ПУВА-терапия (см. ниже)
Терапия затруднена. Используются топические и системные кортикостероиды, антигистаминные и противозудные препараты. Рекомендовано ношение компрессионного трикотажа. Возможно применение ПУВА-терапии (см. ниже), гризеофульвина, циклоспорина А, витамина С и биофлавоноидов
Топические кортикостероиды и антигистаминные препараты
Рис. 1. Посттравматический гемосидероз на ногах (www.healthline.com; Photo: MavCure)
Рис. 2. Пигментный прогрессирующий дерматоз Шамберга (Chatterjee S. Schamberg disease: uncommon reaction to a common drug. CMAJ 2009; 181(12): E275)
Рис. 3. Кольцевидная телеангиэктатическая пурпура Майокки — в центре крупного очага заметна область осветления кожи (Hoesly F. J., et al. Purpura annularis telangiectodes of Majocchi: case report and review of the literature. Int J Dermato 2009; 48(10): 1129–1133)
Рис. 4. Дерматит Гужеро-Блюма (А) и пурпура Дукаса-Капетанакиса (В, С) (Kim D.H., et al. Characteristics and clinical manifestations of pigmented purpuric dermatosis. Ann Dermatol 2015; 27: 404–410)
Принципы лечения
На сегодняшний день считается, что ни одно лекарственное средство не имеет 100-процентной доказательной базы по эффективности при гемосидерозах. Таким образом, лечение этих болезней представляет собой проблему и является вызовом для врачей. При этом некоторые гемосидерозы могут проходить самостоятельно, а затем неожиданно рецидивировать.
В снижении воспаления и подавлении зуда при некоторых гемосидерозах эффективны кортикостероидные средства. Антигистаминные препараты угнетают эндогенную выработку гистамина и также снижают ощущение зуда у пациентов.
Определенную пользу несет назначение гризеофульвина, циклоспорина А, витамина С и биофлавоноидов. Есть данные о положительном влиянии ПУВА-терапии (psoralen (P) + ultraviolet A (UVA) = PUVA или ПУВА) — облучении кожи ультрафиолетом спектра А с предварительным приемом фотосенсибилизатора (псоралена) для большей эффективности светового воздействия.
В комплексной терапии гемосидерозов, особенно локальных подкожных отложений гемосидерина, вызванных предшествующей гематомой, могут применяться аппаратные методики, направленные на избирательное разрушение пигмента. Для локальной деструкции гемосидерина в эстетических целях может использоваться IPL-терапия: метод, при котором высокоинтенсивный импульсный свет разрушает пигмент, делая его более доступным для эвакуации в ходе фагоцитоза.
Цитологическая диагностика заболеваний щитовидной железы
Полный текст:
Аннотация
Цитологическая диагностика различных заболеваний человека широко применяется в современной медицине, особенно для ранней дооперационной диагностики новообразований разных органов и тканей. Тонкоигольная аспирационная пункционная биопсия с последующим микроскопическим исследованием ее цитограммы — одна из интегральных частей диагностической цитологии, в том числе при диагностике заболеваний щитовидной железы (ЩЖ). Методы, используемые для верификации различных вариантов тиреоидной патологии (пальпация, ультразвуковое исследование — УЗИ, сцинтиграфия, биохимические и иммунологические тесты и др.), далеко не всегда позволяют уточнить характер патологических изменений в ЩЖ. Например, холодные узлы (по данным сканирования) лишь в части случаев оказываются злокачественными новообразованиями ЩЖ, как и основная масса узловых зобов у больных из регионов, эндемичных по зобу; в большинстве случаев нет нужды в их оперативном удалении. И только микроскопическое исследование пунктатов ЩЖ, особенно ее узловых образований, позволяет уточнить диагноз и принять адекватное решение о характере лечебных мер. Тонкоигольная аспирационная пункционная биопсия ЩЖ относится к неинвазивным морфологическим диагностическим средствам, позволяющим практически со 100 % долей вероятности поставить правильный диагноз. Вместе с тем, поскольку ЩЖ является эпителиальным органом, в структурах которого клетки тесно «спаяны» между собой, клеточные связи рвутся с трудом, что крайне затрудняет получение информативного материала для последующего микроскопического исследования. Для облегчения процесса получения материала на иглу, которой производят пункционную биопсию, в Эндокринологическом научном центре РАМН стали наносить насечки на расстоянии примерно 0,5—0,7 см от острого конца иглы (канд. мед. наук А. В. Антонов), что позволяет брать материал, как гарпуном, без аспирации и получать обильный пунктат. При ишемизации пунктируемого участка железы удается получить обильный пунктат практически без примеси периферической крови (канд. мед. наук И. В. Пантелеев). Полученный таким образом материал наносят на обезжиренное предметное стекло и с помощью шлифованного предметного стекла получают мазок (аналогично мазку крови). Высушенные на воздухе мазки окрашивают по Маю—Грюнвальду— Гимзе. Ежегодно мы исследуем от 1,5 до 2,5 тыс. пункционных биопсий от больных с различной патологией. Информативность полученного материала во многом зависит от опыта и умения хирурга. Скудные пунктаты, как правило, малоинформативны и позволяют лишь описать пунктат без заключения о характере патологических изменений в ЩЖ. Обильные клеточные пунктаты из разных точек железы, особенно при подозрении на диффузную и (или) сочетанную патологию, дают возможность поставить окончательный диагноз.
Ключевые слова
Для цитирования:
Бронштейн M.Э. Цитологическая диагностика заболеваний щитовидной железы. Проблемы Эндокринологии. 1997;43(3):30-38. https://doi.org/10.14341/probl10393
For citation:
Bronstein M.E. Cytological diagnosis of thyroid disease. Problems of Endocrinology. 1997;43(3):30-38. (In Russ.) https://doi.org/10.14341/probl10393
Цитологическая диагностика различных заболеваний человека широко применяется в современной медицине, особенно для ранней дооперационной диагностики новообразований разных органов и тканей. Тонкоигольная аспирационная пункционная биопсия с последующим микроскопическим исследованием ее цитограммы — одна из интегральных частей диагностической цитологии, в том числе при диагностике заболеваний щитовидной железы (ЩЖ). Методы, используемые для верификации различных вариантов тиреоидной патологии (пальпация, ультразвуковое исследование — УЗИ, сцинтиграфия, биохимические и иммунологические тесты и др.), далеко не всегда позволяют уточнить характер патологических изменений в ЩЖ. Например, холодные узлы (по данным сканирования) лишь в части случаев оказываются злокачественными новообразованиями ЩЖ, как и основная масса узловых зобов у больных из регионов, эндемичных по зобу; в большинстве случаев нет нужды в их оперативном удалении. И только микроскопическое исследование пунктатов ЩЖ, особенно ее узловых образований, позволяет уточнить диагноз и принять адекватное решение о характере лечебных мер. Тонкоигольная аспирационная пункционная биопсия ЩЖ относится к неинвазивным морфологическим диагностическим средствам, позволяющим практически со 100 % долей вероятности поставить правильный диагноз. Вместе с тем, поскольку ЩЖ является эпителиальным органом, в структурах которого клетки тесно «спаяны» между собой, клеточные связи рвутся с трудом, что крайне затрудняет получение информативного материала для последующего микроскопического исследования. Для облегчения процесса получения материала на иглу, которой производят пункционную биопсию, в Эндокринологическом научном центре РАМН стали наносить насечки на расстоянии примерно 0,5—0,7 см от острого конца иглы (канд. мед. наук А. В. Антонов), что позволяет брать материал, как гарпуном, без аспирации и получать обильный пунктат. При ишемизации пунктируемого участка железы удается получить обильный пунктат практически без примеси периферической крови (канд. мед. наук И. В. Пантелеев). Полученный таким образом материал наносят на обезжиренное предметное стекло и с помощью шлифованного предметного стекла получают мазок (аналогично мазку крови). Высушенные на воздухе мазки окрашивают по Маю—Грюнвальду— Гимзе. Ежегодно мы исследуем от 1,5 до 2,5 тыс. пункционных биопсий от больных с различной патологией. Информативность полученного материала во многом зависит от опыта и умения хирурга. Скудные пунктаты, как правило, малоинформативны и позволяют лишь описать пунктат без заключения о характере патологических изменений в ЩЖ. Обильные клеточные пунктаты из разных точек железы, особенно при подозрении на диффузную и (или) сочетанную патологию, дают возможность поставить окончательный диагноз.
Наш многолетний опыт исследования пунктатов ЩЖ в сопоставлении в значительной части случаев с результатами последующего гистологического исследования операционного материала у тех же больных, а также с данными литературы позволяет нам описать подходы к оценке исследуемого пунктата и микроскопические критерии, в том числе цитологические, для диагностики известных заболеваний ЩЖ.
При микроскопическом исследовании окрашенных мазков пунктатов ЩЖ следует учитывать количество полученного материала, его клеточный состав, наличие коллоида, его состояние (плотность — густой, жидкий). При оценке паренхиматозного компонента пунктата — тиреоцитов (фолликулярных, или так называемых А-кле- ток) — следует учитывать их форму и размеры; моно- или полиморфность; изолированные они или формируют агрегаты; количество клеток в агрегате, отражающее пролиферативную активность клеток; особенности агрегатов и скоплений; наличие тяжей, клеточных шаров. Исследуя тиреоциты, нужно обращать внимание на текстуру цитоплазмы, ее окрашиваемость, наличие включений (их особенности и окрашиваемость), на признаки, отражающие функциональную активность клетки, в том числе на число, размеры и форму ядер, их положение в клетке; характер хроматина, распределение и окрашиваемость его частиц; наличие ядрышек, цитоплазматических включений, вакуолей, фигур митоза и признаков амитотического деления и оценивать ядерно-плазменное отношение. Особое внимание следует обращать на признаки, отражающие реакцию организма на патологический процесс: наличие транссудата, экссудата, фибрина, некротических масс, детрита, признака дистрофических изменений клеток; на присутствие крови в пунктате и ее происхождение — из кровеносных сосудов железы или из очагов кровоизлияний в ней. При правильном проведении пункционной биопсии и ишемизации пунктируемого участка периферическую кровь, как правило, берут только при диффузном токсическом зобе (ДТЗ), когда железа необычайно богато васкуляризирована. Наличие периферической крови в пунктате ЩЖ при ДТЗ — важный критерий в цитологической диагностике этого заболевания. Напротив, присутствие крови из очага кровоизлияния (измененные эритроциты, отсутствие среди них лейкоцитов, наличие макрофагов, в том числе гемосидерофагов) является, хотя и косвенным, но все же достоверным признаком наличия узла в железе, чаще всего — узлового зоба, реже — аденомы и еще реже — рака, хотя во всех этих случаях кровоизлияния могут иметь место. Реже всего они возникают при диффузных изменениях в железе, причем только в просвете кистозно-расширенного фолликула.
При обнаружении патологических (атипичных) клеток следует прежде всего определить их тип (тканевую принадлежность), изолированные они или формируют комплексы, взаимосвязь клеток в комплексах, в частности наличие признаков разобщения (дискомплексации) клеток; типы формируемых комплексов и структур, форму и размеры клеток и их ядер, ядерно-плазменное отношение, особенности цитоплазмы и ее тинкториальные свойства, наличие включений в цитоплазме, их число, размеры и тинкториальные свойства, характер распределения в цитоплазме; особенности ядер (форма, размеры, локализация); характер окрашивания хроматина, наличие ядрышек и их особенности, наличие цитоплазматических включений в ядрах, фигур митоза и другие особенности, способные дать информацию для решения вопроса о характере патологических изменений в железе, по крайней мере в пропунктированном образовании или фокусе.
Цитологическая диагностика заболеваний ЩЖ должна базироваться на данных макро- и микроскопического исследования пунктатов в сопоставлении с результатами клинического обследования, УЗИ и гормональными проявлениями заболевания. Цитологический и морфологический диагнозы по сути являются клинико-патологическим диагнозом. Несовпадение же клинического и цитологического диагнозов является результатом либо неадекватной оценки клинических и лабораторных проявлений заболевания, либо неадекватной оценки цитограммы пунктата, либо (что чаще всего имеет место) того, что патология ЩЖ сочетанная, оказывающая взаимное влияние друг на друга, в связи с чем клинические и лабораторные проявления оказываются как бы ’’смазанными», не отражающими истинный характер патологических изменений в железе. Так, аутоиммунный тиреоидит (АИТ), особенно атрофический вариант, на фоне которого имеются узловой токсический зоб или токсическая аденома, как правило, не сопровождается признаками нарушения функции ЩЖ (дефицит гормонов ЩЖ вследствие АИТ нивелируется избытком гормонов, вырабатываемых гиперфункцио- нирующим узлом), вследствие чего на периферии отсутствуют проявления нарушения гормонального статуса. В таких ситуациях только при сканировании в ЩЖ обнаруживают горячий (токсический) узел на фоне непоглощающей радиофармпрепарат тиреоидной ткани. УЗИ ЩЖ у таких больных выявит наличие узлового зоба или аденомы на фоне АИТ, но не объяснит отсутствия каких-либо клинических и лабораторных признаков нарушения функции ЩЖ. И только цитологическое исследование пунктатов обеих долей ЩЖ и пальпируемого узлового образования позволит поставить окончательный диагноз: АИТ в сочетании с узловым токсическим зобом (или токсической аденомой).
Цитологическая верификация заболеваний ЩЖ должна базироваться прежде всего на современной общепринятой классификации тиреоидной патологии, в соответствии с которой различают следующие ее варианты.
а) узловой зоб: солитарный, многоузловой или конгломератный, когда узлы интимно спаяны между собой; б) диффузный зоб;
г) смешанный зоб (диффузно-узловой или многоузловой).
а) болезнь Грейвса (ДТЗ, базедова болезнь);
б) АИТ (разнообразные клинические и морфологические варианты).
а) эмбрионального строения (солидного, трабекулярного, тубулярного);
б) микрофолликулярного строения;
в) фетального строения (характеризуется наличием участков, образованных микрофолликулами, разбросанными по рыхлой строме, чаще в центре узла; по периферии — фолликулы с коллоидом нормального диаметра);
г) фолликулярного строения (только из В-клеток);
д) папиллярного строения, в том числе папиллярные цистаденомы.
а) папиллярные раки;
б) фолликулярные раки;
в) смешанные папиллярно-фолликулярные раки;
г) низкодифференцированные, недифференцированные или анапластические раки.
а) С-клеточные аденокарциномы разнообразного строения;
б) медуллярный рак, нередко с амилоидозом стромы.
Зобная болезнь, возникающая вследствие дефицита йода, характеризуется прежде всего гипертрофией ЩЖ за счет как ее диффузного увеличения, так и формирования в ней узлов. Известны 2 основных механизма гипертрофии ЩЖ при дефиците йода — накопление коллоида в фолликулах и пролиферация фолликулярных клеток, степень выраженности которой зависит от уровня тиреотропного гормона в крови. Накопление коллоида приводит к растяжению фолликулов и уплощению фолликулярных клеток; при преобладании такого процесса развивается так называемый коллоидный зоб. При гиперстимуляции фолликулярных клеток тиреотропным гормоном усиливается пролиферация тиреоцитов; дифференцировки фолликулов не происходит или формируются мелкие фолликулы без коллоида, в результате развивается так называемый паренхиматозный зоб. Чаше всего мы сталкиваемся со смешанными вариантами зобов — коллоидными, в разной степени пролиферирующими. При пунктировании ЩЖ с такими зобами получают коллоид разной плотности (чаще густой) и тиреоциты. Соотношение этих компонентов отражает морфологический тип зоба: при преобладании коллоида говорят о коллоидном зобе, а при наличии значительного количества тиреоцитов, особенно с признаками пролиферации, — о пролиферирующем коллоидном зобе. При этом степень выраженности пролиферации весьма разнообразна — от частичной до резко выраженной. Подобное строение могут иметь как диффузные, так и узловые зобы. Цитологическими признаками пролиферации тиреоцитов являются обилие клеток, наличие укрупненных фолликулярных клеток с достаточно крупными молодыми ядрами; наличие 2 ядерных клеток и более; формирование такими клетками папиллярных и микрофолликулярных структур. Фигуры митоза никогда не встречаются.
Рис. I. Кистозный коллоидный узловой зоб. В пунктате — геморрагическая кистозная жидкость с примесью коллоида (в ячейках «сети» кистозной жидкости).
Отличительной особенностью узловых зобов является наличие собственной капсулы, отсутствующей в случае фокальных зобных изменений в ЩЖ. Цитологически верифицировать клетки, принадлежащие капсуле узла, невозможно. Поэтому цитологическая диагностика узлового зоба базируется на наличии признаков регрессивных изменений, которые часто возникают в них и крайне редко — в диффузных зобах. При пункти- ровании узлового зоба с регрессивными изменениями обычно получают кистозную жидкость с примесью коллоида (рис. 1). Микроскопически она выглядит по-разному: она может не окрашиваться, о ее присутствии судят по «сети» из складов, возникающих в результате денатурации белков при фиксации мазков; в складках обычно располагаются измененные эритроциты и гемоси- дерофаги. Примесь коллоида обусловливает окрашивание кистозной жидкости, причем тем интенсивнее, чем гуще коллоид. Геморрагическая кистозная жидкость характеризуется обилием измененных и (или) лизированных эритроцитов и ге- мосидерофагов (см. рис. 1). По соотношению сохранившихся, измененных и лизированных эритроцитов можно судить о давности кровоизлияния.
Цитологически, как и гистологически, удается верифицировать узловые зобы разнообразного строения: коллоидные, в пунктате которых преобладает густой коллоид, а эпителиальный компонент представлен небольшим количеством уплощенных и (или) мелких кубических тиреоцитов без признаков пролиферации; коллоидные, частично пролиферирующие узловые зобы, в которых эпителиальный компонент выражен в большей степени, чем в предыдущем варианте, часть клеток — с признаками пролиферации; пролиферирующий коллоидный зоб (эпителиальные клетки многочисленные, основная их часть или все они с признаками пролиферации). Во всех этих случаях могут иметь место выраженные в разной степени регрессивные изменения, приводящие к кистозной дегенерации узлов. Подобные морфологические варианты характерны и для диффузных зобов, которые верифицируются по сходству цитограмм пунктатов из обеих долей и отсутствию выраженных регрессивных изменений в сопоставлении с данными пальпации и УЗИ ШЖ.
Рис. 2. ДТЗ. В пунктате — секретирующий эпителий (капли секрета в апикальной части отдельных клеток и внеклеточно).
Ув. 200.
При различных вариантах зобной болезни в ЩЖ нередко наблюдаются морфологические признаки аутоиммунного процесса. Сводятся они обычно к очаговой лимфоидной инфильтрации стромы железы и реже — узловых зобов без признаков повреждения их паренхимы. Эти инфильтраты, как правило, немногочисленные, небольшие, представлены в основном зрелыми лимфоцитами. В этих случаях следует отмечать лишь факт лимфоидной инфильтрации стромы доли и (или) узла.
Цитологически удается разграничивать и известные морфологические варианты АИТ: классический (зоб Хашимото, хронический АИТ), хронический лимфоматозный тиреоидит, фиброзный тиреоидит и хронический лимфоматозный и(или) фиброзный струмит (аутоиммунный процесс, возникающий на фоне предсушествуюшей струмы). Классический вариант (рис. 4) характеризуется обильным клеточным пунктатом практически без примеси коллоида, представленным лимфоидными элементами различной степени зрелости с примесыо иммунобластов, плазматических клеток; фагоцитирующими гистиоцитами (макрофагами), в цитоплазме которых обнаруживаются остатки клеток, ядер и т. д.; единичными многоядерными гигантскими клетками типа клеток инородных тел; стромальными клетками или их ядрами; немногочисленными гистиоцитами и разнообразным, чаще небольшим, количеством тиреоцитов, основную массу которых могут представлять клетки Ашкенази (синонимы: клетки Гюртле, онкоциты, эозинофильные клетки, оксифильные клетки). Во всех случаях наблюдается преобладание лимфоидных элементов над эпителиальным компонентом.
Рис. 3. ДТЗ с явлениями хронического лимфоматозного струмита. В пунктате — обилие тиреоцитов и примесь лимфоидных элементов и стромальных клеток.
Рис. 4. АИТ, классический вариант. Пунктат обильный, представлен иммунобластами, лимфоцитами разной степени зрелости и плазматическими клетками.
В отличие от классического варианта АИТ хронический лимфоматозный тиреоидит (другой морфологический вариант АИТ) характеризуется более скудным пунктатом, представленным в основном зрелыми лимфоцитами с небольшой примесью клеток светлых центров лимфоидных фолликулов, большим количеством стромальных клеток и числом тиреоцитов, примерно равным числу элементов, основная масса которых уплощена и с признаками дистрофических изменений или трансформирована в клетки Ашкенази. В пунктате встречаются различного размера глыбки плохо окрашивающегося коллоида.
Для фиброзного варианта АИТ характерен прежде всего скудный пунктат, представленный небольшим количеством лимфоидных клеток, большей частью зрелых лимфоцитов, плазматических клеток, таким же количеством стромальных клеток или их ядер и еще меньшим числом эпителиальных клеток (тиреоцитов) — плоских, кубических или низких цилиндрических; коллоид встречается редко.
Хронический лимфоматозный струмит — вариант АИТ на фоне предсуществующего зоба, прежде всего диффузного или смешанного. Лимфоидная инфильтрация выражена в меньшей степени, чем при классическом варианте АИТ, но представлена теми же структурами и, следовательно, соответствующими лимфоидными стромальными клетками, а паренхиматозный компонент представлен разнообразными тиреоцитами, в том числе пролиферирующими, и разнообразным количеством коллоида разной плотности, отражающими наличие зобных изменений в железе в сочетании с аутоиммунным процессом (рис. 5). Последний может иметь место и в узловых зобах при диффузно-узловых вариантах зоба.
Цитологическая диагностика новообразований ЩЖ (доброкачественных и злокачественных) сложна и ставит перед собой по крайней мере 2 задачи: 1) дифференциальный диагноз с узловым зобом, поскольку любая опухоль подлежит обязательному хирургическому удалению в отличие от узловых зобов; 2) дифференциальный диагноз между доброкачественной и злокачественной опухолью, поскольку объем оперативного вмешательства на ЩЖ зависит от характера роста опухоли.
Рис. 5. Аденома эмбрионального строения (тубулярно-солидного). Пунктат обильный, опухолевые клетки мономорфные с гипертрофированными ядрами.
Рис. 6. Аденома микрофолликулярного строения. Пунктат обильный, опухолевые клетки мономорфные с гипертрофированными ядрами, формируют микрофолликулярные структуры.
Рис. 7. Аденома из клеток Ашкенази с кистозными изменениями. В пунктате на фоне кистозной жидкости с измененными эритроцитами — скопления из клеток Ашкенази — округло-полигональных с округлыми ядрами и мелкозернистой цитоплазмой.
Рис. 8. Папиллярно-фолликулярная аденокарцинома. Пунктат обильный, основная часть клеток изолированные (выраженная дискомплексация), в части ядер — цитоплазматические включения, вакуоли.
По существующим в настоящее время представлениям доброкачественные опухоли из С-кле- ток ЩЖ не формируются.
Злокачественные новообразования ЩЖ представлены в основном раками разной степени дифференцировки из всех типов тиреоидных клеток — А, В и С. Наиболее часто встречаемыми в эндокринологической практике являются раки из А- клеток папиллярного, фолликулярного или смешанного строения, а также фолликулярно-солидные раки. Все они, за исключением папиллярных раков, растущих в кисте, представляют собой фокусы опухолевого роста, лишенные собственной капсулы. При пунктировании этих новообразований получают обильный клеточный материал, цитограмма которого характеризуется большим количеством изолированных клеток или комплексов опухолевых клеток (рис. 8) — гипертрофированных атипичных тиреоцитов с четко выраженными клеточными границами, резко базофильной цитоплазмой, гипертрофированными ядрами, нередко содержащими ядрышки. Ядра молодые, пузыревидые, с нежной хроматиновой сетью, располагаются центрально или эксцентрично в зависимости от формы клетки. В части ядер имеются цитоплазматические включения и структуры, напоминающие спилы ствола дерева (рис. 9), а также вакуоли. В комплексах, представляющих собой обрывки стенок фолликулов, мелкие фолликулы, солидные опухолевые структуры, отмечается выраженная дискомплексация клеток, приводящая к их разобщению, в результате чего в пунктате имеется значительное количество изолированных клеток. Дискомплексация клеток и наличие в ядрах цитоплазматических включений — цитологические признаки, патогномоничные для А-клеточных раков ЩЖ. Для цитограмм пунктатов папиллярных раков характерно также присутствие папиллярных структур и наличие в ядрах, помимо цитоплазматических включений, складок или бороздок вдоль длинной оси ядра. Если опухоль представляет собой склерозирующую аденокарциному, в пунктате встречаются и стромальные клетки, а если опухоль растет в кисте (основная масса папиллярных раков), в пунктате имеется кистозная жидкость с примесью плохо окрашивающегося коллоида. В случае папиллярной цистаденокарциномы — редкого варианта папиллярного рака ЩЖ — диагноз ставят на основании присутствия в пунктате, помимо обрывков опухолевых сосочков с массивной рыхлой стромой, покрытых большей частью одним слоем относительно мелких округло-полигональных опухолевых клеток со всеми описанными выше признаками и подобных изолированных клеток, также кистозной жидкости, содержащей макрофаги, детрит, дистрофически-измененные опухолевые клетки и т. д.
Рис. 9. Фолликулярно-солидная аденокарцинома. Комплекс опухолевых клеток. В одном из ядер — включение в виде спила ствола дерева.
Рис. 10. С-клеточный рак. Основная масса опухолевых клеток с зернистой цитоплазмой. В части из них наблюдается вакуолизация цитоплазмы.
Раки из В-клеток по структуре мало отличаются от раков из А-клеток, вместе с тем цитологически они труднее диагностируются из-за отсутствия выраженных цитологических признаков, отличающих их от доброкачественных новообразований из В-клеток. Окончательный диагноз ставится лишь при гистологическом исследовании удаленной опухоли. Цитологически же по описанным ранее признакам можно лишь верифицировать опухоль из В-клеток без уточнения характера ее роста.
Наиболее сложно цитологически дифференцировать опухоли из С-клеток из-за полиморфно- сти опухолевых клеток как в пределах одной опухоли, так и в разных опухолях в связи с разнообразием структур, формируемых этими клетками (железистые, папиллярные, перицитарные и т. д.). Эти опухоли возникают как спорадические варианты и как часть синдромов множественных эндокринных опухолей. Как и большинство раков из А- и В-клеток, раки из С-клеток не имеют собственной капсулы. Пунктаты С-клеточных опухолей обильные клеточные. Большинство опухолевых клеток изолированные, морфология их варьирует от опухоли к опухоли, от веретеновидных до округло-полигональных, иногда они напоминают плазматические клетки с четкими клеточными границами или без таковых, с центрально или эксцентрично расположенными вытянутыми или округлыми ядрами, с обильной или скудной, гомогенной или мелковакуолизированной, светлой или темной цитоплазмой, богатой мелкими метахроматически окрашивающимися гранулами (так называемые зернистые клетки; рис. 10). Все эти клетки независимо от формы и размеров объединяют нерезко выраженная базофилия цитоплазмы, наличие в ядрах 1—2 мелках ядрышек. Встречаются варианты с многоядерными опухолевыми клетками. В умеренно-дифференцированных С- клеточных раках, наиболее типичным представителем которых является медуллярный рак, опухолевые клетки четких структур не формируют, они ’’собираются» в пласты, гроздья, тяжи, войлокоподобные структуры; патогномичным для них следует считать наличие амилоида в виде гранул или глыбок различного размера, располагающихся внутри- или внеклеточно и окрашивающихся метахроматически в ярко-малиновый цвет (при окраске основными красителями типа азура II). В более высокодифференцированных раках из С- клеток опухолевые клетки могут формировать и описанные выше структуры, что позволяет относить их к аденокарциномам. И в таких опухолях может иметь место отложение амилоида в строму, но в значительно меньшем количестве, чем в медуллярных раках.
Острый тиреоидит цитологически диагностируется по тем же признакам, что и острое воспаление любой другой локализации. Гранулематозные процессы в ЩЖ могут быть как первичными (подострый тиреоидит де Кервена вирусной этиологии), так и вторичными при генерализации специфического процесса с вовлечением ЩЖ в патологический процесс (туберкулезный, сифилитический и т. д.). Цитологическая диагностика подострого тиреоидита базируется на наличии в пунктате клеточного детрита, излившегося коллоида, немногочисленных дистрофически-измененных тиреоцитов и (или) тиреоцитов с признаками пролиферации в сочетании с многоядерными гигантскими клетками инородных тел, многочисленными гистиоцитами, клетками типа эпителиоидных и немногочисленных фагоцитирующих макрофагов, а также лимфоидных элементов (рис. 11). Специфические тиреоидиты характеризуются теми же цитологическими особенностями, что и соответствующие процессы в других органах и тканях.
Рис. 11. Подострый тиреоидит де Кервена. Фон мазка — клеточный детрит, коллоид. Имеются скопления тиреоцитов (пролиферирующих или с дистрофическими изменениями); много гистиоцитов и стромальных клеток.
Тиреоидит Риделя — редкая патология ЩЖ, его приходится прежде всего дифференцировать с фиброзным вариантом АИТ. В отличие от последнего при тиреоидите Риделя в пунктате редко встречаются тиреоциты, отсутствуют клетки Ашкенази и клетки центров размножения лимфоидных фолликулов.
Резюмируя изложенное, следует подчеркнуть, что цитологическая диагностика различных заболеваний ЩЖ возможна, поскольку каждый вариант тиреоидной патологии имеет характерные микроскопические, в том числе цитологические, особенности, отражающие патологические изменения в ЩЖ при соответствующих ее заболеваниях. Вместе с тем она возможна и достоверна при условии получения во время проведения пункционной биопсии информативного материала, достаточно обильного, в котором представлены все возможные структуры и типы клеток, а также содержимое полостей. Трудности цитологической диагностики заболеваний ЩЖ обусловлены прежде всего тем, что в большинстве случаев мы сталкиваемся с сочетанными вариантами тиреоидной патологии. Однако если цитолог располагает хорошими пунктатами (из обеих долей, раздельно из образований и прилежащей к ним ткани соответствующей доли), микроскопическое исследование таких пунктатов позволяет достоверно оценить практически весь спектр патологических изменений, возникающих в железе, и поставить окончательный диагноз. Скудные пунктаты, особенно из одного патологического очага, позволяют цитологу лишь описать особенности полученного материала без уточнения характера патологических изменений в железе. Поэтому следует стремиться к получению обильных и информативных пунктатов без примеси или с минимальной примесью периферической крови, из-за которой клетки из железы нередко деформируются, что крайне затрудняет их микроскопическую идентификацию и исследование. Данные цитологического исследования пунктатов ЩЖ следует сопоставлять прежде всего с данными клинического обследования и УЗИ больных, поскольку это может позволить, с одной стороны, оценить результаты микроскопического исследования пунктатов с клинических позиций, а с другой — понять и объяснить часто несовпадающие результаты клинических и цитологических исследований, что в конечном счете позволяет уточнить диагноз и выбрать адекватную терапию.