лейкоцитарная инфильтрация в гистологии что значит
Цитологическая диагностика заболеваний шейки матки
Цитологическое исследование мазков из шейки матки позволяет оценить состояние слизистой оболочки, наличие или отсутствие признаков патологических процессов (реактивных, предопухолевых, опухолей). При выявлении другими лабораторными методами инфекционного агента (вирус папилломы человека, бактериальные и паразитарные инфекции), цитологический метод позволяет оценить реакцию организма на инфекционный агент, наличие или отсутствие признаков повреждения, пролиферации, метаплазии или трансформации эпителия. Возможно также при исследовании мазка определить причину изменений эпителия (наличие воспаления с ориентировочным или уверенным определением патогенной микробиоты (микрофлоры), патологических процессов, связанных с гормональным, лекарственным, механическим, лучевым воздействием на организм женщины и шейку матки, состояний, чреватых опасностью возникновения дисплазии и рака шейки матки, а при их развитии установить правильный диагноз. В связи с этим цитологическое исследование применяют как при скрининге (мазки с визуально нормальной шейки матки), так и при наличии видимых при гинекологическом осмотре изменений слизистой оболочки.
Получение материала
Рак шейки матки чаще всего развивается в зоне трансформации, ему предшествуют фоновые процессы и внутриэпителиальные поражения (дисплазия эпителия), которые могут располагаться на небольших участках, поэтому важно, чтобы материал был получен со всей поверхности шейки матки, особенно из зоны стыка плоского и цилиндрического эпителия. Число измененных клеток в мазке бывает различным, и если их мало, то увеличивается вероятность, что патологические изменения могут быть пропущены при просмотре препарата. Для эффективного цитологического исследования необходимо учитывать:
Материал из шейки матки должен брать врач-гинеколог или (при скрининге, профилактическом осмотре) хорошо обученная медицинская сестра (акушерка).
Важно, чтобы в мазок попадал материал из зоны трансформации, так как около 90% опухолей исходит из зоны стыка плоского и цилиндрического эпителия и зоны трансформации и только 10% из цилиндрического эпителия цервикального канала.
С диагностической целью материал получают раздельно из эктоцервикса (влагалищной порции шейки матки) и эндоцервикса (цервикального канала) с помощью шпателя и специальной щетки (типа Cytobrush). При проведении профилактического осмотра используют Cervex-Brush, различные модификации шпателя Эйра и другие приспособления для получения материала одновременно из влагалищной части шейки матки, зоны стыка (трансформации) и цервикального канала.
Перед получением материала шейку матки обнажают в “зеркалах”, дополнительных манипуляций не проводят (шейку не смазывают, слизь не удаляют; если слизи много – ее аккуратно снимают ватным тампоном, не надавливая на шейку матки.). Щетку (шпатель Эйра) вводят в наружный зев шейки матки, осторожно направляя центральную часть приспособления по оси цервикального канала. Далее ее наконечник поворачивают на 360° (по часовой стрелке), достигая тем самым получения достаточного числа клеток из эктоцервикса и из зоны трансформации. Введение инструмента выполняют очень бережно, стараясь не повредить шейку матки. Затем щетку (шпатель) выводят из канала.
Приготовление препаратов
Перенос образца на предметное стекло (традиционный мазок) должен происходить быстро, без подсушивания и потери прилипших к инструменту слизи и клеток. Обязательно перенести на стекло материал с обеих сторон шпателя или щетки.
Если предполагается приготовление тонкослойного препарата с помощью метода жидкостной цитологии, головку щетки отсоединяют от ручки и помещают в контейнер со стабилизирующим раствором.
Фиксация мазков выполняется в зависимости от предполагаемого метода окрашивания.
Окрашивание по Папаниколау и гематоксилин-эозином наиболее информативны в оценке изменений эпителия шейки матки; любая модификация метода Романовского несколько уступает этим методам, однако при наличии опыта позволяет правильно оценить и характер патологических процессов в эпителии и микрофлору.
Клеточный состав мазков представлен слущенными клетками, находящимися на поверхности эпителиального пласта. При адекватном получении материала с поверхности слизистой оболочки шейки матки и из цервикального канала в мазок попадают клетки влагалищной порции шейки матки (многослойный плоский неороговевающий эпителий), зоны стыка или трансформации (цилиндрический и, при наличии плоскоклеточной метаплазии, метаплазированный эпителий) и клетки цервикального канала (цилиндрический эпителий). Условно клетки многослойного плоского неороговевающего эпителия принято делить на четыре типа: поверхностные, промежуточные, парабазальные, базальные. Чем лучше выражена способность эпителия к созреванию, тем более зрелые клетки попадают в мазок. При атрофических изменениях на поверхности эпителиального пласта расположены менее зрелые клетки.
Интерпретация результатов цитологического исследования
Наиболее распространенная в настоящее время – классификация Bethesda (The Bethesda System), разработанная в США в 1988 г, в которую вносили несколько изменений. Классификация создана для более эффективной передачи информации из лаборатории врачам клинических специальностей и обеспечения стандартизации лечения диагностированных нарушений, а также последующего наблюдения за больными.
В классификации Bethesda выделяют плоскоклеточные интраэпителиальные поражения низкой и высокой степени (squamous intraepithelial lesions of low grade and high grade – LSIL и HSIL) и инвазивный рак. Плоскоклеточные интраэпителиальные поражения низкой степени включают изменения, связанные с папилломавирусной инфекцией и слабой дисплазией (CIN I), высокой степени – умеренную дисплазию (CIN II), тяжелую дисплазию (CIN III) и внутриэпителиальный рак (cr in situ). В этой классификации имеются также указания на специфические инфекционные агенты, вызывающие заболевания, передавае мые половым путем.
Для обозначения клеточных изменений, которые трудно дифференцировать между реактивными состояниями и дисплазией предложен термин ASCUS – atypical squamous cells of undetermined significance (клетки плоского эпителия с атипией неясного значения). Для клинициста этот термин мало информативен, однако он нацеливает врача на то, что данная пациентка нуждается в обследовании и/или в динамическом наблюдении. В классификацию Bethesda в настоящее время введен также термин NILM – no intraepithelial lesion or malignancy, объединяющий норму, доброкачественные изменения, реактивные изменения.
Так как данные классификации используются в практике врача-цитолога, ниже приведены параллели между классификацией Bethesda и классификацией, распространенной в России (Табл. 22). Цитологическое стандартизованное заключениепо материалу из шейки матки (форма № 446/у), утверждено приказом Минздрава России от 24.04.2003 № 174.
Причины получения неполноценного материала различны, поэтому цитолог перечисляет типы клеток, обнаруженные в мазках и по возможности указывает причину, по которой материал признан неполноценным.
Мазок на цитологию: как правильно расшифровать?
Что значит «мазок на цитологию» в гинекологии? Как прочитать его результаты и почему всем женщинам необходимо ежегодно обследоваться у гинеколога? Найти ответы на эти и другие вопросы нам помогла врач – акушер-гинеколог «Клиники Эксперт» Воронеж Валентина Ивановна Хвостикова.
— Валентина Ивановна, расскажите, в чём суть цитологического исследования в гинекологии?
— Цитологическое исследование – это пап-тест (мазок) на патологию шейки матки, который необходимо сдавать ежегодно. Проводится он для ранней диагностики предраковых и раковых болезней шейки матки.
— Какие бывают виды цитологического исследования? Каковы их особенности?
— Существует два вида цитологического исследования. Традиционный, когда материал, взятый из канала шейки матки и с поверхности шейки матки (эндоцервикса и экзоцервикса), наносится на предметное стекло. И второй – метод жидкостной цитологии. В этом случае материал забирается специальной щёточкой сразу с эндо- и экзоцервикса и переносится в контейнер с жидкостной средой. Преимущество этого метода в том, что все клетки, взятые из канала шейки матки и с поверхности шейки матки, находятся в контейнере и не высыхают. В ходе исследования методом жидкостной онкоцитологии в материал могут попасть слизь, эритроциты, лейкоциты. Цитолог отделяет клетки эндоцервикса и экзоцервикса, чтобы провести качественное исследование. Жидкостная онкоцитология считается более информативным методом диагностики. Но это достаточно дорогостоящее исследование, и в практике широко не используется.
Традиционная онкоцитология – основной способ, которым пользуются акушеры-гинекологи в своей практике для диагностики патологий шейки матки. Очень важны качество забора материала и техника его нанесения на стекло.
— Правильно ли я понимаю, что качество мазка может быть плохим (неинформативным)?
— Да, это возможно. Но такое бывает очень редко. Когда мы получаем результат онкоцитологии, взятой традиционным способом (на два стекла), то в нём обязательно отмечается, что мазок хорошего качества, содержит достаточное число клеток цилиндрического и плоского эпителия.
— Какие патологии могут быть выявлены в ходе исследования мазков на цитологию? Как правильно расшифровать результат исследования?
— Сама цель забора материала для анализа – ранняя диагностика патологий шейки матки. Результаты анализа мазков на цитологию шейки матки могут быть следующими:
А) «Цитограмма без особенностей. Негативный в отношении интраэпителиальных поражений и злокачественности материал». Это хороший результат, у женщины нет патологии шейки матки. Интраэпителиальные поражения – дисплазия шейки матки, которая является предраковым заболеванием.
Б) Следующий вид заключений цитологических исследований – «цитограмма ЦИН 1 (CIN1)», т. е. цитограмма дисплазии лёгкой степени. Это международная классификация.
В) Ещё один результат – цитограмма ЦИН 2 (CIN2), т. е. цервикальная интраэпителиальная неоплазия второй (средней) степени.
Г) Четвёртый возможный результат мазка – ЦИН 3 (CIN3), цервикальная интраэпителиальная неоплазия 3 степени. Это тяжёлая дисплазия шейки матки, расценивается как рак in situ (начальная ступень развития рака шейки матки).
Д) Следующее цитологическое заключение – рак шейки матки.
— Валентина Ивановна, а известны ли причины таких изменений? Почему они возникают?
— На сегодняшний день установлено, что причина дисплазии и рака шейки матки – ВПЧ-инфекция. ВПЧ – это аббревиатура вируса папилломы человека. Синоним ВПЧ-инфекции, который встречается в информационном поле – папилломавирусная инфекция (ПВИ).
Немецкий учёный Харальд цур Хаузен в 1983 году доказал, что рак шейки матки вызывается вирусом папилломы человека, передающимся половым путём. За это открытие в 2008 году он получил Нобелевскую премию.
— Что делают акушеры-гинекологи после того, как получат результаты мазка на цитологию?
— При выявленных дисплазиях (любой степени) выполняется кольпоскопия и биопсия шейки матки. Женщина обследуется на ВПЧ-инфицирование и проводится лечение ВПЧ-инфекции.
При получении результата цитологического исследования ЦИН 2 нужно провести выскабливание цервикального канала, а также биопсию шейки матки, чтобы исключить более тяжёлую патологию.
По результатам анализа ЦИН 3 мы направляем пациентку в онкодиспансер, где она в дальнейшем наблюдается.
По цитологическому заключению «рак шейки матки» женщина направляется в онкодиспансер, где ей проводят расширенную экстирпацию матки с придатками (операция Вертгейма). Впоследствии она наблюдается в онкодиспансере и проходит курс терапии.
Важно помнить, что каждая женщина должна обследоваться на папилломавирусную инфекцию. ВПЧ-инфицирование обязательно нужно лечить, чтобы предупредить развитие рака шейки матки. В ранней диагностике заболевания нам помогает обследование на цитологию и ВПЧ-инфекцию.
Записаться на приём к врачу – акушеру-гинекологу можно здесь
ВНИМАНИЕ: услуга доступна не во всех городах
Беседовала Марина Воловик
Редакция рекомендует:
Для справки:
Хвостикова Валентина Ивановна
В 1991 г. с отличием окончила Воронежский государственный медицинский институт, в 1993 г. – ординатуру по акушерству и гинекологии. Работала в областном роддоме.
Дополнительная специализация по УЗИ-диагностике.
В настоящее время – врач – акушер-гинеколог в «Клинике Эксперт» Воронеж. Принимает по адресу: ул. Пушкинская, д. 11.
Гинекологический мазок «на флору»: на что смотреть, и как понять
Большинству женщин мазок «на флору» знаком, как самый «простой» гинекологический анализ. Однако исследование куда «полезнее», чем может казаться. И всего несколько (а то и одно) отклонений способны подсветить значимые проблемы, еще до появления каких-либо симптомов. Так как же понять полученные результаты? Рассказываем по пунктам.
1. Эпителий
Как известно, любой живой объект в природе имеет ограниченный срок жизни, по истечении которого он погибает «от старости».
Эпителий в гинекологическом мазке – это и есть слущенные «старые» клетки слизистой оболочки влагалища, цервикального или уретры (в зависимости от оцениваемого локуса). Которые могут присутствовать в материале в умеренных количествах.
Превышение нормативных пределов («много» или «обильно») может указывать на:
Уменьшение или отсутствие эпителия в мазке – на атрофические изменения, недостаток эстрадиола или избыток андрогенов.
Кроме того, ввиду зависимости эпителия от уровня половых гормонов, его количество в материале может сильно меняться в зависимости от дня цикла, начиная с единичного «в поле зрения» в самом начале – до умеренного и даже большого количества ближе к овуляции и во время нее.
А появление в мазке так называемых «ключевых клеток» (эпителий, «облепленный» мелкими кокковыми бактериями) – является маркером бактериального вагиноза.
2. Лейкоциты
«Норма» лейкоцитов в мазке также сильно зависит от стадии цикла и уровня половых гормонов, а также исследуемого локуса.
Так, за «максимум» для:
Повышение показателя – очевидно, свидетельствует о воспалении, а полное отсутствие может иметь место в норме в самом начале цикла.
Слизь
Результат «отсутствует», «мало» или «умеренно» для этого показателя является нормой, что тоже связано с индивидуальными особенностями гормонального фона и циклом.
А вот «много» слизи в мазке – может свидетельствовать о том, что мазок взят в середине цикла, дисбиотических изменениях или избытке эстрогенов. Поэтому требует внимания специалиста или, как минимум, контроля в динамике.
Флора
Преобладающей флорой женских половых путей в норме у женщин репродуктивного возраста, как известно, являются лактобактерии (или палочки Дедерлейна). Количество которых может быть от умеренного до обильного, в том зависимости, в том числе, от фазы менструального цикла.
Патологические элементы
Присутствия мицелия грибов, трихомонад, диплококков (в том числе и возбудитель гонореи), лептотрикса, мобилункуса и прочих патогенных микроорганизмов в нормальном мазке не допускается, даже в минимальном количестве. А их выявление – серьезный повод незамедлительно обратиться за лечением.
Лейкоцитарная инфильтрация в гистологии что значит
Плацента – важный орган, основное предназначение которого – снабжение кислородом и питательными веществами развивающийся плод во время беременности. При физиологическом течении беременности плацента также обеспечивает иммунологическую толерантность организма матери по отношению к плоду, предотвращая развитие аутоиммунных реакций, являясь своеобразной «подушкой безопасности», а также выполняет эндокринную функцию, синтезируя те гормоны, которые эндокринная система плода не способна синтезировать [1, 2]. Для иммунной системы матери во время беременности баланс между реактивностью и иммуносупрессией склоняется в сторону реактивности. Однако не менее важна барьерная роль плаценты в защите плода от различных микроорганизмов. Локальные иммунные реакции могут потенциально активировать материнский иммунный ответ, что также способствует проникновению патогенных микроорганизмов в амниотическую жидкость, ткань плаценты, проникновение их в ткани, ииммунокомпетентные органы плода. Иммунная система плода ещё незрелая, не готова адекватно распознать болезнетворные бактерии и их эллиминировать. В качестве антигенов могут выступать как микроорганизмы, так и аллоантигены плода, антигены плаценты, аутоантигены матери, которые становятся мишенью для материнского организма. Независимо от их этиологии, в результате сбоя иммунной системы эти факторы могут привести к неблагоприятным результатам, таким как внутриутробная гибель плода, преждевременная роды, задержка роста плода, нарушение развития и дифференцировки внутренних органов.
Одно из первых мест в структуре акушерской патологии занимают инфекционные и воспалительные заболевания беременной, часто скрыто протекающие, достигающие 15–30 % всех преждевременных родов (ПР). Хориоамнионит (ХА) встречается примерно у 15 % беременных [3]. Распространенность ХО составляет в 3–5 % плацент доношенного срока геcтации из которых в 94 % проявляется на 21–24 неделе беременности [4]. В соответствии с современной международной морфологической классификацией повреждений плаценты, разработанной Амстердамской рабочей группой (Amsterdam Placenta Working Group) (2014) [5], воспалительные изменения плаценты делятся на изменения, обусловленные инфекционными агентами и связанные с асептическим воспалением, опосредованные иммунными процессами. В свою очередь воспаление, вызванное инфекционными факторами, бывает с преобладанием воспалительного ответа со стороны матери (преимущественно острым (например, воспаление амниотических оболочек – острый хориамнионит, или со стороны плода (васкулиты сосудов пуповины – фунизит), поражения ворсин плаценты и межворсинчатого пространства – виллиты и интервиллиты), а также децидуальной пластинки, граничащей с полостью матки – децидуит. Воспаление, обусловленное иммунопатологическими процессами, чаще бывает хроническим и представлено хроническим виллитом и хроническим ХА, хроническим децидуитом с инфильтрацией лимфоцитами и плазмоцитами, а также к хроническому воспалению относятся Т-клеточный эозинофильный фетальный васкулит, хронический гистиоцитарный интервиллузит.
Взаимосвязь инфекции влагалища и цервикального канала с ХА, разрывами плодных оболочек и преждевременными родами показано рядом авторов [6]. Однако соответствие гистологических критериев, клинических признаков воспаления и выявление возбудителя (выявленного посредством ПЦР) происходит менее чем в половине случаев [7].
Как и все органы, плацента и плацентарная площадка содержат популяции резидентных воспалительных клеток, которые, как считается, играют решающую роль в развитии и функционировании плаценты. К наиболее важным относятся популяции больших зернистых (гранулярных) лимфоцитов в децидуализированном эндометрии и клетки Гофбауэра стромы ворсин. Первые состоят преимущественно из натуральных киллеров и играют роль в трансформации и ремоделировании спиральных артерий [8], имеют тенденцию к образованию кластеров около желёз эндометрия, и материнских сосудов, но это не сопровождается повреждением тканей. Клетки Гофбауэра представляют собой тканевые макрофаги и, как полагают, принимают участие в васкуляризации ворсин плаценты и защите плода от патогенов и других потенциально опасных медиаторов, которые могут нарушить гемоплацентарный барьер [9], а также играют роль в ангиогенезе, который проявляется на этапе незрелых промежуточных ворсин, когда присутствуют клетки стромы, формирующие пространство будущего кровеносного сосуда с образованием так называемых стромальных каналов, в просвете которых циркулируют макрофаги [10], что особенно важно на ранних сроках гестации. Клетки Гофбауэра обычно по внешнему виду выглядят одинаковыми и, как правило, равномерно распределены в строме ворсин и больше представлены в плаценте на ранних сроках. Выявление в ткани плаценты и матки нейтрофилов, эозинофилов, В- и Т-лимфоцитов, а особенно плазмоцитов составляет основу для патологического воспаления ткани плаценты. Острый воспалительный ответ с преобладанием нейтрофилов наблюдается преимущественно в амниотических оболочках, при ХА, и выявляется примерно в 20 % всех плацент [11]. Хронический хориоамнионит (ХХА) воспаление с преобладанием лимфоцитов встречается в 5–15 % плацент нередко связано инфекцией, но может быть опосредовано аутоиммунными заболеваниями или аллоиммунными реакциями против последствий предыдущих инфекций или инфекций, вызванных еще нераспознанными патогенами, хотя этот вопрос требует дальнейшего изучения.
Хориамниониты являются отражением большого количества факторов риска, при котором гистологические критерии не всегда полно отражают клиническую картину. ХА часто сочетаются с воспалением других частей плацентарного диска (децидуальной оболочки (децидуит), ворсин плаценты (виллит), пупочного канатика (фунизит).
Гистологически острый хориоамнионит (ОХА) определяется как материнская нейтрофильная реакция на бактериальную инфекцию с или без сопутствующего ответа со стороны плода. ХА традиционно имеет место две основных классификации: гистологическую базирующуюся на воспалительной инфильтрации плодных оболочек (нейтрофилами, макрофагами и Т-лимфоцитами). Вторая основана на клинической манифестации локального и системного воспаления:
1) температура более 37,5 °С;
2) наличие болезненности при пальпации матки;
3) боли внизу живота;
4) неприятный запах при влагалищном исследовании;
5) тахикардия у беременной (более 100 ударов в минуту);
6) тахикардия у плода (более 160 ударов в минуту);
7) повышение лейкоцитов крови матери более 15 000 тыс/мм3) [7, 12].
Кроме того, повышение температуры тела может быть ассоциировано также с эпидуральной анальгезией, что затрудняет дифференциальную диагностику [7].
Наибольшим фактором риска в развитии острого ОХА являются микроорганизмы, присутствующие в цервико-влагалищном тракте, нарушение нормальной микрофлоры влагалища, истмико-цервикальная недостаточность, преждевременное раскрытие шейки матки и разрыв плодных оболочек, а также длительный безводный период [7]. Менее распространенными путями заражения, которые нередко не учитываются, но которые не являются менее важными, являются гематогенный путь распространения, например инфекция периодонта, а также патогенная микрофлора органов малого таза (например, инфекция мочевого пузыря, фаллопиевых труб, прямой кишки) может привести к ОХА, после проникновения микроорганизмов в ткань плаценты.
При гистологически подтвержденном ОХА анаэробные бактерии при микробиологическом исследовании выделяются примерно в 50 % случаев. В меньшем проценте наблюдений ОХА ассоциированы с более высокопатогенными организмами, представляющими угрозу жизни и здоровья плода (например, стрептококки, грамотрицательные бациллы и стафилококки), обладающие повышенной способностью к проникновению в организм плода. При ХО, обусловленных этими микрорганизмами, имеет место повышенный риск к развитию внутриутробной инфекции, а также заболеваниям неинфекционной природы, например образование очагов ишемического повреждения головного мозга, которые бывают вызваны Escherichia coli [13]. Распространенность ХО с подтверждёнными гистологическими признаками снижается в зависимости от гестационного возраста: выявляется до 70 % в плаценте от младенцев, рожденных на сроке до 30 недель гестации и приблизительно в 10 % у доношенных новорожденных [11]. Считается, что 25 % всех преждевременных родов обусловлены ХО [14], из которых ХО, ассоциированные с интактными плодными оболочками (без их разрыва) до 45 %, из них только 14–21 % случаев с гистологически подтверждённым ХО. Случаи с преждевременным разрывом плодных оболочек) (ПРО) [14] составляют 30 % наблюдений, из них только от 26 % до 50 % случаев гистологически подтверждённого ХО. Менее 5 % случаев хориоамнионита протекают наиболее тяжело, имеют угрозу для здоровья матери и плода.
Наряду с этим обнаружены микроорганизмы в ткани плаценты, которые могут не вызывать воспалительную реакцию (асимптоматическое течение ХО, однако нередко приводящие к ПРО и преждевременным родам [15]. В исследовании Hillier (1988) до 65 % наблюдений с гистологически подтверждённым ХО из плацент была выделена Ureaplasma urealyticum. Более того, данный микроорганизм был ассоциирован с другими микробными агентами и определялся более, чем в половине наблюдений [16]. Подтверждением этому служит колонизация U. urealyticum дыхательных путей плода, связанная с увеличением хронических заболеваний легких у недоношенных детей [17].
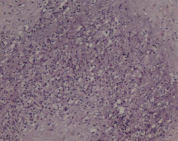
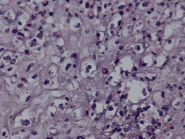
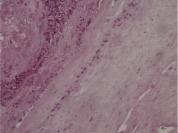
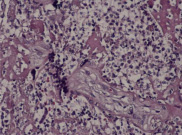
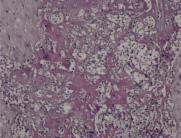
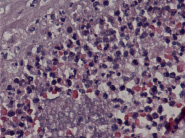
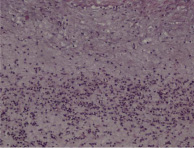
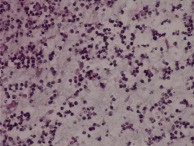
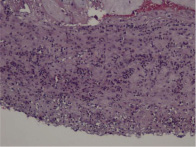
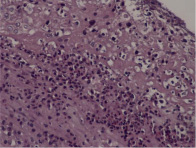
Гистологические критерии острого хориоамнионита. Классификация. Согласно Амстердамской классификации поражений плаценты выделяют материнский и фетальный воспалительный ответ. К материнскому воспалительному ответу относятся поражения плодных оболочек, к фетальному ответу – поражения сосудов пуповины, сосудов стволовых ворсин, васкулиты хориальной пластинки (рис. 1, А–Е).
Рис. 1. Воспалительные изменения хориальной пластинки и плодных оболочек (окраска гем и эоз). А–Б – Инфильтрация хориальной пластинки ПЯЛ, присутствуют лимфоциты, макрофаги и единичные плазмоциты. А – х100, Б – х200. В–Е – Острый хориоамнионит 2–3 стадии, 2 степени В – х100, Г – х200, Д – х100. Е – х400
В материнском воспалительном ответе выделяют стадии, отражающие прогрессию заболевания.
Стадия 1. (острый субхориоамнионит/ранний острый хориоамнионит) = очаговое и диффузное скопление полиморфно-ядерных лейкоцитов (ПЯЛ) в и под хориальной пластинкой и/или в и под амниотической базальной мембраной (отмечаются несколько разбросанных ПЯЛ в менее чем в половине толщины хориальной пластинки и / или в соединительной ткани мембранозной части хориальной пластинки). Воспалительная инфильтрация отмечается лишь под хориальной пластинкой, в последующем нейтрофилы инфильтрируют также как плодный фибриноид под хориальной пластинкой, так и границу децидуальной и хориальной пластинок (острый субхорионит), а затем вовлекаются децидуальные посткапиллярные венулы (острый хорионит). Эта стадия длится обычно менее 12 часов.
Стадия 2. Острый хориоамнионит. Количество нейтрофилов увеличено в хориальной пластинке и / или мембранозной части хориальной пластинке оболочках амниона. Стадия длится в течение 12–24 часов
Стадия 3. Некротический хориоамнионит. Отмечается распад ПЯЛ (кариорексис), утолщение амниотической базальной мембраны, которая становится эозинофильной, присутствует также дистрофия и слущивание амниотического эпителия. После длительной экспозиции инфекции (>48 часов) нейтрофилы подвергаются кариорексису, слущенные амниотические эпителиальные клетки проникают в амниотическую жидкость, что является следствием появления ярко-красной полосы фибриноида на базальной мембране амниона. Это обнаруживается в 50 % случаев и является признаком некротического хориоамнионита.
Спустя несколько дней или недель острые воспалительные инфильтраты стихают и смешанная нейтрофильно-гистиоцитарная инфильтрация сохраняется только в верхних слоях хориона. Этот вариант ХО был назван подострым ХО, который коррелирует с увеличением заболеваемости хроническими заболеваниями легких новорожденных [18]. Важно, что наличие субхориальных микроабсцессов на любой стадии инфекции является проявлением повышенного риска развития тяжелых осложнений, включая сепсис [19].
Степень хориоамнионита (отражает выраженность воспалительных реакций)
Степень 1 (умеренно выраженная): присутствуют единичные или мелкие скопления материнских ПЯЛ, диффузно инфильтрирующих амниотические оболочки, хориальную пластинку и/или расположенный под хориальной пластинкой плодный фибриноид.
Степень 2 (тяжёлая): присутствие трех или более микроабсцессов в хориальной пластинке (не менее 10–20 ПЯЛ), а также между хориальной и децидуальной пластинками в экстраплацентарных оболочках и / или под хориальной пластинкой плацентарного диска. Поражение может иметь вид непрерывной линии из более 10 ПЯЛ, занимающую более половины плодного фибриноида, расположенного под хориальной пластинкой или один оборот в «ролле» плодных оболочек. Хронический (или подострый) ХО диагностируется на основании более выраженной инфильтрации мононуклеарами (обычно макрофагами), в хориальной пластинке (чаще под амнионом). В ряде случаев макрофаги присутствуют как реакция на отложение экзогенных пигментов (например, мекония или гемосидерина).
Фетальный воспалительный ответ
Стадии, отражающие прогрессию заболевания.
Стадия 1 (васкулит хориальных сосудов / флебит пупочной вены): выявление ПЯЛ в стенке сосудов хориальной пластинки или стенке пупочной вены. Проникновение ПЯЛ в вартонов студень допустимо при этой стадии, но пока отсутствуют микроабсцессы и концентрические полосы, окружающие пупочную вену.
Фетальный воспалительный ответ, обусловленной инфильтрацией ПЯЛ на бактериальную инфекцию при беременности, может развиться с 15 недели гестации, но значительно чаще имеет место при доношенных сроках беременности [20]. Фетальный воспалительный ответ начинается с сосудов хориона или пупочной вены, практически всегда сопровождается материнским ответом в виде острого (подострого) хориоамнионита. Острый васкулит фетальных сосудов как изолированное состояние является дискутабельным вопросом.
Стадия 2 (васкулит пупочных сосудов): нейтрофилы присутствуют в стенке одной или обеих пупочных артерий и в пупочной вене. Наличие ПЯЛ в вартоновом студне допустимо при отсутствии микроабсцессов, и концентрических полос, окружающих пупочные сосуды. Фетальные воспалительные реакции в стенке пупочных артерий (пупочный артериит) возникают позже, их развитие коррелирует с повышенным уровнем циркулирующих цитокинов в пупочной крови).
Впоследствии ПЯЛ могут мигрировать в вартонов студень пуповины, где они образуют полоску, выявляемую при гистологическом исследовании, окружающие фетальные сосуды (стадия 3).
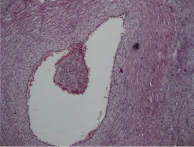
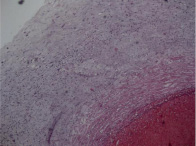
Стадия 3 (некротический фунизит или концентрический периваскулит пупочных сосудов): диагностируют на основании присутствия ПЯЛ, клеточного детрита, эозинофильных преципитатов, и/ или отложений солей кальция, которые визуализируются в виде полоски или ободка, окружающих один или все пупочные сосуды (в большинстве случаев наиболее тяжёлые изменения присутствуют на участках близким к периферии пуповины). Полосу или ободок, который образуют ПЯЛ некоторые авторы называют некротический или субнекротический фунизит и связывают с отложением иммунных комплексов, состоящих из бактериального антигена амниотических оболочек и материнских иммуноглобулинов, диффундирующих из пупочных сосудов [21]. Через несколько недель клетки и эти аркуатные структуры могут исчезнуть, и смениться на эозинофильнуые преципитаты, микрокальцинаты, при этом нередко вовлекаются хориальные сосуды мелкого диаметра (рис. 2, А–Г).
Рис. 2. Воспалительные изменения пуповины и децидуальной пластинки (окраска гем. и эоз.). А–Г – Воспалительные изменения пуповины (воспалительная инфильтрация вартонова студня лимфоцитами, макрофагами и ПЯЛ) А – х40, Б – х100, В – х200, Г – х200. Д–Е – Воспалительные изменения базальной пластинки (очаговая и рассеянная инфильтрация преимущественно ПЯЛ), Д – х100, Е – х200
Степень, отражающая интенсивность воспаления фетального воспалительного ответа
Степень 1 (умеренно выраженная): разбросанные инфильтраты, образованные ПЯЛ, расположены субэндотелиально или стенках хориальных или пупочных сосудов.
Степень 2 (тяжелая): стенки сосудов хориальной пластинки (или сосудов пуповины) с выраженной инфильтрацией ПЯЛ и отёком, наличием повреждения гладкомышечной стенки сосудов на стороне, близкой к амниотической полости. Кроме того, часто отмечаются тромбозы фетальных сосудов (свежие тромбы в сосудах хориальной пластинки или пуповины). Все эти признаки являются отражением картины фетального воспалительного ответа – англ. fetal inflammatory response syndrome (FIRS) – по аналогии с SIRS (англ. Systemic inflammatory response syndrome). Важно отметить, что воспалительный ответ плода не всегда свидетельствует о фетальной инфекции, но является показателем иммунной активации, которая ассоциируется с высокими уровнями цитокинов плода, что приводит к увеличению риска повреждений головного мозга и заболеваний лёгких плода [22–24]. При 2 степени тяжести васкулиты хориальных сосудов ассоциированы с повышенным риском ишемического повреждения головного мозга плода; тромбы в их просвете являются также дополнительном фактором риска [25].
Другие специфические изменения
К другим специфическим изменениям плаценты, ассоциированным с ОХА, относится: периферический фунизит, диагностируемый на основании наличия мелкоточечных абсцессов с участками инфильтрации ПЯЛ на внешней стороне пуповины; острый виллит: присутствие ПЯЛ в строме ворсин и /или под трофобластом; острый интервиллузит / внутриворсинчатый абсцесс – ПЯЛ располагаются в пределах периворсинчатого фибриноида или периворсинчатого пространства, а также в ряде случаев отмечается инфильтрация ПЯЛ децидуальной пластинки (острый децидуит) (рис. 2, Д–Е).
Другие воспалительные изменения, ассоциированные с ОХА, особенно на ранних сроках гестации, включают лимфоплазматический децидуит, и свежие ретроплацентарные гематомы вызывающие диагностическую сложность из-за интенсивной инфильтрации ПЯЛ. В некоторых случаях ОХА могут быть вызваны специфическими микроорганизмами. Так, ОХА с острым интервиллузитом и образованием межворсинчатого абсцесса (так называемые септические инфаркты) чаще всего ассоциируются с Listeria monocytogenes [26, 27]. ОХА с ассоциации с периферическими абсцессами пуповины наиболее часты при инфекции Candida, и часто связаны с преждевременным разрывом плодных оболочек, истмико-цервикальной недостаточностью, а также присутствием внутриматочной спирали или вагинальных колец [28]. ОХА в сочетании с острым виллитом наблюдаются при врождённом бактериальном сепсисе, обычно вызванном стрептококками или грамотрицательными бактериями, в частности E. coli. ОХА в ассоциации с очаговым острым интервиллузитом и периворсинчатым отложением плодного фибриноида могут сочетаться с материнским сепсисом, нередко вызываемого стрептококками и грамотрицательной флорой [29]. Гибель плода редко является следствием непосредственно ОХА, гораздо чаще это происходит при развитии врождённого сепсиса. Преждевременные роды, связанные с ХО, имеют высокий риск рецидива. К возможным причинам этого относят наличие дефектов матки, подострого хронического эндометрита, вызванного стрептококками группы В, бактериального вагиноза, истмико-цервикальной недостаточности.
Изолированный фетальный васкулит может поражать артерии и вены пуповины, хориальной пластинки или крупных стволовых ворсин. Хотя обычно сопровождается острым хориоамнионитом или хроническим виллитом, эти повреждения иногда могут наблюдаться изолированно. Поражения с инфильтрацией ПЯЛ или смешанной воспалительной инфильтрацией (с примесью ПЯЛ) и/или эозинофилами чаще всего обусловлены воздействием мекония, более часто встречаются в стенке пупочной вены [30]. Наблюдения с лимфоцитарной или смешанной лимфоцитарной / эозинофильной инфильтрацией (эозинофильный Т-клеточный хорионический васкулит) имеют место в хориальных или крупных сосудах стволовых ворсин, но данный вопрос является недостаточно изученным [31, 32].
Хронический хориоамнионит (ХХ) встречается в двух различных клинико-патологических вариантах [33]: подострый (хронический) хориоамнионит, является преимущественно затяжной формой инфекционного хориоамнионита и связан чаще с микроорганизмами с низкой патогенностью, такими как микоплазма или вагинальные анааэробы [18]. Один из морфологических вариантов представлен преобладающей воспалительной инфильтрацией гистиоцитами, мононуклеарами с примесью единичных нейтрофилов под амнионом. Этот вариант сочетается с экстремально низкой массой тела детей при рождении и является одной из причин преждевременных родов, часто сочетается с хроническим виллитом. Второй морфологический вариант диагностируется как преобладание лимфоцитарной инфильтрации, по выявленной локализации в хорионе в средней части амниона в виде полос.
Хронический децидуит (ДХ) диагностируется на основании обнаружения инфильтрации мононуклеарами и/или с наличием плазмоцитов [34]. В ряде случаев обнаруживается также большое количество эозинофилов.
Есть предположение, что ДХ может быть результатом эндометритов низкой степени активности и подострых эндометритов, вызванных микоплазмой или другими микроорганизмами с низкой патогенностью, что может быть связано с нарушением микрофлоры влагалища [35]. Это может приводить к преждевременным родам во втором и третьем триместрах. ДХ часто сочетаются с ХО.
Известно, что при отсутствии лечения хронический эндометрит – фактор высокого риска при невынашивании беременности. Кроме того, хронические виллиты сочетаются в 25–30 % случаев с лимфоплазмоцитоидными хроническими децидуитами.
В этих случаях ДХ могут представлять собой неинфекционный воспалительный материнский ответ на аутоантигены или аллоантигены плода [36]. Пациенты с ДХ часто имеют высокий процент аутоиммунных заболеваний различного генеза [37]. Общая перинатальная смертность высока. Антенатальная гибель плода, привычное невынашивание беременности также часто ассоциированы с ДХ. У выживших младенцев нередко отмечается задержка роста и развития. Данное состояние следует также отличать от морфологической картины, при инфицировании Plasmodium falciparum во время беременности.
Децидуальный васкулит/периваскулит диагностируется по наличию выраженности воспалительной инфильтрации вокруг артериол децидуальной пластинки, включая децидуальную пластинку плодных оболочек [3, 38, 39]. Это поражение наиболее часто наблюдается у пациентов с преэклампсией, задержкой развития плода, при невынашивании беременности. Децидуальный васкулит может быть как изолированным, так и сочетаться с острым атерозом и гипертрофией стенок сосудов [39].
Хотя интраамниотическая инфекция обычно считается причиной острого хориоамнионита и фунизита, а также причиной преждевременного разрыва плодных оболочек, однако данные ряда авторов свидетельствуют о том, что «асептическое» внутриамниотическое воспаление (без выявленного микробного агента), может происходить в отсутствии видимых микроорганизмов, и повреждающее действие связано с молекулами повреждения или молекулы «опасности» (DAMP – от англ. Damage-associated molecular pattern или danger-associated molecular patterns), а также интерлейкинами, хемокинами и другими «сигналами опасности». В контексте внутриамниотической инфекции интерлейкины и хемокины (например, интерлейкин-8 и хемотаксические факторы гранулоцитов) создают градиент, который способствует миграции нейтрофилов из системы кровообращения матери или плода в плодные оболочки или пуповину, соответственно. Молекулы повреждения, которые высвобождаются в при повреждении и гибели клеток также в свою очередь могут способствовать высвобождению хемокинов и нейтрофилов [40].
Таким образом, восходящий тип инфекции, обусловленный воспалительным ответом, вызываемый микробными агентами вовлекает 2 типа иммунного ответа: (1) материнский, с инфильтрацией воспалительной инфильтрации (прежде всего ПЯЛ) хориоамниона и хориальной пластинки; и (2) фетальный, определяемый как воспалительная инфильтрация (преимущественно ПЯЛ) вартонова студня, стенок крупных сосудов хориальной пластинки и сосудов пуповины.