неврологические боли в пояснице лечение период обострения что делать
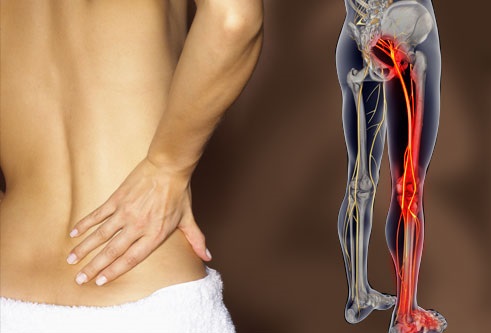
Корешковый синдром поясничного отдела
Причины
Любые морфологические образования или патологические процессы, которые приводят к компрессионному воздействию на нервный корешок, могут стать причиной корешкового синдрома.
Основными причинами поясничной радикулопатии являются:
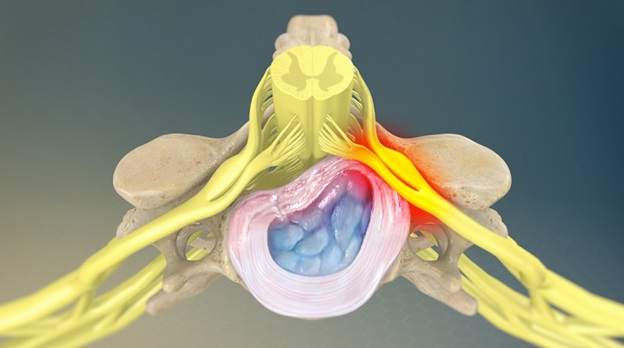
У пациентов моложе 50 лет наиболее частой причиной корешкового синдрома в поясничном отделе позвоночника является грыжа межпозвоночного диска. После 50 лет корешковая боль часто вызвана дегенеративными изменениями позвоночника (стеноз межпозвоночного отверстия).
Факторы риска развития поясничной радикулопатии:
Симптомы
Симптомы, возникающие в результате корешкового синдрома (радикулопатии), локализуются в зоне иннервации конкретного корешка.
Паттерны боли
Начало появления симптомов у пациентов с пояснично-крестцовой радикулопатией (корешковым синдромом) часто бывает внезапным и включает боль в пояснице.
Сидение, кашель или чихание могут усугубить боль, которая распространяется от ягодицы по задней поверхности голени, лодыжки или стопы.
Необходимо быть бдительным при наличии определенных симптомов (красных флажков). Такие красные флажки могут означать более тяжелое состояние, требующее дальнейшего обследования и лечения (например, опухоль, инфекция). Наличие лихорадки, потери веса или ознобов требует тщательного обследования.
Возраст пациента также является фактором при поиске других возможных причин симптоматики у пациента. Лица моложе 20 лет и старше 50 лет подвержены повышенному риску возникновения более серьезных причин боли (например, опухоли, инфекции).
Диагностика
Первичный диагноз корешкового синдрома пояснично-крестцового отдела позвоночника выставляется на основании симптоматики истории болезни и данных физического обследования (включая тщательное изучение неврологического статуса). Тщательный анализ моторной, сенсорной и рефлекторной функций позволяет определить уровень поражения нервного корешка.
Если пациент сообщает о типичной односторонней иррадиирущей боли в ноге и есть один или несколько положительных результатов неврологического теста, то тогда диагноз радикулопатии очень вероятен.
Тем не менее, существует ряд состояний, которые могут проявляться схожими симптомами. Дифференциальную диагностику необходимо проводить со следующими состояниями:
Для постановки клинически достоверного диагноза, как правило, требуются инструментальные методы диагностики:
Лечение
Лечение корешкового синдрома пояснично-крестцового отдела позвоночника будет зависеть от тяжести симптоматики и клинических проявлений. Чаще всего, используется консервативное лечение, но в определенных случаях бывает необходимо хирургическое лечение.
Консервативное лечение:
Иглорефлексотерапия. Этот метод широко используется в лечении корешкового синдрома в пояснично-крестцовом отделе позвоночника и помогает как снизить симптоматику в остром периоде, так и входит в комплекс реабилитации.
Хирургическое лечение
Оперативные методы лечения корешкового синдрома в пояснично-крестцовом отделе позвоночника необходимы в тех случаях, когда есть устойчивость к консервативному лечению или имеются симптомы, свидетельствующие о выраженной компрессии корешка такие как:
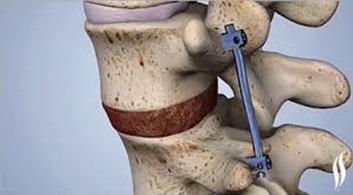
Некоторые хирургические процедуры, используемые для лечения поясничной радикулопатии:
Прогноз
В большинстве случаев удается лечить корешковый синдром в пояснично-крестцовом отделе позвоночника консервативно (без хирургического вмешательства) и восстановить трудоспособность. Продолжительность лечения может варьироваться от 4 до 12 недель в зависимости от тяжести симптомов. Пациентам обязательно необходимо продолжать в домашних условиях выполнять упражнения для улучшения осанки, а также на растяжение, усиление и стабилизацию. Эти упражнения необходимы для лечения состояния, вызвавшего корешковый синдром.
Невралгия спины причины, симптомы, методы лечения и профилактики
Невралгия спины – поражение периферического нерва, сопровождающееся приступами боли, при этом сохраняются двигательная активность и чувствительность. Чаще всего оно встречается у пожилых людей и медленно поддается лечению. Невралгия спины развивается при дегенеративно-дистрофических и воспалительных заболеваниях позвоночника. Также развитию патологии способствуют грипп, ОРВИ, травмы, переохлаждения и прочие факторы. Своевременное обращение к врачу поможет избежать серьезных осложнений.
Причины невралгии спины
Патология возникает на фоне следующих причин:
Даже резкое движение тела может вызвать приступ невралгии. При неловком повороте человек чувствует острую боль. В некоторых случаях обезболивающие препараты не дают никакого результата.
Невралгия грудного отдела позвоночника возникает при деформации грудной клетки, после инфекционных заболеваний, аллергии или травм. Нередко болезнь развивается при злоупотреблении алкоголем, дефиците витамина B в организме, нарушении пищеварения, сахарном диабете и сердечно-сосудистых патологиях.
Невралгия затылочного и шейного отдела позвоночника развивается при дефектах осанки, перенесенных инфекциях, болезнях сосудов, остеохондрозе и сахарном диабете. Человек жалуется на приступ боли длительностью до 5 минут.
К причинам невралгии у детей врачи относят:
БОЛИ В СПИНЕ: болезненный мышечный спазм и его лечение миорелаксантами
Боли в спине — одна из наиболее распространенных жалоб, которые пациенты предъявляют в общемедицинской практике. Часто они вызываются остеохондрозом позвоночника — дегенеративным поражением хряща межпозвонкового диска и реактивными изменениями со стороны
Боли в спине — одна из наиболее распространенных жалоб, которые пациенты предъявляют в общемедицинской практике. Часто они вызываются остеохондрозом позвоночника — дегенеративным поражением хряща межпозвонкового диска и реактивными изменениями со стороны тел смежных позвонков. Поражение межпозвонкового диска развивается вследствие его повторных травм (подъем тяжести, избыточная статическая и динамическая нагрузка, падения и др.) и возрастных дегенеративных изменений. Студенистое ядро, центральная часть диска, высыхает и частично утрачивает амортизирующую функцию. Фиброзное кольцо, расположенное по периферии диска, истончается, в нем образуются трещины, к которым смещается студенистое ядро, образуя выпячивание (пролапс), а при разрыве фиброзного кольца — грыжу. В настоящее время созданы препараты, оказывающие структурно-модифицирующее действие на хрящевую ткань (старое название — хондропротекторы). Типичным представителем группы является препарат хондро, назначаемый курсом по 4 месяца (эффект сохраняется 2 месяца после отмены). В пораженном позвоночном сегменте возникает относительная нестабильность позвоночника, развиваются остеофиты тел позвонков (спондилез), повреждаются связки и межпозвонковые суставы (спондилоартроз). Грыжи межпозвонковых дисков наиболее часто наблюдаются в нижних поясничных дисках, реже — в нижних шейных и верхних поясничных, крайне редко — в грудных. Грыжи диска в тело позвонка (грыжи Шморля) клинически не значимы, грыжи диска в заднем и заднебоковом направлении могут вызвать сдавление спинно-мозгового корешка (радикулопатию), спинного мозга (миелопатию на шейном уровне) или их сосудов.
Кроме компрессионных синдромов возможны рефлекторные (мышечно-тонические), которые обусловлены импульсацией из рецепторов в ответ на изменения в дисках, связках и суставах позвоночника — болезненный мышечный спазм. Рефлекторное напряжение мышц вначале имеет защитный характер, поскольку приводит к иммобилизации пораженного сегмента, однако в дальнейшем этот фактор становиться причиной возникновения боли. В отличие от компрессионных синдромов остеохондроза позвоночника, которые встречаются относительно редко, болевые мышечные спазмы возникают в течение жизни практически у каждого второго человека.
Классический пример болезненного мышечного спазма представляет люмбаго (поясничный прострел), который характеризуется резкой, простреливающей болью в пояснице, развивающейся, как правило, при физической нагрузке (подъем тяжести и др.) или неловком движении. Больной нередко застывает в неудобном положении, попытка движения приводит к усилению боли. При обследовании выявляют напряжение мышц спины, обычно сколиоз, уплощение поясничного лордоза или кифоз.
Люмбалгия — боль в спине — и люмбоишиалгия — боль в спине и по задней поверхности ноги — развиваются чаще после физической нагрузки, неловкого движения или переохлаждения, реже — без каких-либо причин. Боли носят ноющий характер, усиливаются при движениях в позвоночнике, определенных позах, ходьбе. Для люмбоишиалгии характерна боль в ягодице, в задненаружных отделах ноги, не достигающая пальцев. При обследовании выявляют болезненность, напряжение мышц спины и задней группы мышц ноги, ограничение подвижности позвоночника, часто сколиоз, симптомы натяжения (Ласега, Вассермана и др.).
На шейном уровне могут возникать рефлекторные мышечно-тонические синдромы: цервикалгия и цервикобрахиалгия, которые чаще развиваются после физической нагрузки или неловкого движения шеи. Цервикалгия — боль в шейной области, которая нередко распространяется на затылок (цервикокраниалгия). Цервикобрахиалгия — боль в шейной области, распространяющаяся на руку. Характерно усиление болей при движениях в шее или, наоборот, при длительном статическом положении (в кино, после сна на плотной высокой подушке и др.). При обследовании выявляют напряжение шейных мышц, часто наблюдается ограничение движений в шейном отделе, болезненность при пальпации остистых отростков и межпозвонковых суставов на стороне боли.
При компрессии нервного корешка (радикулопатии) кроме болезненного мышечного спазма и ограничений подвижности в позвоночнике и конечностях выявляются чувствительные, рефлекторные и (или) двигательные нарушения в зоне пораженного корешка. На поясничном уровне чаще поражаются пятый поясничный (L5) и первый крестцовый (S1) корешки, реже — четвертый поясничный корешок и очень редко — верхние поясничные корешки. Радикулопатии нижних шейных корешков встречаются значительно реже.
Важно помнить, что боли в спине могут быть единственным симптомом при опухоли спинного мозга, сирингомиелии и других заболеваниях спинного мозга. Боли возникают при деструкции позвонков и поражении нервных корешков вследствие инфекционных процессов (туберкулезный спондилит, спинальный эпидуральный абсцесс), новообразованиях (первичные и метастатические опухоли позвоночника, миеломная болезнь), дисметаболических нарушениях (остеопороз, гиперпаратиреоз, болезнь Педжета). Боль в спине может быть следствием перелома позвоночника, его врожденных или приобретенных деформаций (сколиоза и др.), стеноза позвоночного канала, спондилолистеза, анкилозирующего спондилоартрита.
Она возможна при различных соматических заболеваниях (сердца, желудка, поджелудочной железы, почек, органов малого таза и др.) по механизму отраженных болей.
Обследование пациента с болью в спине требует тщательности. Нельзя любые боли в спине списывать на «остеохондроз» — состояние, которое при рентгенологическом исследовании выявляется у большинства людей среднего и пожилого возраста. Для неврологических проявлений остеохондроза позвоночника и миофасциальных болей характерны болезненный мышечный спазм и ограничение подвижности позвоночника.
Диагноз рефлекторных и компрессионных осложнений остеохондроза основывается на клинических данных и требует исключения других возможных причин болей в спине. Рентгенографию позвоночника используют, в основном, для исключения врожденных аномалий и деформаций, воспалительных заболеваний (спондилитов), первичных и метастатических опухолей. Рентгеновская КТ или МРТ позволяет выявить грыжу диска, определить ее размеры и локализацию, а также обнаружить стеноз позвоночного канала, опухоль спинного мозга.
Диагноз миофасциальных болей основывается на клинических данных (выявление болезненного мышечного напряжения одной или нескольких мышц) и требует исключения других возможных причин боли; дифференциальный диагноз с рефлекторными синдромами (мышечно-тоническими синдромами) вследствие остеохондроза позвоночника часто вызывает сложности; возможно сочетание этих заболеваний.
Лечение рефлекторных синдромов и радикулопатий вследствие остеохондроза основывается в остром периоде на обеспечении покоя — больному рекомендуется избегать резких наклонов и болезненных поз. Предписаны постельный режим в течение нескольких дней до стихания резких болей, жесткая постель (щит под матрац), прием миорелаксантов центрального действия, при необходимости — также дополнительно анальгетиков, нестероидных противовоспалительных средств. Для облегчения передвижения в этот период следует надеть шейный или поясничный корсет (фиксирующий пояс). Можно использовать физиотерапевтические анальгезирующие процедуры, втирание обезболивающих мазей, компрессы с 30–50-процентным раствором димексида и новокаином, новокаиновые и гидрокортизоновые блокады. При ослаблении болей рекомендуют постепенное увеличение двигательной активности и упражнения на укрепление мышц.
При хроническом течении рефлекторных синдромов и радикулопатий могут быть эффективны мануальная терапия, рефлексотерапия, физиотерапевтическое лечение, санаторно-курортное лечение. Хирургическое лечение (удаление грыжи диска) необходимо в тех редких случаях, когда возникает сдавление спинного мозга или корешков конского хвоста. Хирургическое лечение также показано при дискогенной радикулопатии, сопровождающейся выраженным парезом, и при длительном (более трех-четырех месяцев) отсутствии эффекта от консервативного лечения и наличии большой грыжи диска. Для профилактики обострений остеохондроза рекомендуют избегать провоцирующих факторов (подъем больших грузов, ношение тяжелой сумки в одной руке, переохлаждение и др.), регулярно заниматься лечебной гимнастикой.
При миофасциальных болях необходимо, чтобы мышца находилась в покое в течение нескольких дней. В качестве лечения можно назначать упражнения на растяжение мышц (постизометрическая релаксация), физиотерапию, рефлексотерапию или местное введение анестетиков в триггерные зоны, компрессы с димексидом и анестетиками.
Как уже было отмечено, и при острых болях, и при хронических болевых синдромах большое значение имеет лечение болезненного мышечного спазма. Тоническое напряжение мышц может не только само по себе быть причиной боли, но и способно вызвать деформацию и ограничивать подвижность позвоночника, а также обуславливать компрессию проходящих вблизи нервных стволов и сосудов. Для его лечения помимо нестероидных противовоспалительных средств, анальгетиков, (например, нимулид в форме трансдермального геля для местной терапии или в форме лингвальных таблеток при остром болевом синдроме), физиотерапии и лечебной гимнастики в качестве препаратов первого ряда применяют миорелаксанты — препараты, способные разорвать «порочный круг» болевого синдрома [2].
Для лечения болезненного мышечного спазма миорелаксанты используются внутрь или парентерально. Снижая рефлекторное мышечное напряжение, миорелаксанты уменьшают боль, улучшают двигательные функции и облегчают проведение лечебной физкультуры. Лечение миорелаксантами начинают с обычной терапевтической дозы и продолжают до тех пор, пока сохраняется болевой синдром; как правило, курс лечения составляет несколько недель. В ходе целого ряда исследований удалось доказать, что при болезненном мышечном спазме добавление к стандартной терапии (нестероидные противовоспалительные средства, анальгетики, физиотерапия, лечебная гимнастика) миорелаксантов приводит к более быстрому регрессу боли, мышечного напряжения и улучшению подвижности позвоночника.
В качестве миорелаксантов применяются мидокалм, баклофен и сирдалуд. Миорелаксанты обычно не комбинируют друг с другом. Для снятия болезненных мышечных спазмов можно также использовать диазепам (седуксен, реланиум) в индивидульно подобранной дозе.
Сирдалуд (тизанидин) — агонист α-2 адренергических рецепторов. Препарат снижает мышечный тонус вследствие подавления полисинаптических рефлексов на уровне спинного мозга, что может быть вызвано угнетением высвобождения возбуждающих аминокислот и активацией глицина, снижающего возбудимость интернейронов спинного мозга; сирдалуд обладает также умеренным центральным анальгезирующим действием. При приеме внутрь максимальная концентрация сирдалуда в крови достигается через час, прием пищи не влияет на его фармакокинетику. Начальная доза препарата составляет 6 мг в сутки в три приема, средняя терапевтическая доза — 12—24 мг в сутки, максимальная доза — 36 мг в сутки. В качестве побочных эффектов отмечаются сонливость, головокружение, незначительное снижение артериального давления; требуется осторожность при приеме препарата больными пожилого возраста.
Мидокалм (толперизон) в течение длительного времени широко используется при лечении рефлекторных и компрессионных осложнений дегенеративно-дистрофических изменений позвоночника (остеохондроз, спондилез, спондилоартроз) и миофасциальных болей [3]. Мидокалм оказывает преимущественно центральное миорелаксирующее действие. Снижение мышечного тонуса при приеме препарата связывается с угнетающим влиянием на каудальную часть ретикулярной фармации и подавлением спинно-мозговой рефлекторной активности. Препарат обладает умеренным центральным анальгезирующим действием и легким сосудорасширяющим влиянием. Прием мидокалма начинают с 150 мг в сутки три раза в день, постепенно увеличивая дозу до получения эффекта, у взрослых обычно до 300—450 мг в сутки. Для быстрого эффекта препарат вводится внутримышечно по 1 мл (100 мг) два раза в сутки или внутривенно по 1 мл один раз в сутки.
Эффективность и безопасность применения мидокалма при болезненном мышечном спазме доказана в ходе двойного слепого плацебо-контролируемого исследования [4]. В восьми исследовательских центрах 110 больных в возрасте от 20 до 75 лет методом рандомизации получали мидокалм в дозе 300 мг в сутки или плацебо в сочетании с физиотерапией и реабилитацией в течение 21 дня. В качестве объективного критерия эффективности лечения рассматривают болевой порог давления, измеряемый с помощью специального прибора (Pressure Tolerance Meter) в 16 симметричных точек туловища и конечностей. Кроме того, пациенты субъективно оценивали свое состояние по интенсивности боли, ощущению напряжения мышц и подвижности позвоночника; врач также оценивал напряжение мышц и подвижность позвоночника. Перед началом лечения и после его окончания проводилось развернутое клиническое и лабораторное обследование, включая ЭКГ, измерение артериального давления, биохимический анализ крови по 16 показателям.
Согласно результатам исследований, применение мидокалма достоверно снижает болезненный мышечный спазм, измеряемый объективно инструментальным методом. Различие между группами лечения и плацебо, которое отмечалось уже на четвертый день, постепенно увеличивалось и становилось статистически достоверным на 10-й и 21-й дни лечения, которые были выбраны в качестве конечных точек для доказательного сравнения. Анализ субъективной оценке результатов лечения, данной врачами и пациентами после его окончания (через 21 день), показал, что в группе больных, получавших мидокалм, достоверно чаще результаты лечения оценивались как очень хорошие, тогда как в группе плацебо эффект существенно чаще отсутствовал. Согласно субъективной оценке результатов лечения, данной больными после его окончания (через 21 день), каких-либо значимых различий, касающихся переносимости мидокалма и плацебо, выявлено не было. У подавляющего большинства больных отмечалась хорошая переносимость мидокалма. Результаты ЭКГ, биохимические и гематологические показатели в группе пациентов, принимавших как мидокалм, так и плацебо, также не различались.
Важно отметить, что более половины (62%) пациентов, включенных в исследование, получали другие виды терапии до начала исследования, и у большинства из них (68%) при этом не отмечалось улучшения. Это свидетельствует об эффективности мидокалма в лечении болезненного мышечного спазма, резистентного к другим видам терапии.
Введение мидокалма парентерально позволяет быстро снять боль и уменьшить мышечное напряжение. При вертеброгенном мышечно-тоническом синдроме внутримышечное введение 100 мг мидокалма ослабляет боль уже через 1,5 ч, а лечение мидокалмом в течение недели по 200 мг/сут в/м, а затем на протяжении двух недель по 450 мг/сут перорально имеет достоверное преимущество над стандартной терапией; при этом терапия мидокалмом не только позволяет уменьшить боль, но и снимает тревожность, повышает умственную работоспособность [1].
При болезненном мышечном спазме достоинствами мидокалма помимо эффективного миорелаксирующего и обезболивающиего эффекта являются отсутствие побочных эффектов и хорошее взаимодействие с нестероидными противовоспалительными средствами, что во многих случаях позволяет уменьшить дозу последних и вследствие этого ослабить или даже полностью устранить их побочные эффекты, не снижая эффективности лечения.
Важным преимуществом мидокалма перед другими миорелаксантами является отсутствие седативного эффекта и мышечной слабости при его приеме. Это преимущество доказано в ходе двойного слепого плацебо-контролируемого исследования [5]. В исследовании вошли 72 здоровых добровольца в возрасте от 19 до 27 лет (средний возраст — 21,7 лет). Исследование проводилось в течение восьми дней, все это время добровольцы методом рандомизации получали 150 или 450 мг мидокалма в сутки в три приема либо плацебо — также в три приема. Нейропсихологические исследования осуществляются утром в первый и последний (восьмой) дни исследования до и после приема мидокалма через 1,5, 4 и 6 ч либо плацебо. Результаты исследования не показали каких-либо существенных различий в скорости сенсомоторных реакций и быстроте выполнения различных психологических тестов через 1,5, 4 и 6 ч после приема мидокалма в дозе 50 или 150 мг либо плацебо. Аналогичные исследования, проведенные на восьмой день с начала приема мидокалма, также не показали существенных различий в сравнении с группой плацебо. Это свидетельствует о хорошей переносимости мидокалма и возможности назначения его в тех случаях, когда по роду деятельности пациенту требуется сохранить быстроту реакций и способность концентрировать внимание, в том числе при вождении автомобиля.
Таким образом, болезненный мышечный спазм представляет собой одну из наиболее распространенных причин болей в спине (вследствие рефлекторных синдромов остеохондроза или миофасциальных болей). В таких случаях рекомендуется применение миорелаксантов в комбинации с различными лекарственными средствами, физиотерапией и лечебной гимнастикой. В последние годы доказана эффективность и безопасность миорелаксанта мидокалма, который не вызывает седативного эффекта и выпускается в форме для парентерального введения с целью быстрого купирования болевого синдрома.
Литература.
В. А. Парфенов, доктор медицинских наук, профессор ММА им. И. М. Сеченова
Т. Т. Батышева, кандидат медицинских наук Поликлиника восстановительного лечения №7 Москвы
Вертебральная поясничная боль: полифакторное происхождение, симптоматология, принципы лечения
Боль в спине, знакомая почти каждому человеку, чаще всего связана с поражением пояснично-крестцового отдела позвоночника. Развитию хронической вертебральной, в том числе поясничной боли, способствуют большие физические нагрузки и наоборот — отсутств
Боль в спине, знакомая почти каждому человеку, чаще всего связана с поражением пояснично-крестцового отдела позвоночника. Развитию хронической вертебральной, в том числе поясничной боли, способствуют большие физические нагрузки и наоборот — отсутствие адекватных нагрузок, неблагоприятные метеорологические факторы (особенно перманентные, связанные с неудовлетворительными условиями труда и быта), врожденная или приобретенная патология опорно-двигательного аппарата и позвоночного столба, а также наличие избыточного веса и остеопороза. По своей распространенности в нашей стране хроническая вертебральная боль относится к числу массовых проблем здоровья населения.
Поясничная вертебральная боль, помимо первичного поражения позвоночника, может иметь «вневертебральное» происхождение — за счет вторичного вовлечения костно-хрящевых и нервных структур позвоночного столба.
Основные факторы и клинические формы поражения позвоночника
К первичным факторам поражения позвоночника — в частности, его пояснично-крестцового отдела — относятся очаговые или распространенные вертебральные изменения, связанные с самостоятельно возникшей патологией позвоночного столба. Среди них основным фактором является дистрофический вертебральный процесс (остеохондроз позвоночника).
Вторичные факторы поражения связаны с наличием экстравертебрального патологического процесса, также приводящего к развитию очаговых или распространенных изменений в позвоночнике. Наибольшее клиническое значение среди них имеют остеопороз и метастатическое поражение позвоночника.
Первый фактор (остеопороз) отличается значительной распространенностью среди женщин среднего, пожилого и старческого возраста. В то же время остеопороз позвоночника чаще всего протекает без развития неврологических расстройств, в связи с чем его клинические проявления редко являются поводом неврологического наблюдения. Второй фактор (метастатическое поражение) во много раз превышает частоту первичных опухолей позвоночника. В ряде случаев вертебральные нарушения метастатического происхождения попадают в сферу наблюдения невролога еще до установления диагноза основного заболевания. Схема — факторы и клинические формы первичного и вторичного поражения позвоночника — представлена на рис. 1.
Клинические проявления патологии пояснично-крестцового отдела позвоночника
В неврологической практике дифференциация форм вертебрального поражения начинается с определения вертебрального синдрома, с учетом особенностей которого проводится установление основного заболевания. Клинические проявления патологии пояснично-крестцового отдела позвоночника представляют собой 3 группы вертебральных синдромов (рис. 2):
Болевые (рефлекторные) синдромы
Болевые (рефлекторные) синдромы пояснично-крестцовой области, не сопровождающиеся очаговой неврологической симптоматикой, могут проявляться:
Корешковые синдромы (радикулопатии)
Корешковые синдромы (радикулопатии), вызванные поражением пояснично-крестцового отдела позвоночника, встречаются реже болевых поясничных синдромов. О наличии радикулопатии свидетельствуют симптомы выпадения чувствительной, рефлекторной и двигательной функций определенного спинномозгового корешка.
Проявления пояснично-крестцовых радикулопатий:
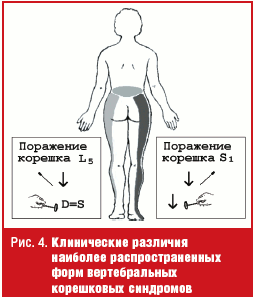
Наиболее распространенные формы пояснично-крестцовых радикулопатий связаны с поражением пятого поясничного (L5) и первого крестцового (S1) спинномозговых корешков. Клинические различия данных радикулопатий касаются зон локализации боли и чувствительных расстройств, а также наличия ахиллова рефлекса, исчезающего при радикулопатии S1 (рис. 4).
Клинические особенности остеохондроза позвоночника
В подавляющем большинстве случаев развитие поясничных болевых и корешковых синдромов вызвано остеохондрозом позвоночника, особенно часто затрагивающим сочленения двух нижних поясничных позвонков и основания крестца (межпозвоночные диски LIV–LV, LV –SI).
Основные клинические проявления остеохондроза позвоночника, в разной степени ограничивающие двигательную активность больного, включают рецидивирующую или хроническую вертебральную боль, болезненную подвижность позвоночника, а также монорадикулярные неврологические расстройства.
Течение клинических проявлений остеохондроза позвоночника чаще всего циклическое — с чередованием периодов обострения и ремиссии (полной или частичной). Обострения, как правило, носят сезонный характер (осень и весна). Наибольшая частота обострений заболевания приходится на пятое десятилетие жизни. В большинстве случаев развитие обострений вертебральной патологии бывает предсказуемым — при нарушении режима, ограничивающего физические нагрузки и исключающего охлаждение.
Самой характерной клинической особенностью остеохондроза позвоночника как заболевания с хроническим, многолетним течением является неизбежность постепенного «затихания» вертебральной боли (обычно на рубеже 5–6-го десятилетий жизни). Данная особенность остеохондроза позвоночника обусловлена переходом текущего дистрофического процесса в заключительную стадию, стабилизирующую положение костных и мягкотканных структур позвоночного столба. В связи с этим регресс вертебральной боли часто сопровождается еще большим ограничением подвижности позвоночника. Сохраняющиеся после 50 лет боль и ограничения повседневной двигательной активности больного чаще всего бывают связаны с предшествующей травмой, иной формой поражения позвоночника или остеоартрозом тазобедренного сустава.
Наиболее неблагоприятной формой проявлений поясничного остеохондроза является развитие дискогенной компрессии структур позвоночного канала, в частности — конского хвоста, угрожающей тяжелыми неврологическими осложнениями и инвалидизацией больного. Компрессия структур позвоночного канала также может быть связана с вторичными формами поражения позвоночника (рис. 1).
Признаки острой компрессии структур позвоночного канала (в том числе конского хвоста):
Клинические особенности вторичного поражения позвоночника
Симптоматическая вертебральная боль, вызванная вторичным поражением позвоночника, в самом начале своего развития может протекать подобно проявлениям остеохондроза позвоночника. Наличие данной боли часто становится поводом для проведения физиотерапии, способной еще больше усугубить проявления основного заболевания.
Установлению симптоматического характера вертебральной боли способствуют:
Атипичные вертебральные проявления (характерны для вторичного поражения позвоночника):
–чаще возникает у больных старше 40, особенно 50 лет;
–постепенно нарастает;
–усиливается при движениях, сохраняется или усиливается в покое;
–дневная, а также ночная, в том числе «пробуждающая»;
–сопровождается локальной вертебральной болью — «болезненностью» или резкой болью в пределах одного или двух смежных позвонков при надавливании и «поколачивании» остистых отростков;
–повышением температуры тела;
–общей слабостью, снижением аппетита, потерей массы тела;
–изменениями лабораторных показателей— ускорением СОЭ, анемией, лейкоцитозом.
Принципы лечения
Анальгетические средства
Основными анальгетическими средствами для устранения вертебральной боли являются нестероидные противовоспалительные препараты (НПВП). НПВП, как и другие обезболивающие препараты, обычно самостоятельно принимаются больными при усилении и возобновлении боли. Однако длительное применение анальгетических средств, повышающее риск развития осложнений лекарственной терапии, предусматривает контролируемое врачом применение НПВП.
На сегодняшний день в арсенале практикующего врача имеется широкий ряд НПВП, относящихся по механизму действия к «неселективным» противовоспалительным препаратам — блокирующим фермент циклооксигеназу (ЦОГ) и «селективным» — блокирующим изофермент ЦОГ-2. Эти препараты существенно различаются между собой соотношением преимуществ и недостатков, соответственно — выраженностью и продолжительностью лечебных эффектов и вызываемыми побочными действиями. Вероятно, более предпочтительными для больных с вертебральной болью (по доступности, эффективности и меньшей вероятности побочных эффектов) являются: среди «неселективных» НПВП — диклофенак, ибупрофен и кетопрофен, а среди «селективных» — мелоксикам.
Способы применения НПВП:
Диклофенак — внутрь 100–150 мг/сут (обычные таблетированные формы 25–50 мг, форма ретард — 100 мг); внутримышечно или подкожно; ректально; местно.
Ибупрофен — внутрь 1200 мг/сут; местно.
Кетопрофен — внутрь 150–300 мг/сут (обычная таблетированная форма 50 мг, форма ретард— 150 мг); внутримышечно; ректально; местно.
Мелоксикам— внутрь 7,5–15 мг/сут (однократно); внутримышечно; ректально.
Общим правилом для НПВП является применение пероральных форм во время или сразу после еды с достаточным количеством воды.
Длительность применения НПВП зависит от выраженности и продолжительности вертебральной боли. При остро возникшей боли в спине бывает достаточно кратковременного (в течение нескольких дней) применения НПВП. При наличии интенсивной, особенно корешковой боли, период применения одного и того же НПВП обычно составляет не менее 3–4 недель.
Наиболее вероятные побочные эффекты НПВП связаны с их воздействием на желудочно-кишечный тракт. Меньшая частота развития желудочной и кишечной диспепсии, а также желудочно-кишечного кровотечения отмечается при использовании мелоксикама.
Витамины группы В
Применение нейротропных витаминов группы В — распространенный в клинической практике метод лечения больных с поражением периферической нервной системы, в том числе неврологическими проявлениями остеохондроза позвоночника. Для проведения так называемой витаминотерапии традиционно использовался способ попеременного введения растворов тиамина (витамина В1), пиридоксина (витамина В6) и цианокобаламина (витамина В12) — по 1–2 мл внутримышечно с ежедневным чередованием каждого препарата — в течение 2–4 недель. Недостатки такой схемы уже давно известны — малые дозы и частые инъекции приводят к низкому комплайенсу.
В настоящее время чаще применяется поликомпонентный препарат «Мильгамма», каждая ампула которого содержит по 100 мг тиамина и пиридоксина и 1000 мкг цианокобаламина, а также лидокаин, обеспечивающий местноанестезирующий эффект при внутримышечном введении препарата. Мильгамма, обладающая антиноцицептивным (вероятно, серотонинергическим) действием, применяется при острой, рецидивирующей и хронической вертебральной боли. Ввиду установленного влияния Мильгаммы на процессы регенерации нервных волокон и миелиновой оболочки, данный препарат особенно широко используется при вертебральных и экстравертебральных формах поражения периферической нервной системы.
Мильгамма композитум — для перорального приема, включает бенфотиамин (жирорастворимая форма витамина В1, сохраняющая свою фармакологическую активность после всасывания в желудочно-кишечном тракте) и пиридоксин. Наличие этих двух компонентов обеспечивает эффективность дальнейшей терапии (в течение 6 недель, после курсового применения препарата «Мильгамма».
Мильгамма — внутримышечно 2 мл, ежедневно, в течение 10 или 15 дней.
Мильгамма композитум — внутрь, по 1 драже 3 раза в день, в течение 6 недель.
Немедикаментозные методы лечения
При обострении вертебральной боли и ее обратном развитии наряду с медикаментозным лечением попеременно и в различной последовательности проводятся физиотерапия (включая массаж), иглотерапия и мануальная терапия. Одновременно с этим должна проводиться постепенная, не усиливающая выраженности боли, двигательная активизация, являющаяся для больного действенным методом «самопомощи», а вне обострения — методом предупреждения хронической вертебральной боли.
Хирургические методы лечения
Хирургические методы лечения вертебральной патологии могут носить плановый или экстренный характер. Плановый порядок проведения хирургического вмешательства определяется относительно стабильной клиникой вертебральной патологии, требующей радикального удаления или доступной для хирургического воздействия.
Целью проведения подобных операций (на поясничном уровне) является:
Большинство хирургических операций на позвоночнике проводится по поводу хронической или часто рецидивирующей поясничной боли. Основным аргументом в пользу выбора хирургического лечения обычно является «исчерпанность» всего арсенала доступных для данного случая консервативных методов.
При принятии решения о проведении хирургического лечения — радикального, но значительно более дорогостоящего, — необходимо учитывать:
Необходимость проведения экстренного хирургического вмешательства возникает при остром развитии неврологических расстройств, обусловленных компрессией спинного мозга и конского хвоста. При отсутствии радикального лечения, на фоне дальнейшего нарастания спинномозговой и полирадикулярной симптоматики, возможно развитие необратимых неврологических нарушений. Однако проведенная в экстренном порядке хирургическая операция позволяет устранить остро возникшую компрессию спинного мозга, его сосудов и конского хвоста, и обеспечить восстановление двигательных, чувствительных и тазовых функций.
Ю. В. Грачев, доктор медицинских наук
В. И. Шмырев, доктор медицинских наук, профессор
НИИ ОПП РАМН, МЦ Управления делами Президента РФ, Москва